au sommaire
Le nom scientifique « argent » vient du latin argentum qui dérive du mot grec argyros qui signifie blanc étincelant ou blanc clair. Le mot néerlandais zilver dérive de l'ancien saxon silubar qui est devenu silbar en allemand ancien et silber en allemand moderne.

Les alchimistes du Moyen Âge ont consacré l'argent, à cause de son magnifique éclat, à la déesse de la Lune (Luna)). Le tout premier symbole pour ce métal était par conséquent une demi-lune.

L'argent natif était déjà connu environ 3 500 ans avant J.-C., en Égypte et dans la région du fleuve Euphrate. Par la suite, une grande quantité d'argent a été exploitée dans les mines d'argent en Espagne, en Asie Mineure et en Grèce. Au début du Moyen Âge, l'exploitation de l'argent a commencé en Europe centrale (Allemagne, Autriche, Hongrie). Après 1500, on a importé une grande quantité d'argent d'Amérique centrale et d'Amérique du Sud. Mais si l'argent est connu depuis très longtemps, il n'en va pas de même de ses sels restés ignorés longtemps. Le nitrate fondu et coulé par Glaser pour la première fois a été nommé pierre infernale, en 1663, pour son pouvoir cautérisant.

L'argent est par importance le 68e élément constituant de l'écorce terrestre ; celle-ci en contient 7,5.10-6 % jusqu'à une profondeur de 16 kilomètres. On rencontre l'argent aussi bien à l'état natif (sous forme de métal) que dans des composés.

Les minérauxminéraux les plus importants sont :
- l'argentite : Ag2S ;
- la bromargyrite ou la bromite : AgBr ;
- la chlorargyrite ou l'argent corné : AgCl ;
- la dyscrasite : Ag3Sb ;
- la fischessérite : Ag3AuSe2 ;
- la hessite : Ag2Te ;
- l'iodargyrite : AgI ;
- la miargyrite : AgSbS2 ;
- la naumannite : Ag2Se ;
- la petzite : Ag3AuTe3 ;
- la proustite : Ag3AsS3 ;
- la pyrargyrite ou l'antimonite d'argent : Ag3SbS3 ;
- la stéphanite : Ag5SbS4 ;
- la stromeyérite : AgCuS.
L'argent apparaît également, la plupart du temps en de petites quantités, dans les mineraisminerais dont on extrait l'or, le plomb, le cuivre et le zinc.

Provenance du métal
À l'état natif, on trouve de l'argent en Allemagne, aux États-Unis, en Italie et en Bolivie. On le trouve sous forme d'Ag, probablement que les sulfures ont été réduits par l'oxygèneoxygène, on le trouve aussi sous forme d'électrum, alliage or-argent ou sous forme d'amalgameamalgame argent-mercuremercure avec jusqu'à 75 % de mercure ou encore, et pour finir, sous forme de dysérasite un alliagealliage d'argent (70-85 %) et d'antimoineantimoine.
Les régions d'exploitation les plus importantes pour les minerais d'argent se situent :
- au Mexique, au Pérou : argentite ou argyrose avec 87 % d'Ag ou cérargyrite avec 75 % d'Ag ;
- en Russie (partie asiatique), aux États-Unis, au Canada (Ontario), en Australie, au Chili, au Japon, en Chine, aux Philippines et en Afrique du Sud ;
- en Europe, on produit de l'argent en de nombreux endroits, entre autres en Saxe à partir de l'acanthite qui contient 87 % d'Ag ou de la naumannite avec 73 % d'Ag.
Il y a bien d'autres minerais possibles : proustite, polybasite, sylvanite, etc.
Les propriétés physiques de l’argent
- Il cristallise dans le système cubiquesystème cubique CFCCFC.
- Il a une densité de 10,4923 à 20 °C et de 9,51 à 960 °C (liq). Cette densité bien plus faible que celle du palladiumpalladium qui le précède dans le tableau est due à l'augmentation du rayon atomique à cause de « l'ouverture » d'une nouvelle orbitaleorbitale s pour l'électron de valenceélectron de valence.
- PF 960,5 °C, cette température est difficile à déterminer avec exactitude ; l'argent s'oxyde facilement et sa liaison avec l'oxygène fait baisser le PF.
- Hormis les propriétés métalliques traditionnelles, mentionnons que l'argent est le meilleur conducteur thermique et électrique.

- Son pouvoir réflecteurpouvoir réflecteur est très élevé mais manifeste une chute brutale à 316 nm et ceci entraîne une préférence pour l'aluminiumaluminium dans les miroirs de télescopes.
- Les films très minces - 0,1 à 0,2 micromètremicromètre - d'argent ont des propriétés particulières en optique et en électricité, entre autres et ils sont peu altérables.
- Les sols d'argent, hydrosols et organosols sont très appréciés comme catalyseurcatalyseur, pour les films et en médecine.
- Les isotopesisotopes nombreux sont radioactifs sauf deux, le 107 (qui a un isomèreisomère radioactif) et le 109, présents dans la nature dans un rapport voisin de 1.
- L'ionion le plus commun Ag+ a un rayon de 1,55Å en sels minéraux et 1,62Å en sels organiques.
- Les potentiels d'ionisationionisation sont les suivants : 7,542 V pour Ag+ diamagnétique, 21,4 V pour Ag 2+ paramagnétiqueparamagnétique et 35,9 V pour Ag 3+.
Les alliages
L'argent se mélange facilement avec les autres métauxmétaux, nous ne prendrons ici que quelques exemples parmi les plus utilisés.
Alliages binairesbinaires :
- Ag 92,5 % et Cu 7,5 %, orfèvrerie et monnaie anglaise ;
- Ag 90 % et Cu 10 %, monnaie américaine ;
- Ag 71,9 % et Cu 28,1 % (eutectiqueeutectique) brasurebrasure ;
- Ag et Pt, orfèvrerie et contacts électriques ;
- Ag et Pb, métal antifriction pour des charges élevées ;
- Ag, Zn et Ag, Cd brasure souduresoudure résistant à la corrosioncorrosion ;
- les alliages avec l'or, or pâle ou or vert, etc.
Alliages ternaires :
- Ag 20 à 30 %, Cu 35 à 50 % et Ni 25 à 30 % (ruoltz), orfèvrerie bon marché ;
- Ag, Cu, Zn pour la brasure ;
- Ag, Pb, Cu pour les alliages dentaires ;
- l'amalgame dentaire a une composition proche de : Ag 33 % - Hg 52 % - Sn 12 % - Cu 2 % - Zn 1 %.
Préparations de l’argent
- Traitement du minerai broyé par cyanuration : un procédé un peu ancien consiste à dissoudre de l'argent, à partir de minerai d'argent réduit en poudre, à l'aide de cyanure. On procède à une oxydationoxydation, 2 Ag2S + 10 NaCN + O2 + 2 H2O → 4 Na[Ag(CN)2] + 2 NaSCN + 4 NaOH. La solution d'argentocyanure est maintenue à un pH >7 et traitée par Zn et Al finement divisés. L'argent précipite, et la solution de cyanure est recyclée. L'argent recueilli est fondu, coulé en barres affinées par électrolyseélectrolyse. Soit la réaction : Al + 3 Na[Ag(CN)2] + 3 NaOH- 3 Ag (ppte) + 6 NaCN(recyclé) + Al(OH)3.
- Dans le procédé faisant appel à un amalgame, on dissout l'argent du minerai dans le mercure, comme indiqué ci-après : 2 Ag3AsS3 + 3 CuCl2 → 6 AgCl + 3 CuS + As2S3 ; AgCl + Cu + Hg → CuCl + Ag(Hg). Le mercure est éliminé par distillationdistillation. L'argent obtenu peut ensuite être soumis à une purification ultérieure. Ce procédé était auparavant toujours utilisé pour la production d'argent à partir de hornblende d'argent (AgCl).
- Le grillage chlorurant était une méthode très pratiquée au XIXe siècle et pratiquement abandonnée aujourd'hui. Le sulfure d'argent était chauffé à 600 °C en atmosphèreatmosphère oxydante en présence de sel puis, après le grillage on ajoute une solution saturée de sel. Il y avait différents procédés : Patera, Kiss, Ziervogel, par exemple.
- À l'heure actuelle, une grande partie de l'argent produit provient du recyclagerecyclage. Pour la récupération, il existe divers procédés, entre autres l'électrolyse, la précipitation avec des métaux non nobles tels que le fer ou le zinc et l'échange d'ions. On obtient principalement l'argent nouvellement produit sous la forme d'un sous-produit lors de la préparation d'autres métaux tels que l'or, le cuivrecuivre, le plomb, le nickelnickel et le zinc. La boue anodique, que l'on obtient lorsqu'on prépare des métaux, est dissoute dans de l'acide sulfuriqueacide sulfurique chaud. Le résidu, qui contient de l'argent, est porté en fusionfusion et les autres métaux éventuellement présents sont éliminés.
- L'argent brut, que l'on obtient, peut être purifié par électrolyse. On place l'argent brut pour faire office d'anodeanode (dans un sac de polypropylènepolypropylène) dans une solution de nitrate d'argent acidifiée. Lors de l'électrolyse, l'anode se dissout et de l'argent très pur (> 99,99 %) précipite sur la cathodecathode. L'argent formé est raclé et éliminé en continu. On désigne ce procédé par l'appellation « procédé de Möbius ».
Traitement du plomb argentifère
Le procédé ancien est la coupellation : chauffé en atmosphère oxydante, le plomb s'oxyde et pas l'argent.

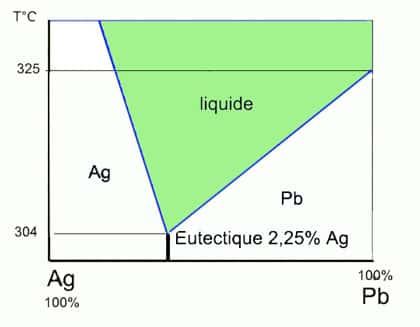
Le pattinsonage enrichit le minerai avant la coupellation : on met à profit l'eutectique en chauffant plusieurs fois. Le plomb se sépare lors du refroidissement et on rajoute du minerai avant de re-chauffer. C'est un procédé lent et coûteux.
Le procédé moderne est le zingage
L'argent est plus soluble dans le zinc que dans le plomb, le zinc et le plomb fondus se séparent en deux couches dont les compositions varient avec les températures. Aux environs de 800 °C, les deux métaux sont complètement misciblesmiscibles et, troisième élément sur lequel se base cette technique, au-dessous de leur température de fusion, les alliages argent-zinc sont plus ou moins insolubles dans le plomb saturé de zinc. L'opération se déroule en trois étapes :
- alliage ternaire Ag-Pb-Zn vers 450 degrés ;
- élimination du zinc par distillation ;
- coupellation de l'alliage Pb-Ag restant (4 % Ag). Cette dernière se fait dans des sortes de fours à réverbère portant des rigoles pour l'écoulement de la litharge qui est éliminée. Quand on atteint 1 000 °C environ, on voit apparaître l'argent métal (phénomène de l'éclairéclair) sous la litharge.

Traitement du cuivre argentifère
La récupération des métaux précieux dans les boues du raffinageraffinage électrolytique du cuivre est facile et rentable (à titre d'exemple, dans une mine de cuivre que j'ai visitée en Australie la totalité des frais salariaux était payée par la récupération annexe d'or...).
La composition des boues peut être la suivante :
- Cu 10 à 40 % ;
- Ag 10 à 50 % ;
- Au 1 % ;
- Pb 2 à 10 % ;
- Se 3 à 20 % ;
- Te jusqu'à 7 % ;
- S jusqu'à 10 % ;
- Sb jusqu'à 8 %.
On élimine le cuivre, le selenium et le tellurium par grillage oxydant vers 500 °C puis on dissout le cuivre dans l'acide sulfurique. Par coupellation à 1 200 °C, on élimine le pb, le bismuthbismuth et l'antimoine dans un premier temps puis As, Sb et Se partent sous forme d'oxydes volatils et pour finir Te et Se sont éliminés par addition de nitrate et carbonate de sodiumsodium. L'opération prend environ trois jours et le métal doré obtenu contient environ 98 % d'argent et 2 % d'or et de platineplatine, il est ensuite purifié par électrolyse (Möbius).
Obtention d’argent chimiquement pur
L'obtention d'argent chimiquement pur est très compliquée et dérive de la méthode de Stas. On dissout d'abord le métal dans l'acide nitrique. On évapore à sec. Puis fusion et décomposition des autres sels métalliques. Redisssolution dans l'eau. Cristallisation fractionnéeCristallisation fractionnée. Reprise par l'ammoniaqueammoniaque. Réduction par le sulfite d'ammoniaque à 70 °C. Fusion de AgO sur de la chaux vive dans un courant d'hydrogènehydrogène puis sous vide. On obtient enfin de l'argent pur avec moins de 4.10-5 % de Ca.





























