au sommaire
Le terme cathode fait référence à l'une des deux électrodes -- avec l'anode -- que l'on peut trouver dans un système générateur de courant -- une pile, par exemple -- ou dans un système consommateur de courant -- un bain d'électrolyse ou un quelconque composant électronique.
Attention, le terme cathode ne se confond pas avec la notion de borne positive ou négative, car selon la situation -- génération et consommation de courant --, il s'applique à l'une ou l'autre des bornes. En revanche, les électrons circulent toujours de l'anode vers la cathode.
Cathode et générateur de courant
Le sens conventionnel du courant électrique dans un circuit est orienté de la borne positive à la borne négative du générateur de courant. Mais les électrons circulent en réalité dans le sens inverse. Ils sont émis par la borne négative de cet élément dit actif et reçus par la borne positive. Cette borne-là est de fait appelée cathode.
Notez que dans le cas d'une batterie, par exemple, la cathode désigne également la borne positive, mais uniquement lorsque l'appareil fournit de l'électricité. Lorsqu'il est en charge, il se transforme en élément passif et le terme cathode désigne alors le pôle négatif de la batterie.
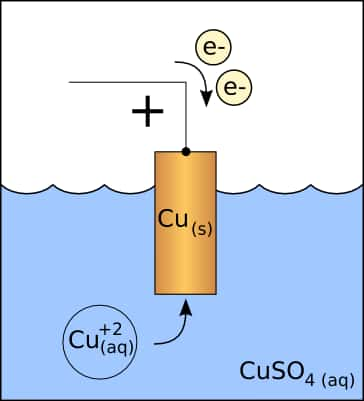
Principe de fonctionnement d’une cathode en cuivre. © Jleedev, Wikipedia, CC by-sa 3.0
Cathode et électrolyse
Lors d'une électrolyse, une réaction chimique d'oxydoréductionoxydoréduction a lieu sur les électrodes. On appelle cathode, l'électrode sur laquelle se produit une réaction réduction, une réaction qui consomme des électrons. C'est alors l'électrode reliée au pôle négatif du générateur et elle correspond donc au pôle négatif de l'électrolyseur. Petit moyen mnémotechnique : « cathode » et « réduction » commencent par une consonne. La réaction d'oxydationoxydation a quant à elle lieu sur l'anode.
Si la cathode est en cuivrecuivre (Cu), par exemple, les ionsions Cu2+ y captent des électrons du circuit extérieur. Il y a alors formation de cuivre métalmétal. La solution dans laquelle baigne la cathode perd de sa couleurcouleur bleue caractéristique. Et un dépôt de cuivre se forme sur la cathode.