au sommaire
Le récepteur de l'élastine-laminine, son rôle dans le vieillisement vasculaire
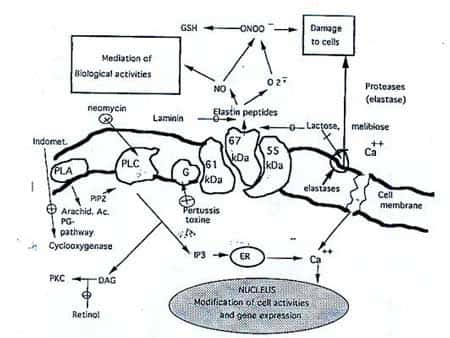
Ce récepteur comporte apparemment trois sous-unitéssous-unités (Fig. 1), dont deux transmembranaires et une, de 67 Kd environ, facile à détacher de la membrane cellulairemembrane cellulaire. Cette sous-unité est la seule qui a été clonée (16). Elle fait partie de la famille des galectines, possède un site lectinique réagissant spécifiquement avec des séquences osidiquesayant la configuration du lactoselactose.

Figure 1 : Représentation schématique du récepteur de l'élastine-laminine avec ses trois sous-unités, dont, au centre,celui de 67kD reconnaissant l'élastine, la laminine et ayant un site lectinique pour des séquences de type lactose. Indication de la voie de transmission du message vers l'intérieur de la cellule et certaines des réactions déclenchées : libération d'élastase et de radicaux libres.
D'autres sites « reconnaissent » des séquences retrouvées dans l'élastineélastine et la lamininelaminine. La présence de ce récepteur a été détectée sur des cellules mésenchymateuses (fibroblastesfibroblastes, chondrocyteschondrocytes, cellules musculairescellules musculaires lisses), des-cellules mononucléées (monocytesmonocytes, PMN, lymphocyteslymphocytes) ainsi que sur des cellules glialescellules gliales. Il paraît probable que d'autres cellules encore, comme les neuronesneurones, l'expriment aussi. Son affinité pour des peptides d'élastine (la k-élastine) est de l'ordre de nanomolaires (27). En présence de peptides d'élastine, ces cellules présentent une augmentation plus OU moins rapide de la teneur en calcium libre intracellulaire (Ca, ++)) suivie par le déclenchement de réactions cellulaires dont certaines sont énumérées dans le Tableau 1. La Pharmacologie de ce récepteur a été étudiée en détail avec Marie-Paule Jacob et Tamas Fülôp (12, 27), Gilles Faury, dans l'équipe de Jean Verdetti, a pu montrer récemment que les cellules endothéliales vasculaires expriment ce récepteur (20). En présence de peptides d'élastine à faible concentration (~ 10-8 M), on assiste a une vasodilatationvasodilatation dose dépendante, médiée par le relargage de NONO* (12). Ce phénomène apparaît au cours de l'ontogenèseontogenèse et disparaît progressivement au cours du vieillissement (13).

Tableau 1 : Réaction cellulaire déclenchée par l'activation du récepteur de l'élastine-laminine.
Le développement ontogénétique de cette réaction peut-être attribuée au rôle de chaperon de la sous-unité 67kD dans l'elastogenèse, intense aucours de la période post-natale. La perte progressive de l'effet vasodilatateurvasodilatateur médié par ce récepteur peut être attribuée à l'effet cytotoxiquecytotoxique des protéasesprotéases et radicaux libresradicaux libres dégagés par les cellules endothéliales et musculaires lisses lors de la stimulationstimulation de ce même récepteur (28). La présence d'agonistesagonistes (peptites d'élastine) augmente l'expression de protéases de types élastase (2). Les cellules mononuclées libérent le radical superoxyde aussi dans les mêmes conditions (14). La libération simultanée de NO' et de 0 27 peut résulter de la production de l'anion toxique peroxynitrite (ONOO-) dont la neutralisation exige la production simultanée de glutathion réduit (GSH). Or les défenses antiradicalairesantiradicalaires baissent avec l'âge (8). Par contre, la présence de peptides d'élastine dans le sang circulant à des concentrations saturant le récepteur (5) provoque la décharge de protéases et de radicaux libres d'une façon quasi-permanente. La présence de protéases de type élastase (métalloendopeptidase) dans le sang circulant est aussi en faveur de cette hypothèse (6). Ainsi l'action de ce récepteur impliqué dans des réactions d'intérêt biologique (Tableau 1) s'avère à la longue nuisible. Son rôle dans le vieillissement vasculaire (28) et dans celui d'autres tissus paraît probable.
Les études récentes de ce récepteur sur des lymphocytes, par Gabriella Peterszegi et Sophie Texier (23) ont confirmé cette hypothèse. En présence de peptides d'élastine dans le milieu de culture, l'expression de ce récepteur est induite dans les lymphocytes « helper » (CD4+) et à mémoire (CD45 RO + ). L'activation du récepteur provoque une accélération de la prolifération et une augmentation de l'expression et de la sécrétionsécrétion d'une sérinesérine-élastase apparemment identique à celle des PMN, donc de la série myél6ide. Cet effet stimulant du récepteur est obtenu avec une concentration de peptides d'élastine de l'ordre de 1 à 2 gg/mI. En augmentant la concentration en peptides d'élastine, on note une augmentation progressive de morts cellulaires à partir de O,l mg/ml (Fig. 2). L'étude détaillée de ce phénomène a révélé l'apparition de l'apoptoseapoptose à des concentrations élevées de k-élastine (1 à 5 mg/ml) avec environ 40 % des cellules subissant l'apoptose. A des concentrations plus faibles de k-élastine, la mort cellulaire n'est pas apoptotique, mais due probablement à des mécanismes assimilables à la nécrose (33). La laminine, dans nos expériences, inhibe aussi bien l'effet vasodilatateur des peptides d'élastine (12) que l'effet sur les lymphocytes (33). Des oligosaccharides avec un résidu de galactose en position terminale non réducteur, comme le lactose, en particulier, le mélibiose inhibent fortement la mort cellulaire (33). Cette inhibitioninhibition est attribuée à une modification conformationnelle de la sous-unité 67 kD du récepteur quand son site lectinique est occupé, abolissant affinité de son site d'agoniste pour les peptides d'élastine.
D'après nos études en cours (DEA de Sophie Texier) il apparaît que les mécanismes radiculaires et protéolytiques ci-dessus évoqués sont responsables de la mort lymphocytaire. Il apparaît donc qu'il est difficile de séparer l'effet physiologique du récepteur de l'élastine-laminine (Tableau 1) des effets pathogènespathogènes, impliqués dans le vieillissement vasculaire et tissulaire. La mise en évidence de lymphocytes exprimant ce récepteur au sein des plaques d'athéromeathérome confirme aussi notre hypothèse (23). D'autre part, ce récepteur a pu être détecté sur des cellules tumorales métastasiantes, dans nos expériences sur les cellules du cancercancer pulmonaire de Lewis (34), et dans celles de l'équipe de Sobel-Liotta sur des cellules du cancer de côloncôlon qui la surexpriment (9).
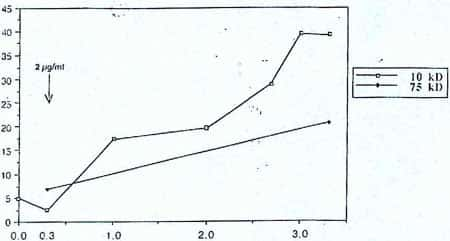
Figure 2 : Augmentation de la proportion de cellules mortes (en % sur les ordonnées) dans une culture de lymphocytes T humains, en présence de concentration croissante de peptides d'élastine (échelle logarithmique en abscisses, en lig/ml). Deux préparations de k-élastine ont été utilisées, de plus faible (10 kD moyen) et de plus haut (75 kD moyen) poids moléculaire (33).
Un autre argument en faveur de l'hypothèse invoquée provient de la perte progressive des régulations assurant l'homéostasiehoméostasie calcique des cellules, démontrée pour ce récepteur ainsi que pour le récepteur du peptide FMLP (24, 37). Cette perte, attribuée aux réactions radicalaires et protéolytiques, résulte dans une augmentation progressive de la teneur en calcium intracellulaire, phénomène impliqué dans le vieillissement vasculaire (29). La démonstration récente d'induction d'apoptose des cellules endothéliales par l'élastase des PMN conforte aussi notre hypothèse (19).