au sommaire
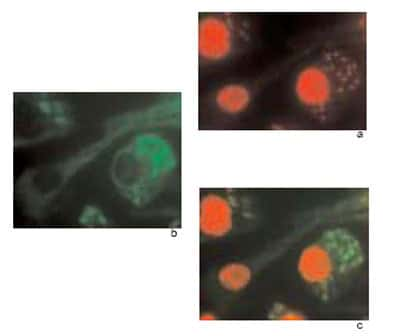
Infection de macrophages humains par le parasite Leishmania.a, marquage du noyau de la cellule et des parasites par le iodure de propidium.b, immunofluorescence avec un anticorps anti-leishmania.c, supperposition des deux images&co
Avec plus de 350 millions de personnes exposées, les leishmaniosesleishmanioses sont des affections endémiquesendémiques présentes dans plus de quatre-vingt-huit pays partout dans le monde, excepté en Océanie. Les responsables de ces maladies sont des protozoairesprotozoaires intracellulaires: les leishmanies. Ces parasitesparasites du genre Leishmania sont transmis aux hommes et aux autres mammifèresmammifères par simple piqûre d'un insecteinsecte vecteur, la femelle phlébotome. Il existe quatre formes de leishmaniose chez l'homme.
Présentant une grande variété de manifestations cliniques, elles ont toutes des conséquences très graves et certaines sont mortelles. L'absence de vaccinsvaccins et les difficultés liées au contrôle du vecteur du parasite font que la seule approche thérapeutique repose actuellement sur la chimiothérapiechimiothérapie. Les molécules utilisées de nos jours possèdent cependant de nombreuses limitations de part leur coût et leur toxicitétoxicité, mais aussi de part l'émergenceémergence de phénomènes de résistancerésistance à travers le monde, principalement à l'antimoine qui reste la molécule principale pour traiter la leishmaniose depuis près de 70 ans. Trouver de nouvelles cibles thérapeutiques pour développer des nouveaux médicaments est donc crucial pour ces parasitosesparasitoses que l'OMSOMS classe désormais parmi les infections prioritaires (catégorie 1 : infections réémergentes ou incontrôlées).
Classiquement, les approches utilisées pour caractériser de nouvelles molécules à activité antiparasitaire sont basées sur des approches empiriques qui consistent à cribler l'activité de molécules naturelles ou synthétiques sur la viabilité du parasite in vitroin vitro. L'étude du mécanisme d'action se faisant (ou non) a posteriori. Les outils moléculaires disponibles aujourd'hui permettent désormais d'identifier des gènesgènes parasitaires candidats à partir desquels desmolécules spécifiques seront synthétisées pour inhiber l'action biologique de leurs produits. Ces cibles sont généralement des gènes ou familles de gènes impliqués dans une voie biologique déterminante pour le parasite (particulièrement sous sa forme intracellulaire) et qui est suffisamment différente, voire absente, chez son hôte.
Il y a quelques années, les travaux sur le processus de vieillissement ont découvert que la restriction calorique sévère - en d'autres termes, une diète radicale - prolonge l'espérance de vieespérance de vie d'une grande variété d'espècesespèces animales. Les données récentes ont montré que dans les organismes eucaryoteseucaryotes, SIR2 (Silent Information Regulator 2) est considéré comme un régulateur universel de la longévité. Les protéinesprotéines de la famille SIR2 font l'objet de recherches intensives, notamment en cancérogenèsecancérogenèse. Un membre de cette famille de protéine a été identifié pour la première fois en 1996 chez Leishmania major.
L'intérêt grandissant pour ces protéines, a amené les chercheurs de l'lRD, en collaboration avec des équipes de l'INSERM et de l'Université de Porto au Portugal, à approfondir les connaissances sur les fonctions biologiques de SIR2 et à étudier son implication éventuelle dans les phénomènes physiopathologiques engendrés par l'infection parasitaire. Ils ont, pour cela, envisagé l'inactivation du gène SIR2 de Leishmania infantum, agent de la leishmaniose viscéraleleishmaniose viscérale. Les résultats de travaux de délétiondélétion du gène SIR2 démontrent que celui-ci est essentiel à la survie des parasites. Ceci constitue à l'heure actuelle le premier exemple montrant qu'un gène SIR2 est nécessaire à la survie d'un organisme.
De manière intéressante, lorsqu'on oblige le parasite à exprimer un niveau minimal de protéine SIR2, il est incapable de proliférer dans le macrophagemacrophage in vitro et sera progressivement éliminé au cours d'une infection expérimentale chez la souris. Bien loin des fonctions décrites chez les autres organismes, cette protéine SIR2 parasitaire pourrait dès lors être considérée comme une nouvelle cible thérapeutique potentielle. Afin d'étayer cette hypothèse, les chercheurs ont testé l'action d'inhibiteurs spécifiques des protéines de la famille SIR2 comme le sirtinol ou le nicotinamide et tous présentent une activité anti-leshmanienne sur le stade parasitaire présent chez l'hôte vertébrévertébré. Sur la base de ces résultats, les recherches proposées en collaboration avec d'autres instituts s'articulent entre l'exploitation de cloneclone (s) parasitaire (s) de virulence atténuée et la validation du produit du gène SIR2 comme cible thérapeutique chez leishmania et éventuellement d'autres parasites de la famille des TTrypanosomatidae (Trypanosoma cruzi et trypanosomestrypanosomes africains).
En effet, il est vraisemblable que les parasites de virulence atténuée seront rapidement tués chez l'hôte, ce qui constitue une source d'antigènesantigènes capables de stimuler la réponse immune. Une telle approche présente l'avantage de mimer une infection naturelle en induisant généralement une réponse immune plus efficace que les vaccins classiques. De même, les études enzymatiquesenzymatiques et la modélisation moléculaire de SIR2 peuvent apporter des informations utiles pour l'élaboration d'inhibiteurs spécifiques.