au sommaire
Les silicates sont une importante famille de minérauxminéraux qui représentent près de 95 % des constituants de la croûte terrestre. Cette famille regroupe environ 600 espèces minérales différentes, dont l'architecture atomique se caractérise par le motif structurel de base (SiO4)4-, un anionanion (ionion négatif) assemblé sous la forme d'un tétraèdre.
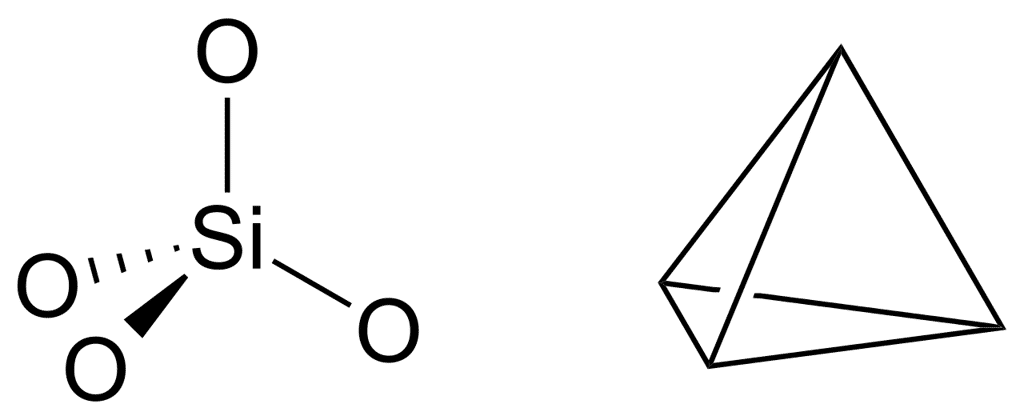
Un silicate est donc un sel composé de dioxyde de siliciumsilicium (SiO2) associé à divers oxydes métalliques : aluminiumaluminium, magnésiummagnésium, ferfer, calciumcalcium, potassiumpotassium, sodiumsodium... Ces oxydes sont des cationscations (ions positifs), qui permettent d'assurer la neutralité électrique du minéral. Le squelette atomique des silicates est donc formé par l'organisation des tétraèdres (SiO4)4-, qui se lient par les atomesatomes d'oxygène situés aux sommets. Cet agencement permet la création de structures de petites dimensions, composées de quelques groupes tétraédriques, ou de structures polymèrespolymères de taille bien plus importante. Dans ce cas, les tétraèdres s'organisent en chaînes linéaires, en rubans, en feuillets, ou sous des formes tridimensionnelles complexes. Dans ces enchaînements, il arrive que la silice soit remplacée par un atome d'aluminium. On parle alors d'aluminosilicate.
Cette variabilité de structure et l'association avec divers cations permet la création d'un nombre très important de minéraux silicatés. Ces différentes espèces minérales sont généralement classifiées suivant leur composition et l'enchaînement des tétraèdres.
Les principales espèces minérales
Les nésosilicates
Les nésosilicates peuvent être considérés comme la forme la plus simple des minéraux silicatés. Ce sont des silicates dits à tétraèdres libres, dans le sens où les tétraèdres (SiO4)4- sont réunis par deux cations bivalents : Mg (magnésium) ou Fe (fer), ou par un cation tétravalent Zr (zirconiumzirconium). Les péridots (olivine), le zirconzircon, les grenats, la topaze, le sphène mais encore l'andalousite, le disthènedisthène, la sillimanite ou la staurotide sont des nésosilicates.
La formule du zircon par exemple est donc : SiO4Zr. L'andalousite, la sillimanite et le disthène ont tous trois la même formule chimique : Al2SiO5. Ils font partie d'une sous-catégorie nommée silicate d'aluminealumine. De fait, on différencie ces trois minéraux non pas par leur composition chimique, mais par l'agencement des tétraèdres et la structure de leur réseau cristallinréseau cristallin.
Le grenat quant à lui accepte une certaine variabilité dans sa composition. De formule R32+X23+Si3O12, le site R peut ainsi être occupé par un atome de Ca, de Mg, de Fe2+ ou de Mn. Le site X peut être occupé par un atome d'Al, de Fe3+, de Ti ou de Cr.
Les sorosilicates
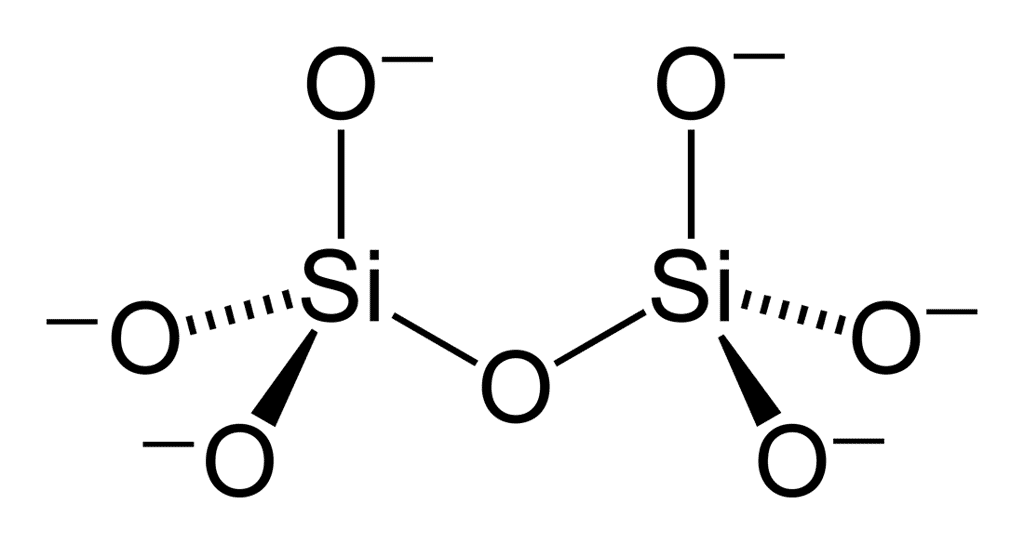
Les sorosilicatessorosilicates sont définis par des groupes de deux tétraèdres unis par un oxygène commun. La formule de base devient donc (Si2O7)6-. Il s'agit d'une espèce minérale assez rare qui comporte notamment les magnifiques épidotes.
Les cyclosilicates
Comme leur nom l'indique, les cyclosilicatescyclosilicates se définissent par une structure cyclique, les tétraèdres formant une chaîne fermée. Le radical de base est donc (SiO3)2- et la formule chimique finale du minéral va dépendre du nombre de tétraèdres dans le cycle. Les cyclosilicates les plus connus sont les tourmalinestourmalines et les béryls, qui comprennent notamment les émeraudes ou l’aigue-marine.

Les inosilicates
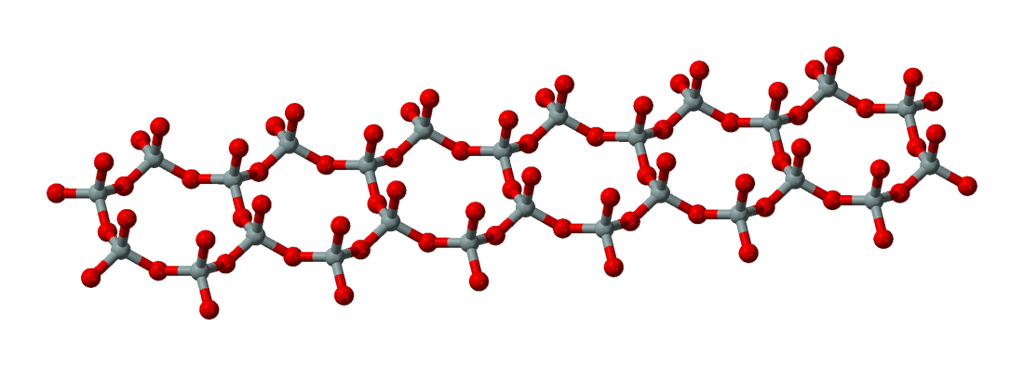
Les inosilicatesinosilicates sont formés par des chaînes de tétraèdres centrés sur l'atome de silice. Ils comportent deux grandes familles minérales : les pyroxènespyroxènes, formés par des chaînes simples de formule (SiO3)2-, et les amphibolesamphiboles, chaînes doubles de formule (Si4O11)6-.
Les phyllosilicates
Grande famille de minéraux silicatés, les phyllosilicatesphyllosilicates se caractérisent par leur organisation en couches de tétraèdres. Ceux-ci sont unis par trois de leurs sommets, formant ainsi un réseau plan. L'empilement de ces couches va donner des minéraux en feuillets ou fibreuxfibreux comme les micas, le talc ou encore les minéraux argileux. Cet agencement spécifique génère des plans de fragilité (on parle de plans de clivageplans de clivage) qu'il est facile de détacher les uns des autres.

Les minéraux argileux ont la particularité d'être composés d'empilement de couches tétraédriques et octaédriques. L'espace entre les feuillets peut contenir de l'eau et divers ions. Quand l'argileargile s'hydrate, cela fait augmenter la distance entre les feuillets : l'argile « gonfle ». Au contraire, lorsqu'elle s'assèche, l'espace entre les feuillets va se contracter. Ces variations de volumevolume lors de l'hydratationhydratation et de la déshydratationdéshydratation sont caractéristiques des minéraux argileux.
Les tectosilicates
Dans le cas des tectosilicatestectosilicates, les tétraèdres sont unis les uns aux autres par leurs quatre sommets, il n'existe aucun site libre. La formule est ainsi SiO2, ou Si4O8. Parmi les tectosilicates, citons les feldspathsfeldspaths et feldspathoïdes. Le quartzquartz, autre tectosilicate, possède la même architecture. Les feldspaths sont caractérisés par la substitution d'un ion Si4+ par un ion Al3+ dans les tétraèdres, la charge positive restante étant compensée par l'insertion d'un cation comme K, Na ou Ca. Ces variations définissent les différents types de feldspaths : potassique, sodique ou calcique.

























