au sommaire
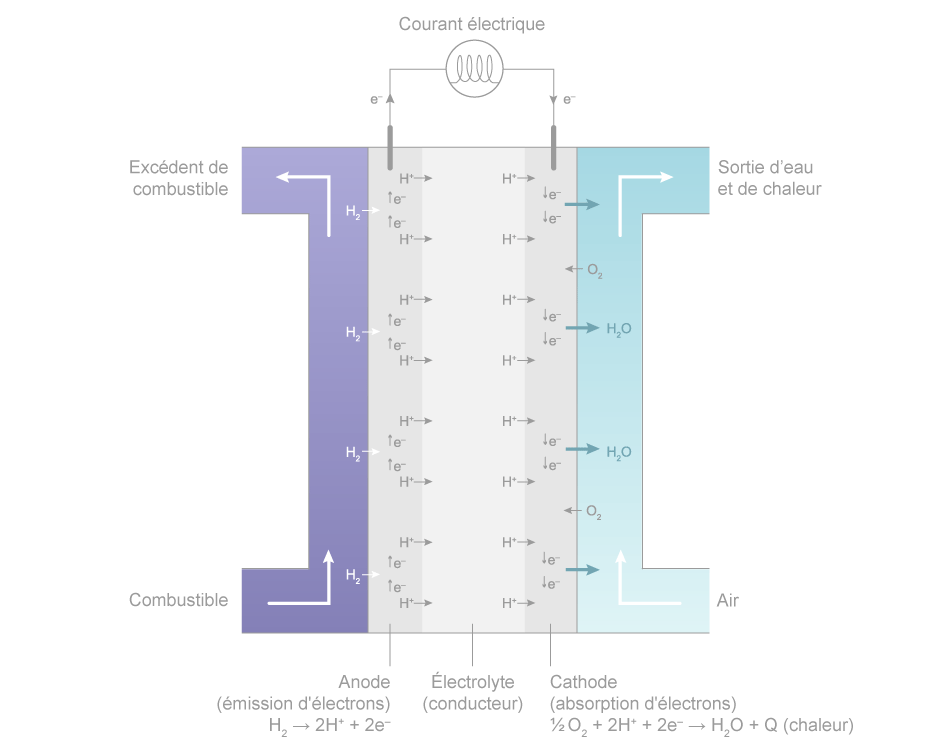
Le principe de fonctionnement de la pile à combustible repose sur l'oxydation d'un combustible (par exemple l'hydrogène) et la réduction d'un comburant (par exemple l'oxygène) aboutissant à la production simultanée d'eau, d'énergieénergie électrique (W) et de chaleurchaleur (Q). Elle est constituée par deux électrodesélectrodes (une anodeanode émettrice d'électronsélectrons et une cathodecathode réceptrice d'électrons), séparées par un électrolyte permettant le passage des ionsions. Une membrane évite la mise en contact des réactifsréactifs à l'anode et à la cathode.
À l'anode, on a donc une oxydation électrochimique de l'hydrogène : H2 → 2H+ + 2e-
À la cathode, on observe la réduction de l'oxygène 1⁄2O2 + 2H+ +2e- → H2O
Le bilan global est alors : H2 + 1/2 O2 → H2O
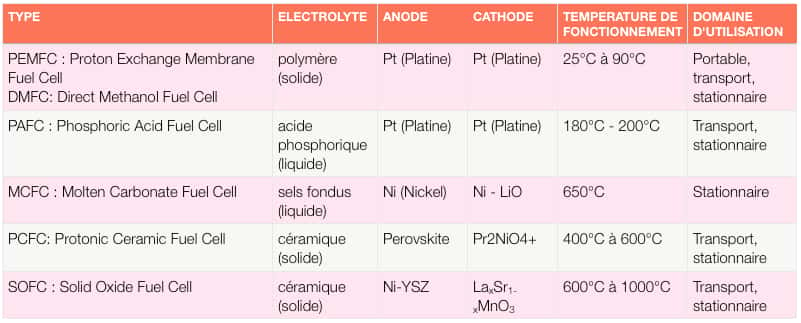
Selon les paramètres souhaités ou les applicationsapplications, il existe différents types de piles à combustible utilisant des électrolytes et des électrodes de nature différente. La PEMFC (ProtonProton Exchange Membrane FuelFuel Cell, ou pile à membrane à échange de protons) est, par exemple, utilisée par tous les constructeurs automobilesautomobiles car elle fonctionne à basse température et évite un chauffage préalable, permettant un démarrage rapide. Grâce à son électrolyte solidesolide, elle a aussi une duréedurée de vie plus longue (jusqu'à 100.000 heures) et elle est compacte, ce qui en fait également un candidat idéal pour l'électronique portable (téléphones, caméras, groupes électrogènes...)). Son inconvénient : le platineplatine, utilisé comme catalyseurcatalyseur aux électrodes, coûte très cher.
Plusieurs types de piles à combustible
Autre technologie, la MCFC (Molten Carbonate Fuel Cell), dont l'électrolyte est constitué de sels fondus et qui utilise le nickelnickel comme catalyseur, ou encore la SOFC (Solid Oxide Fuel Cell), avec un électrolyte en céramiquecéramique et qui offre un excellent rendement, supérieur à 80 %. D'autres piles font l'objet de recherches mais n'en sont pas encore au stade industriel, comme les MFC (Microbial Fuel Cell), qui produisent de l'électricité par digestiondigestion de microbesmicrobes lors du traitement des eaux uséeseaux usées. À noter que si l'hydrogène est le combustible le plus largement utilisé, il est parfaitement possible d'envisager une pile à combustible fonctionnant au méthane (Direct Methanol Fuel Cell), à l'éthanol ou au gaz naturelgaz naturel.
Les applications de la pile à combustible
Les principaux domaines d'applications de la pile à combustible sont le transport (voitures, bus, bateaux...), l'électronique (micropiles à combustible), la production d'électricité ou encore l'espace (alimentation des satellites). Silencieuses, modulaires, sans rejet de CO2 (pour les piles à hydrogène), les piles à combustible ont de sérieux atouts. Mais si l'hydrogène est produit avec des énergies fossilesénergies fossiles (ce qui est encore aujourd'hui majoritairement le cas), le bénéfice environnemental est nul. En revanche, elle pourrait s'avérer très utile comme moyen de stockage et de production à partir des énergies intermittentes, en plein essor. Autres freins : le coût élevé du platine et les problèmes de sécurité (l'hydrogène est un gaz hautement inflammable et explosif en présence d'oxygène).
























