Chez les mammifères, la rétine fait partie des rares tissus pour lesquels tout dommage est irrémédiable. Néanmoins, un mécanisme de régénération spontané chez les mammifères pourrait être activé artificiellement afin de permettre, à terme, aux patients de recouvrer la vue.
au sommaire
Le corps humain -- et de façon plus générale, celui des mammifèresmammifères -- est une admirable machine, aussi complexe que résiliente par sa capacité à guérir et cicatriser. Heureusement, nous pouvons sans crainte nous aventurer en dehors de chez nous sans redouter que la moindre égratignure ne laisse à jamais sa marque. Néanmoins, tous les tissus ne sont pas égaux dans le processus de guérison.
Si, avec les soins adéquats, la plupart d'entre eux ont la possibilité de se régénérer, il n'en va pas de même pour la rétine. Cécité, dégénérescence maculaire liée à l'âge, rétinite pigmentaire sont autant de troubles que les traitements ont plus vocation à retarder qu'à guérir ou à empêcher.
De nombreux vertébrésvertébrés à sang-froid ne rencontrent pourtant pas le même problème. Des études menées sur le poisson-zèbre, avec lequel nous partageons environ 70 % de notre génome, révèlent que celui-ci est capable de régénérer les dommages causés à sa rétine grâce à un ensemble de gènes particulier.

Une fonction perdue...
Or, bonne nouvelle : une récente découverte suggère que les mammifères posséderaient eux aussi une version (inactive) des briques nécessaires à ce type de guérison. « La régénération semble être le mode de fonctionnement par défaut, mais la perte de cette capacité s'est produite à plusieurs moments dans l'arbrearbre de l'évolution », explique Seth Blackshaw, auteur correspondant de l'étude, parue dans la revue Science.
Au sein de notre rétine se trouvent les gliesglies de Müller, des cellules de soutien qui garantissent l'intégritéintégrité structurelle et fonctionnelle des cônes et des bâtonnetsbâtonnets. Celles-ci assurent de nombreuses fonctions dont, chez certains poissonspoissons et reptilesreptiles, celle de remplacer les récepteurs endommagés.
... ou plutôt désactivée
Lorsque de nouvelles cellules doivent être fabriquées, le corps cesse momentanément de produire le facteur nucléaire I (NFI), une protéineprotéine empêchant la cellule d'accéder à certaines séquences de l'ADNADN, permettant alors aux glies de se transformer et de se diviser en récepteurs tout neufs.
Ce processus peut même intervenir chez des mammifères mais n'est généralement que de courte duréedurée, à cause de la réactivationréactivation rapide du NFI qui coupe court au travail des glies. Les chercheurs ont donc tenté de prolonger la période d'inactivité de ce facteur nucléaire chez des souris, avec des résultats étonnants.
« Dans l'ensemble, nos résultats indiquent que le potentiel de régénération existe chez les mammifères, y compris chez l'Homme, mais qu'une certaine pression évolutive l'a jusqu'ici désactivé », commente Seth Blackshaw. Ces résultats ne sont qu'une infime fraction de l'immense chemin qu'il faudra parcourir avant d'en arriver à la réparation de rétines humaines, mais ils représentent une nouvelle étape encourageante pour la biologie et la médecine.
Rétine : le renouvellement des cellules sensorielles mieux compris
Article de Marie-Céline RayMarie-Céline Ray, publié le 19 août 2019
Des chercheurs finlandais ont fait une découverte qui permet de mieux comprendre le fonctionnement de la rétine. Ils ont trouvé des protéines qui participent à la bonne santé des photorécepteurs.
Dans l'œilœil, la rétine est le tissu sensoriel qui capte les signaux lumineux afin de générer un message nerveux pour le cerveaucerveau. Les cellules sensorielles de la rétine sont en contact étroit avec une couche particulière de cellules : l'épithéliumépithélium pigmentairepigmentaire rétinien. Celui-ci la sépare de la choroïdechoroïde, une des enveloppes de l'œil.
L'épithélium pigmentaire rétinien, même s'il n'est pas constitué de cellules sensorielles, joue un rôle important dans la vision : il sécrète des facteurs de croissancefacteurs de croissance, fournit des nutrimentsnutriments aux photorécepteurs, élimine des déchetsdéchets et absorbe de la lumièrelumière.
Le saviez-vous ?
Les cellules sensorielles de la rétine sont les cônes et les bâtonnets. Ces cellules allongées possèdent d’un côté un segment photorécepteur externe, et de l’autre côté, une terminaison synaptique.
Pour conserver une bonne vision au fil du temps, il est important que les cellules sensorielles de la rétine se renouvellent. Ce renouvellement est possible grâce à des phagocytosesphagocytoses qui ont lieu au niveau de l'épithélium pigmentaire rétinien : des parties des cellules sensorielles sont éliminées et « ingérées » par la couche de cellules de l'épithélium pigmentaire adjacent, grâce à un mécanisme de phagocytose qui est essentiel à la vision. Les maladies qui touchent la rétine, comme la DMLA (dégénérescence maculairedégénérescence maculaire liée à l'âge), sont une cause majeure de malvoyance. Dans la DMLA, cette phagocytose ne fonctionne pas correctement, d'où l'importance de mieux comprendre ce phénomène.
Des canaux impliqués dans les messages électriques et la phagocytose
Dans cette étude parue dans la revue BMC Biology, les chercheurs de l'université de Tampere (Finlande) se sont intéressés aux cellules de l'épithélium pigmentaire rétinien. Dans ces cellules, ils ont trouvé des moléculesmolécules spécifiques des tissus électriques comme le cœur et le système nerveux : des canaux sodiumsodium voltage-dépendants. Ces protéines caractéristiques des cellules excitables génèrent des signaux électriques au niveau des neuronesneurones.
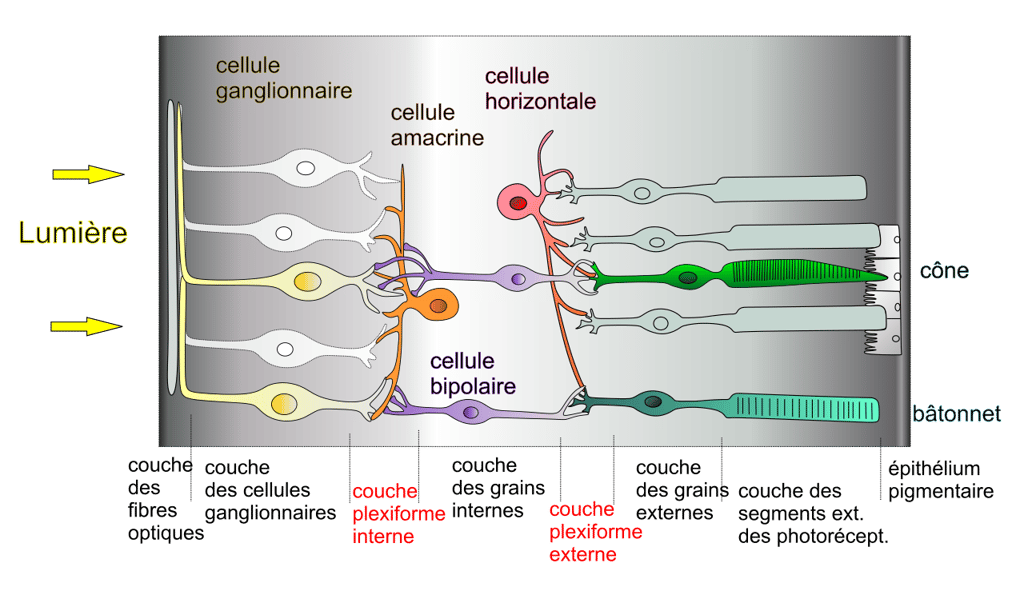
Plusieurs types de canaux sodium voltage-dépendants étaient présents dans des épithéliums pigmentaires rétiniens de souris ou dérivés de cellules embryonnaires humaines. On peut donc se demander si cet épithélium est capable de produire un signal électrique, alors que ce tissu était plutôt considéré comme « inactif » du point de vue électrique.
De plus, les chercheurs ont découvert que ces mêmes canaux influencent le processus de phagocytose de l'épithélium rétinien. Plus précisément, les canaux sodium sont impliqués dans la phagocytose du segment externe photorécepteur des cellules sensorielles de l'œil. Si les canaux sodium sont inhibés, la phagocytose est gênée. Ces canaux ioniquescanaux ioniques sont donc impliqués dans le renouvellement des cellules sensorielles de la rétine.
Cette découverte pourrait aider à trouver de nouveaux traitements contre des maladies dégénératives de la rétine comme la DMLA.