au sommaire
Redonner la vue à des aveugles pourrait devenir une réalité. Des essais cliniques prometteurs sont en cours pour restaurer la vision chez les non-voyants atteints de pathologies de la rétine (rétinite pigmentaire, dégénérescence maculairedégénérescence maculaire, etc.)), avec une efficacité tout de même très relative. L'un d'entre eux porteporte sur l'utilisation de cellules souches embryonnaires, les autres jouent quant à eux la carte de l'électronique avec des implants rétiniens artificiels.
Ces procédés font appel à une technologie de pointe et consistent en une série d'électrodesélectrodes remplaçant les cellules photoréceptrices défaillantes de la rétine. La lumièrelumière excite les photodiodes, qui transmettent un message au cerveau via le nerf optique, permettant à l'organe de former une image. Le nombre d'électrodes étant relativement faible, la résolutionrésolution est de basse qualité et les personnes testées discernent seulement la forme d'un objet, une aide dans la vie courante, mais qui ne leur donne pas encore la possibilité de lire un livre. Comme pour tout objet électronique, ces implants nécessitent une alimentation en énergieénergie, se matérialisant par des câbles qui sortent de la tête et qui manquent cruellement d'esthétisme.
De la caméra jusqu’à l'implant rétinien autonome
Des scientifiques de l'université de Stanford (Californie) viennent de tester chez le rat un nouveau modèle qui pourrait surpasser les rétines artificielles en phase de test, comme ils le révèlent dans Nature Photonics. Grâce à des photodiodes semblables à des minuscules panneaux solaires, ils peuvent convertir l'énergie lumineuse en énergie électrique, et fonctionnent donc sans source d'alimentation extérieure. Mais le travail est encore très préliminaire.
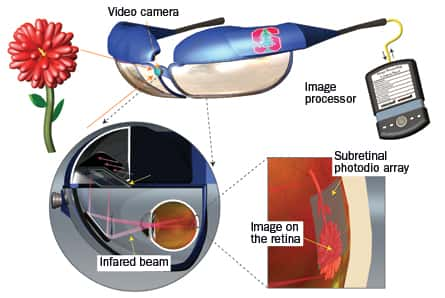
Ce schéma récapitule le fonctionnement du système. L'image est captée par une caméra placée au milieu de lunettes sophistiquées. L'information est traduite par un ordinateur (Image processor) : c'est le seul câble du dispositif et il est externe à l'individu. Des rayons infrarouges (Infrared beam) sont produits et envoyés dans la rétine de manière à exciter des photodiodes (Subretinal photodio array). Le corps se charge du reste. © James Loudin, Nature Photonics
Le principe est le suivant. Une caméra miniature est placée au milieu de lunettes vidéo de haute technicité, reliées à un ordinateurordinateur de la taille d'un téléphone portable, chargé d'analyser les images obtenues. Un rayonnement lumineux, du domaine proche infrarougeinfrarouge et émis par les lunettes, passe dans l'œil et active ensuite des photodiodes en siliciumsilicium. Celles-ci perçoivent le stimulus visuel et génèrent un courant électriquecourant électrique qui stimule les neuronesneurones rétiniens, plus utilisés mais toujours vivants. L'information remonte alors le nerf optique jusqu'au cerveaucerveau, qui la traduit en image.
Une meilleure résolution pour une meilleure vision ?
Les photodiodes sont en plus microscopiques : elles mesurent 70 µm de diamètre, soit un tiers de l'épaisseur d'un cheveu humain. Elles permettraient une meilleure résolution et donc une meilleure vision. Mais il faut parler au conditionnel, car le dispositif a été testé sur des rats morts et vivants, et il est difficile d'évaluer précisément l'apport de l'implant dans la vue.
James Loudin, l'un des auteurs, croit en l'intérêt de sa découverte : « Les chirurgiens devraient être plus heureux avec nous. Nous proposons juste un seul implant. Les autres approches requièrent des pièces logicielles assez grosses à placer dans le corps ». Il n'est pas contredit par Eberhart Zrenner, chercheur à l'université de Tübingen, qui a développé un implant utilisé dans un essai cliniqueessai clinique international testé chez 66 sujets, évoquant « une approche élégante ».
Le principe semble validé, mais il reste encore beaucoup de travail pour améliorer le dispositif, notamment dans la biocompatibilité du matériel, sa stabilité et la mise au point de procédures chirurgicales plus sûres. Tant que ces conditions ne seront pas remplies, l'évaluation chez l’Homme n'est pas envisageable.