au sommaire
Auto-assemblage
Nous avons découvert de manière fortuite cette aptitude singulière des molécules du nucléotidenucléotide G (ou 5'-GMP en termes techniques) à former spontanément des assemblages ordonnés. Nous avions pris pour modèle d'ARNARN, substratsubstrat normal d'une importante enzyme, la ribonucléase, le 5'-GMP; et avons alors constaté une légère anomalieanomalie dans les mesures, conduites dans l'eau, bien entendu. Cette irrégularité s'expliquait très bien, si on supposait qu'un certain nombre, n, de molécules de G venaient s'agglutiner les unes aux autres en des agrégats Gn.

Ribonucléase
Il s'agissait du sel sodique G2_, 2 Na+. La technique d'observation était la résonance magnétique nucléairerésonance magnétique nucléaire du sodium-23, l'isotope naturel, dont l'abondance est 100%. Lorsque les ions Na+ sont sans autre attache que les six molécules d'eau qui les entourent, ils donnent un pic très fin, de largeur quasi nulle, à peine quelques HzHz. Par contre, lorsque les ions Na+ viennent se fixer sur des agrégats Gn, la largeur de raie pourra atteindre plusieurs kHz. Or, on la mesure aisément à ± 5% près. Cette méthode d'observation est donc bien choisie pour suivre le passage du désordre à l'ordre.
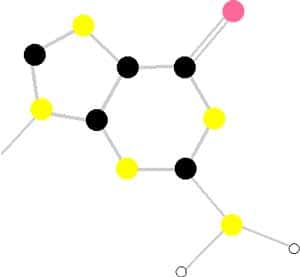
On constate, à température donnée, que si l'on augmente la concentration en G2-,2Na+ les paramètres d'ordre que sont, non seulement la largeur de raie mais aussi sa position (fréquencefréquence de résonance), varient brusquement à partir d'une certaine concentration critique. Au dessous de cette concentration, les G sont isolés. Au dessus de cette concentration, les G se sont assemblés en des Gn. On savait déja que le 5'-GMP forme des gelsgels solidessolides aux pH acidesacides. Leur entité de base provient de ce que quatre G mettent leurs quatre guaninesguanines aux quatre sommets d'un carré. Cette structure d'un tétramère centrosymétrique est d'une grande stabilité, les quatre bases nucléiquesbases nucléiques sont maintenues ensemble par huit liaisons hydrogèneliaisons hydrogène au total. Une liaison hydrogène maintient, peu fortement, trois atomesatomes en ligne droite: un atome d'hydrogène, à charge électrique partielle positive, sert de glu pour deux atomes à charge partielle négative.
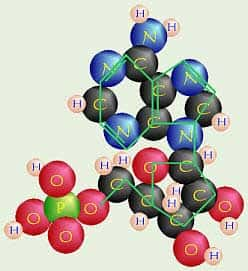
Nucléides
Les quatre guanines ainsi réunies délimitent, à l'intérieur du carré, une cavité, ayant elle aussi la forme d'un carré, aux sommets faits des quatre atomes d'oxygèneoxygène venant des quatre guanines.
Les dimensions de ce carré sont environ 3,8 Å de côté, et donc 5,5 Å en diagonale. Cela rend la cavité centrale apte à recevoir un cationcation Na+, puisque la somme du diamètre de l'ion sodium Na+ (1,90 Å) et de la taille pertinente de deux atomes d'oxygène (2,80 Å), soit 4,70 Å est légèrement inférieure. Ainsi s'explique le gros changement de la fréquence de résonance. Un ion sodium, de charge positive, venant se mettre dans la logette centrale des tétramères, perd tout ou partie de sa sphère d'hydratationhydratation en échange de la stabilisation électrostatiqueélectrostatique reçue de sa fixation sur les quatre oxygènes,à polarité négative.
Les dimensions d'un cation potassiumpotassium K+ sont mieux adaptées encore à l'insertion au cœur des tétramères G4, avec 5,46 Å pour une cavité de, répétons-le, 5,35 Å. En présence d'ions potassium, l'agrégation en une structure ordonnée se fait à des concentrations en G largement inférieures à celles nécessaires pour observer, avec le sel de sodium, une transition ordre-désordre. On peut montrer aussi l'unicité des agrégats alors formés, ce sont des entités de taille fixe. Laquelle?
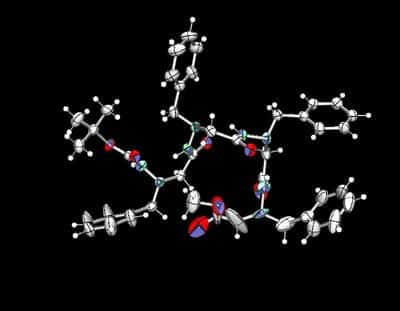
Tétramères
Nous avons pu rendre compte de toutes les données par un modèle assez simple. En premier lieu, quatre G forment un tétramère G4. Celui-ci encapsule un cation potassium. L'entité résultante G4, K+ attire un second tétramère G4. Le cation potassium interagit à présent avec huit atomes d'oxygène dans le complexe résultant G8,K+. Il s'agit de deux tétramères, superposés dans des plans parallèles, à une distance de 3,3 Å, la même que celle entre plateaux de bases dans l'ADNADN. Cette entité G8,K+ possède à son pourtour huit groupements phosphatephosphate, à double charge négative chacun. Une répulsion électrostatique considérable s'exerce entre eux. La structure G8,K+ achève donc de se stabiliser en s'attachant des ions sodium sur son pourtour: il est remarquable qu'une structure si peu élaborée, si rudimentaire en comparaison des systèmes moléculaires biologiques, s'est déja dotée d'une fonction assez complexe (et qu'on associerait volontiers à la cellule vivante), celle du tri et de la ségrégationségrégation spatiale des cations univalents K+ et Na+.
D'un autre point de vue, la formation de G8,K+, nNa+ (n=4, nous l'avons établi) atteste d'une belle synergiesynergie entre les deux espècesespèces, potassium et sodium. Pour revenir aux agrégats sodiques initiaux, ils sont faits en majorité d'octamères, similaires à ceux formés en présence de potassium, avec cinq sites de fixation du sodium ( un site de cœur, et qutatre sites périphériques); coexistant avec des hexadécamères, ayant le double, 10 sites de fixation du sodium.
Avant d'envisager la ou les significations biologiques de ces résultats in vitroin vitro, il n'est sans doute pas inutile d'évoquer la petite histoire de l'établissement, et de la publication des conclusions ci-dessus. Bruno Latour l'a montré de manière convaincante, les chercheurs scientifiques sont mus davantage par l'ardente obligation de publier pour "survivre" (obtenir des crédits, des promotions, des invitations et distinctions honorifiques) que par le seul désir tenace de découvrir les secrets de la nature.