au sommaire
Seule l'eau sous état liquideétat liquide peut donc engendrer des réactions chimiques nécessaires à la vie. On peut alors se demander si les caractéristiques de l'eau liquide sont communes à tous les liquides.

Les caractéristiques chimiques des liquides
Tous les liquides se valent-ils du point de vue de la chimie ? Loin de là ! Supposons qu'on souhaite mélanger deux espècesespèces ensemble dans un liquide tel que de l'huile, afin de les faire réagir. L'espèce la plus lourde tend à se déposer au fond, tandis que celle la plus légère tend au contraire à surnager. Finalement, les deux espèces restent séparées et ne peuvent pas réagir efficacement.
Mélangeons maintenant ces deux espèces dans de l'eau. La molécule d'eau a une propriété intéressante : elle possède un côté chargé positivement, et l'autre chargé négativement. On dit que c'est une molécule « polaire ».
Grâce à l'attraction électrostatiqueélectrostatique due à ces charges, elle tend à se « coller » à beaucoup d'autres espèces.
Ainsi, si on met de l’alcool dans de l'eau, les molécules d'eau vont s'empresser d'entourer chaque molécule d'éthanol : l'alcool se retrouve dissous dans l'eau. Bien qu'il soit plus léger que l'eau, l'alcool ne surnage pas au-dessus : il apparaît un unique mélange eau + éthanol, chaque molécule d'éthanol étant étroitement « collée » aux molécules d'eau. Si ce n'était pas le cas, les premiers à déboucher une bouteille de vin boiraient de l'alcool pur, tandis que les suivants se contenteraient du jus de raisinraisin se trouvant au-dessous...
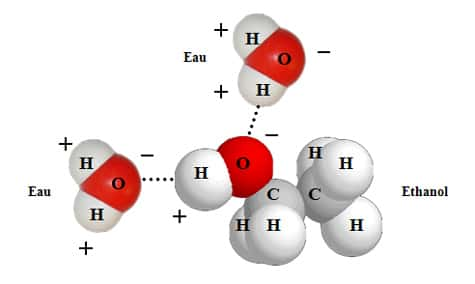
Grâce à sa polarité, l'eau peut ainsi dissoudre de nombreuses molécules, qui se retrouvent en présence sur tout le volume de solution : cela permet à ces molécules de se rencontrer au sein du liquide, et de réagir de façon efficace, ce qui explique l'importance de l'eau liquide dans le développement de la vie.

Précisons enfin que du fait de leur polarité, les molécules d'eau se collent aussi entre elles, et pas seulement aux autres espèces. Cela explique que l'eau soit liquide à la pressionpression et à la température ambiantes : dans un liquide, les molécules « glissent » les unes contre les autres, alors que dans un gazgaz elles sont séparées et suivent chacune leur propre chemin.
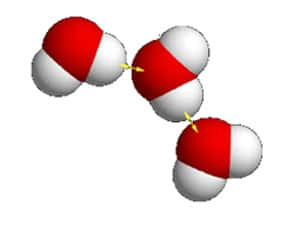
Ainsi, l'airair est gazeux parce que N2 et O2 ne sont pas des molécules polaires (elles ne se collent pas les unes aux autres). L'eau est liquide parce que les molécules H2O sont polaires et « aiment le contact »...