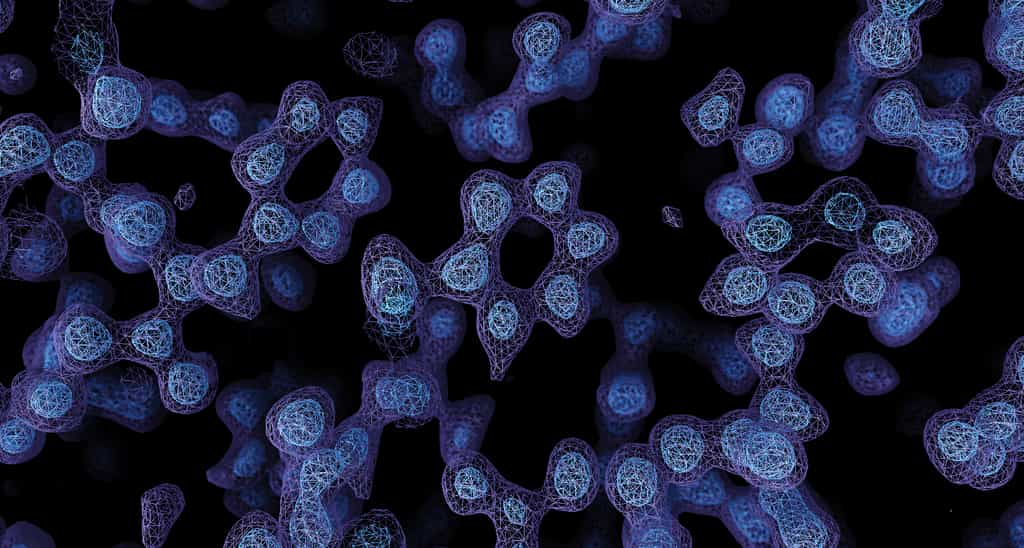
Grâce à la cryo-microscopie électronique (cryo-ME) et à des logiciels d’amélioration d’image avancés, deux équipes de chercheurs sont parvenues à observer les atomes d’une protéine avec un niveau de détail inégalé. Ils ont ainsi pu observer des structures inédites des molécules, ouvrant la voie à la conception de médicaments ciblés.
au sommaire
Jamais une protéineprotéine n'avait été observée avec un tel niveau de détails. Deux équipes de chercheurs de l'Institut Max-PlanckPlanck de chimie biophysique de Göttingen (Allemagne) et du Laboratoire de biologie moléculairebiologie moléculaire du Medical Research Council (MRC-LMB) à Cambridge (Royaume-Uni), ont pu discerner des atomes individuellement dans une protéine avec une précision d'environ 1,25 angström (0,125 nanomètre).
« C'est une étape décisive : nous avons franchi la dernière barrière de résolutionrésolution », s'est félicité Holger Stark, chercheur à l'Institut Max PlanckMax Planck et auteur principal d'une des deux études décrivant la prouesse et toutes deux mises en ligne sur le site de pré-publication BioRxiv. « C'était comme si on avait enlevé la poussière sur nos yeuxyeux », a renchéri son collègue Radu Aricescu du MRC-LMB.
La cryo-ME, une technique qui a révolutionné la vision de l’infiniment petit
Un exploit réalisé grâce à la cryo-microscopie électronique (cryo-ME) inventée dans les années 1990 et pour laquelle le Suisse Jacques Dubochet, le Britannique Richard Henderson et l'Américain Joachim Frank ont reçu le prix Nobel de chimie en 2017. La cryo-ME a été constamment améliorée grâce notamment au perfectionnement des nanotechnologiesnanotechnologies et des logicielslogiciels d'analyse d'image. Elle a, par exemple, permis de dévoiler la structure du virus Zikavirus Zika en 2016, ou celui de la denguedengue.
Le saviez-vous ?
Contrairement à un microscope optique, qui utilise la lumière, le microscope électronique accélère et concentre un faisceau d’électrons afin de créer une image de l’échantillon à observer. Le problème est que cette technique nécessite de colorer ou de déshydrater les échantillons, ce qui dégrade leur qualité. Pour éviter ce processus, la cryo-ME consiste à congeler très vite les échantillons à -190 °C dans de l’éthane liquide, ce qui préserve leur structure.
“À cette échelle, chaque demi-angström ouvre la porte vers un univers entier”
Les chercheurs de Max-Planck et du MRC-LMB ont franchi la dernière étape de cette amélioration en atteignant le niveau atomique. Ils ont travaillé sur l'apoferritine, une protéine stockant le fer et qui possède une excellente stabilité semblable à celle de la roche. À l'aide de différents procédés, notamment un instrument garantissant une vitesse égale des électronsélectrons et un logiciel de réduction de bruit, ils sont arrivés à obtenir une image très complète : « Nous pouvions déceler les atomes d'hydrogènehydrogène individuellement, à la fois dans la protéine et dans les moléculesmolécules d'eau environnantes », explique sur le site Nature Sjors Scheres, biologiste au MRC-LMB. La « carte » de la protéine, reconstituée à partir de plus d'un million d'images, offre ainsi une résolution de 1,25 angström, contre 1,54 angström pour le précédent record. La différence parait a priori minime, mais à cette échelle, « chaque demi-angström ouvre la porteporte vers un universunivers entier », insiste Radu Aricescu.
Résolution au niveau atomique de l’apoferritine grâce à la cryo-ME. © Sjors Scheres
Une mine d’or pour la conception de médicaments sans effets secondaires
Les chercheurs ont également testé leur méthode sur une molécule appelée récepteur GabaGaba(A), que l'on trouve dans la membrane des neuronesneurones et constituée d'unités gycoprotéiques. Ce récepteur est la cible de nombreux médicaments, dont des anesthésiquesanesthésiques et anti-anxiolitiques. L'image a révélé des détails jusqu'ici inédits, comme les molécules d'eau à l'intérieur de la vésicule contenant l’histamine, un neurotransmetteurneurotransmetteur agissant sur l'excitation impliquée dans de nombreuses pathologiespathologies allergiques. Ce type d'observation constitue « une mine d'or pour la conception de médicaments basés sur la structure des molécules, explique Radu Aricescu. Elle montre comment un médicament déplace les molécules d'eau, ce qui peut générer des effets secondaires ».
1 angström, le seuil infranchissable ?
Les chercheurs n'ont pour l'instant pas encore réussi à obtenir une cartographie complète du Gaba(A), car ce dernier est beaucoup moins stable que l'apoferritine. Selon les chercheurs, l'amélioration de la préparation des échantillons est d'ailleurs la dernière marge de manœuvre possible pour descendre à une taille encore inférieure. « Il sera presque impossible d'atteindre un chiffre situé en dessous de 1 angström avec la cryo-EM », estime Holger Stark. « Cela nécessiterait plusieurs centaines d'années d'enregistrement de données et une quantité non réaliste de puissance de calcul et de capacités de stockage », d'après son équipe. La limite n'est donc pas tant biologique que technologique.
Un microscope électronique à la résolution record !
Article de Jean-Luc GoudetJean-Luc Goudet publié le 21/01/2008
Un demi-angström de résolution ! Ce record mondial a été obtenu avec un microscope électroniquemicroscope électronique à transmission assez classique mais doté de plusieurs perfectionnements, dont un système de correction de l'aberration sphériqueaberration sphérique.
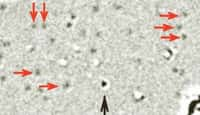
Des atomes d'or apparaissant comme autant de petits points nettement séparés les uns des autres : l'image remarquable démontre incontestablement la performance du Team 0.5, dont la résolution atteint un demi-angström (0,5 x 10-10 mètre). Ce microscope électronique à transmission a été mis au point au National Center for Electron Microscopy (NCEM) du Lawrence Berkeley National Laboratory. L'engin n'est encore qu'un prototype mais il sera tout de même utilisable par des chercheurs au mois d'octobre prochain et la version suivante, Team 1, sera mise en service en 2009.
Comme tout microscope électronique à transmission (MET, ou, à l'anglaise, TEM, préférable pour éviter la confusion avec le microscope à effet tunnelmicroscope à effet tunnel, à l'acronyme identique), le Team 0.5 utilise un faisceau d'électrons focalisé sur l'échantillon, qu'il traverse. Des électro-aimantsaimants assurent ensuite le grossissement. Le principe est similaire à celui d'un microscope optiquemicroscope optique classique, les électro-aimants jouant le rôle des lentilleslentilles.
L'équipe du Team Project (qui s'appuie sur trois laboratoires et deux sociétés privées) a ajouté plusieurs améliorations, dont des circuits électroniques aux signaux rigoureusement stabilisés et une source d'électrons puissante. Mais le secret réside surtout dans une correction de l'aberration sphérique, un défaut connu aussi en optique, qui transforme l'image d'un point en un petit disque. Il impose une limite à la résolution, c'est-à-dire la capacité à distinguer deux points très proches.

Cette aberration sphérique est corrigée par un circuit électronique, de manière active, en modifiant suffisamment rapidement la focalisation du faisceau quand le défaut est détecté. Le principe évoque celui (complètement différent) de l'optique adaptative des grands télescopestélescopes, qui déforment en permanence leur miroirmiroir pour compenser l'effet des turbulencesturbulences de l'atmosphèreatmosphère.
« La correction de l'aberration sphérique dans un microscope électronique est longtemps restée une possibilité théorique, explique Uli Dahmen, membre de l'équipe. Elle n'a pu devenir réalisable que récemment grâce à des circuits électroniques plus stables et des ordinateursordinateurs rapides permettant un ajustement continu en temps réel. » Des dispositifs de correction existent déjà et sont même commercialisés mais celui équipant le Team 0.5 se révèle bien plus efficace.
Il améliore également le contrastecontraste et le rapport signal-bruit, ce qui permet de réduire la puissance du faisceau d'électrons, un avantage intéressant en microscopie électronique. En effet, pour augmenter la résolution (donc le grossissement final), l'observateur doit pousser la puissance (exprimée en kilovolts, indiquant la tension appliquée aux bornes du filament émettant les électrons). Si l'échantillon est fragile, ce déluge électronique a alors tendance à le déformer voire le détruire. Combien de biologistes utilisateurs de TEM ont ainsi vu sous leurs yeux se déchirer la délicate coupe de résine dans laquelle était inclus leur précieux matériel... « Un faisceau électronique de faible énergieénergie a une grande longueur d'ondelongueur d'onde, explique Uli Dahmen. Il est donc plus difficile à focaliser. La correction de l'aberration sphérique permet une résolution inférieure à l'angström avec un excellent contraste, même à 80 kilovolts. » Les gros utilisateurs de TEM sauront apprécier...
Bientôt la troisième dimension
La correction d'aberration du Team 0,5 a également été testée dans un autre mode d'utilisation de la microscopie électronique à transmission, dans lequel l'échantillon n'est pas soumis à un large faisceau mais balayé par un faisceau étroit. On parle de microscopie électronique à balayage à transmission, ou Stem (scanning transmission electron microscopy)), à ne pas confondre avec la microscopie électronique à balayage.
L'équipe du Team 0.5 veut maintenant aborder la troisième dimension, une possibilité connue des TEM. L'échantillon pivote légèrement de sorte que l'angle d'observation se modifie. La succession d'images obtenue permet ensuite la reconstitution d'une vue en 3-D. Avec une résolution d'un demi-angström, il deviendrait possible de voir pour la première fois un atome. Uli Dahmen devient enthousiaste : « Cela nous amène tout prêt de réaliser le défi lancé par le fameux physicienphysicien Richard FeynmanRichard Feynman en 1959 : analyser n'importe quelle substance chimique simplement en la regardant. »
Un autre objectif, qui devrait devenir réalité dans le Team 1, est de corriger également l'aberration chromatiqueaberration chromatique, un défaut auquel est sensible un microscope électronique, bien qu'il ne montre pas les couleurscouleurs. Cette aberration vient d'une réfractionréfraction différente du faisceau selon sa longueur d'onde. Jamais réalisée sur un MET, cette fonction nouvelle « augmenterait la hauteur du microscope de 60 centimètres ». L'engin mesurant déjà plus de deux mètres, il est clair que le Team 1 ne sera pas un microscope de poche...