au sommaire
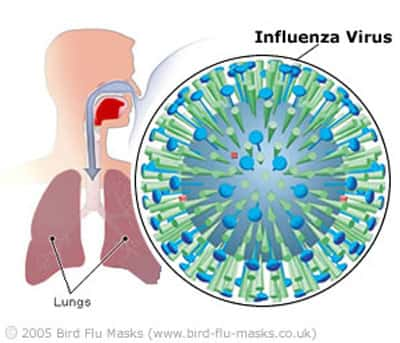
Transmission du virus de type A : oiseaux, mammifères et hommes
Le virus de type A se transmet entre les oiseaux et les mammifèresmammifères. Comment se fait la contaminationcontamination de l'homme ?

Transmission de la grippe. © Bird Flu Masks
Transmission des virus grippaux de type A
D'une façon générale chez les oiseaux, le virus est excrété au niveau des voies respiratoires, de la conjonctive et des excréments ; la transmission se fait par contact direct avec d'autres animaux infectés, ou indirect dans un environnement contaminé par les fientesfientes, les plumes.
La transmission verticale n'est pas établie, même si l'on a pu mettre en évidence la contamination d'œufs au cours d'une épidémieépidémie de grippe aviaire en Pennsylvanie (Cappucci, Johnson et al. 1985 10)). Récemment, un virus A (H5N1H5N1) proche antigénétiquement du virus de Hong Kong de 1997 a été isolé dans des œufs de canard et d'oieoie sauvages (Li, LinLin et al. 2006 34).
La transmission interhumaine des virus influenzavirus influenza de type A se fait par inhalationinhalation d'aérosolaérosol de particules infectieuses, par contact direct ou peut-être indirect, par autoinoculation au niveau de la conjonctive et des voies respiratoires. Elle est d'autant plus efficace en milieu confiné ou clos.
Transmission des virus aviaires aux Mammifères
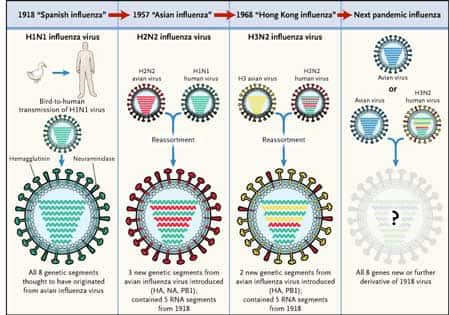
Habituellement, les virus grippaux aviaires n'infectent pas l'homme. Cependant, le XXe siècle a connu trois pandémiespandémies de grippe, toutes dues à des virus grippaux émergentsémergents d'origine aviaire. Les souches virales responsables des pandémies de 1957 et 1968 sont apparues en Asie du sud-est, à l'occasion d'un réassortiment entre des gènesgènes d'origine aviaire et ceux de la souche humaine circulante, responsable des épidémies saisonnières. Il en serait différent pour la souche responsable de la grippe espagnolegrippe espagnole de 1918 : des études ont suggéré la transmission directe à l'homme d'un virus aviaire avec adaptation chez l'homme ou d'autres mammifères (le porc par exemple qui peut héberger des virus humains et des virus aviaires et servir d'hôte intermédiaire (Taubenberger, Reid et al. 2005 55) (Taubenberger, Reid et al. 1997 54).
Depuis 1997, on a régulièrement mis en évidence des cas de contamination humaine directe et indirecte (Capua and Alexander 2002 11) (Banks, Speidel et al. 1998 6). Les premières études virologiques menées dans le cadre de l'épidémie de grippe du pouletgrippe du poulet de Hong Kong, en 1997 (Claas, De et al. 1998 15), ont clairement établi le passage direct à l'homme du virus A (H5N1), totalement d'origine aviaire.
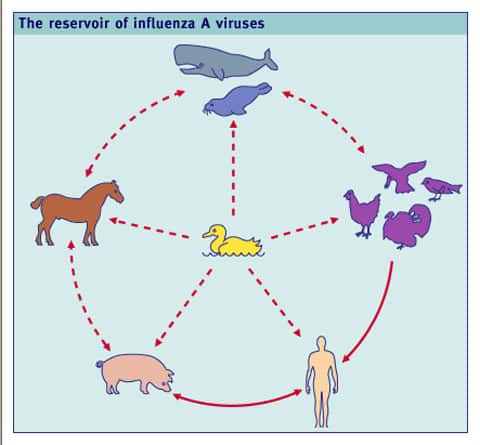
Réservoir des virus influenza A. © Lippincott Williams et Wilkins, Philadelphia
Chez d'autres mammifères, l'infection naturelle par les virus influenza aviaires est peu connue. Des études antérieures datant des années 1970-1980 chez le chat, le furet et le porc, ont démontré la capacité des virus d'origine aviaire à se répliquer dans les tissus pulmonaires, sans manifestation de virulence : l'administration intranasale de virus influenza de type A et B est responsable d'une infection asymptomatique, avec sécrétionsécrétion d'anticorpsanticorps et présence de virus grippal au niveau des voies respiratoires (Hinshaw, Webster et al. 1981 23).
Par contre, le pouvoir pathogènepathogène du virus influenza A (H5N1) est documenté chez le singe (Kuiken, Rimmelzwaan et al. 2003 32), la souris (Bright, Cho et al. 2003 9), le porc (Choi, Nguyen et al. 2005 14), le furet (Govorkova, Rehg et al. 2005 20) ; ils sont utilisés comme modèles expérimentaux dans l'étude de la pathogénie chez l'homme (Rimmelzwaan, Kuiken et al. 2003 45). Les félidésfélidés étaient jusqu'ici considérés comme résistants aux virus influenza A (Keawcharoen, Oraveerakul et al. 2004 27).
Les premiers cas connus d'infection naturelle chez le tigretigre et le léopardléopard datent du début 2004. Ils concernent quatre animaux d'un zoo de Thaïlande chez lesquels le virus influenza A (H5N1) a pu être isolé des tissus pulmonaires. Les séquences génétiquesgénétiques des isolats, hormis une modification au niveau de la position 627 de la protéineprotéine PB2, ne sont pas significativement différentes de la souche responsable des épizootiesépizooties concomitantes dans les élevages de volaille (Keawcharoen, Oraveerakul et al. 2004 27). En octobre 2004, une seconde flambée de pneumopathiespneumopathies sévères causa la mort de 45 tigres (sur 102 cas officiellement répertoriés (Quirk 2004 44)) dans un autre zoo de Thaïlande. L'analyse du génomegénome viral de deux isolats révèle une proximité génétique (99,9 à 100%) avec les virus isolés en Asie du sud-est, chez des mammifères (tigres, léopards et hommes) et les volailles infectées. On y retrouve la substitution par la lysinelysine de l'acide aminéacide aminé en position 627, présente dans le génome des virus isolés chez l'homme et absente du virus A (H5N1), responsable actuellement des épizooties (Amonsin, Payungporn et al. 2005 3) (Thanawongnuwech, Amonsin et al. 2005 56) (Thornley 2004 57).
L'enquête épidémiologique a conclu à une contamination par ingestioningestion de carcasses de poulet cru infectées par le virus A (H5N1).
De même, des cas mortels d'infection naturelle par le virus A (H5N1) ont été reportés à plusieurs reprises chez des chats domestiques, pendant les épizooties de grippe aviaire dans le sud-est asiatique, et plus récemment en février 2006 en Allemagne et mars 2006 en Autriche, enfin, chez la fouinefouine en mars 2006, en Allemagne, pays indemne d'épizootie aviaire.
L'infection expérimentale par inoculation intratrachéale d'une souche virale prélevée chez un patient décédé de grippe aviaire au Vietnam (A/Vietnam/1194/04) ou par ingestion de viande de poulet infectée par ce même virus, provoque une pneumopathie sévère voire mortelle, une excrétion du virus au niveau des voies respiratoires, la contamination des chats sentinelles qui présentent le même tableau clinique (Kuiken, Rimmelzwaan et al. 2004 31) (Enserink and Kaiser 2004 17).