au sommaire
L'ozone stratosphérique : source de vie
C'est très tôt après sa découverte vers la fin du dix-neuvième siècle, grâce à l'amélioration des outils d'observation, qu'on découvre l'aptitude de l'ozone à fortement absorber le rayonnement UVUV (Hartley, 1881). Sous l'impulsion de Fabry et Buisson (1913), puis de Dobson (1920), on établit clairement par une observation minutieuse du rayonnement UV solaire reçu au sol, la présence d'une couche d'ozonecouche d'ozone dans la stratosphèrestratosphère (10 - 50 km d'altitude), variable suivant les saisonssaisons et la latitudelatitude.

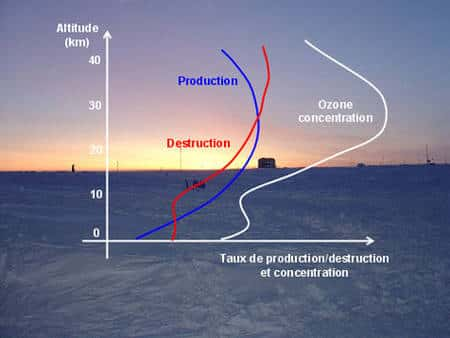
Figure 7 : Production, destruction et concentration de l’ozone en fonction de l’altitude selon le modèle de Chapman (© J. Savarino)
Il faut pourtant attendre 1934 et les mesures de Götz effectuant des mesures des UV lors du coucher et du lever du soleil pour découvrir que le pic d'ozone se situe vers 25 km d'altitude. Cette observation viendra confirmer expérimentalement les travaux de Chapman (1930) prédisant ce pic sur la seule base de calculs théoriques. Le modèle de Chapman, premier modèle de distribution de l'ozone en fonction de l'altitude, repose sur l'idée centrale que l'ozone est formée par l'association d'une molécule de O2 et d'un atome O, O2 + O = O3 et détruit par la réaction O + O3 = 2 O2. Or si la concentration d'O2 décroît avec l'altitude, tout comme la pression, la concentration de O, quant à elle, au contraire croît avec cette même altitude, O étant un produit de photolysephotolyse par le rayonnement UV dont l'intensité croît avec l'altitude. Le maximum d'ozone est donc atteint lorsque le taux de production d'O3 égale son taux de destruction, ce qui place le maximum d'ozone autour de 30 km dans la théorie de Chapman (Figure 7). Il faudra attendre 1970 et les travaux du Prix Nobel de chimiechimie Paul Crutzen pour arriver à un accord quantitatif entre le modèle de Chapman et les observations. Crutzen sera le premier à reconnaître l'importance de la chimie des oxydes d'azoteoxydes d'azote dans la destruction catalytique de l'ozone, avec pour conséquence une diminution de moitié du pic de concentration et un repositionnement de ce maximum autour de 22 km et non 30 km comme prédit par le modèle de Chapman.
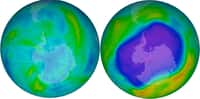
Par la suite l'effet des composés chlorés, les fameux CFCCFC et leur compagnon d'infortune le chlorechlore atomique (c'est ce chlore qui détruit l'ozone par la réaction Cl+O3 -> ClO + O2, et comme on le voit ce chlore atomique est oxydé par la molécule ozone !)) et la découverte du « trou d'ozone » complèteront notre compréhension du fonctionnement de la chimie stratosphérique (A lire sur notre site : "Le climat et la couche d'ozone" un dossier de Marie-Lise ChaninMarie-Lise Chanin)
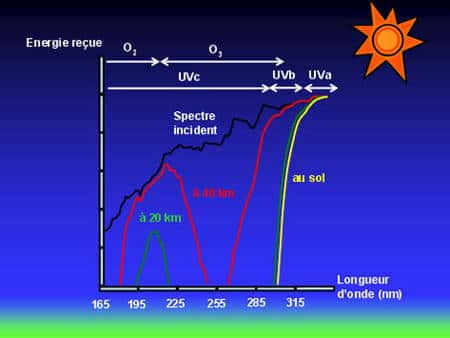
Figure 8 : Spectre solaire incident et absorption de celui-ci en fonction de l’altitude. Au niveau du sol, le rayonnement ultra violet a quasiment disparu. Seuls restent les UVa et un peu d’UVb pour le bronzage (© J. Savarino).
Ainsi formée, la couche d'ozone filtre le rayonnement UV dans la gamme 200-310 nm tandis que l'oxygèneoxygène moléculaire se charge d'éliminer dans la haute atmosphèreatmosphère le reste du spectrespectre UV (Figure 8). De fait, la présence d'O2 et d'O3 dans la haute atmosphère protège le sol du rayonnement destructeur des UV. Ici, l'ozone joue le rôle de bouclier. Son existence conditionne le développement de la vie sur les continents, c'est l'ozone source de vie.