Le cas d’un jeune garçon affecté d’une maladie jusque-là inconnue a conduit des médecins à identifier une nouvelle forme d’agammaglobulinémie, qui se traduit par l’absence totale de lymphocytes B producteurs d’anticorps. Une pathologie extrêmement rare, mais pour laquelle il existe heureusement un traitement.
au sommaire
Lorsque Luke Terrio avait environ sept mois, sa mère a commencé à se rendre compte que quelque chose clochait. Il avait des infections de l'oreille constantes, développait des taches rouges sur son visage et était fatigué tout le temps. Son développement stagnait et les antibiotiques administrés pour traiter ses infections fréquentes ont cessé de fonctionner. Son médecin l'a alors envoyé à l'hôpital pour enfants de Philadelphie, qui a pratiqué une série de tests sanguins. Le verdict est tombé : Luke n'avait pas d'anticorps.
Agammaglobulinémie : une mutation génétique qui empêche la maturation des lymphocytes B
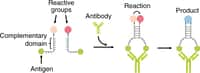
L'équipe a rapidement soupçonné que le garçon souffrait d'agammaglobulinémie liée à l'X, une immunodéficience rare due à la mutation d'un gène du chromosome X qui code pour la protéineprotéine BTK, essentielle au développement et à la maturation des lymphocyteslymphocytes B. Sans cette protéine, la maturation s'arrête et le patient ne produit aucun anticorps, ce qui aboutit à des infections à répétition par des bactériesbactéries, des virusvirus ou des champignonschampignons.
Mais le garçon présentait des symptômessymptômes inhabituels, différents de toutes maladies décrites précédemment. En séquençant son génomegénome, il s'est avéré que Luke ne souffrait pas de cette fameuse mutation. Ils ont alors comparé son génome avec celui de 30 autres patients atteints d'agammaglobulinémie qui n'avaient pas été diagnostiqués et se sont aperçus que six d'entre eux, dont Luke, possédaient une mutation du gène SPI1, situé sur le chromosome 11 et codant pour la protéine PU.1.
« Tout comme avec l'agammaglobulinémie liée à l'X, le développement des cellules B est stoppé très tôt dans la moelle osseusemoelle osseuse chez ces patients, en raison de la diminution de l'expression de la protéine PU.1, primordiale à la maturation des cellules B », explique dans un e-mail à Futura Carole Le Coz, qui a écrit une étude sur ces cas avec plusieurs collègues dans le Journal of Experimental Medicine. « La grande différence avec l'agammaglobulinémie liée à l'X, c'est que cette maladie touche aussi bien les hommes que les femmes (la première se transmettant sur le mode récessifrécessif, il n'atteint pratiquement que les garçons). De plus, pour quatre patients au moins, la mutation n'est pas héritée de l'un des parents, mais elle est apparue spontanément chez l'embryonembryon (on parle alors de mutation de novo) », poursuit la spécialiste.
Une naissance sur un million
La nouvelle maladie, nommée PU.MA par les médecins (PU.1 Mutated agammaglobulinemia), serait extrêmement rare, selon Carole Le Coz. « La prévalenceprévalence globale de l'agammaglobulinémie est d'environ un cas pour 250.000, la plupart ayant pour origine la mutation du gène BTK. Bien qu'il soit un peu tôt pour être fixé, la prévalence du syndromesyndrome PU.MA représenterait 20 % à 30 % des cas, soit une naissance sur million », estime le médecin.
Greffe de moelle osseuse
Les médecins ont d'abord pensé à administrer à Luke le traitement classique de l'agammaglobulinémie, qui consiste à injecter des immunoglobulines substitutives par voie veineuse. Mais c'est un traitement à vie et il peut déclencher des réactions allergiques graves. Les médecins ont alors découvert que Jack, le frère aîné de Luke, était un parfait candidat pour un don de moelle osseuse. Ils ont donc procédé à une greffegreffe, qui a très bien réussi et devrait permettre à Luke de fabriquer ses propres anticorps. En attendant que les lymphocytes B ne soient suffisamment matures, Luke continue de recevoir des anticorps et selon ses parents, « il n'arrête pas de courir après son chienchien ».