Des chercheurs de Singapour proposent une nouvelle approche pour détruire et combattre le cancer. Il s'agit de nanoparticules recouvertes d'acides aminés qui tuent les cellules cancéreuses de l'intérieur.
au sommaire
La communauté scientifique redouble d'inventivité pour trouver des nouveaux traitements contre le cancer. Dans les pays développés, les cancers sont la première cause de mortalité. Le Centre international de recherche sur le cancer estime que 9,6 millions de personnes sont décédées d'un cancer en 2018 au niveau mondial.
Des chercheurs de Singapour proposent une approche originale pour détruire les cellules cancéreuses. Leur idée se base sur l'utilisation de nanoparticulesnanoparticules qui, une fois entrées dans la cellule anormale, la détruisent, à l'image du célèbre épisode du Cheval de TroieCheval de Troie de la mythologie grecque.
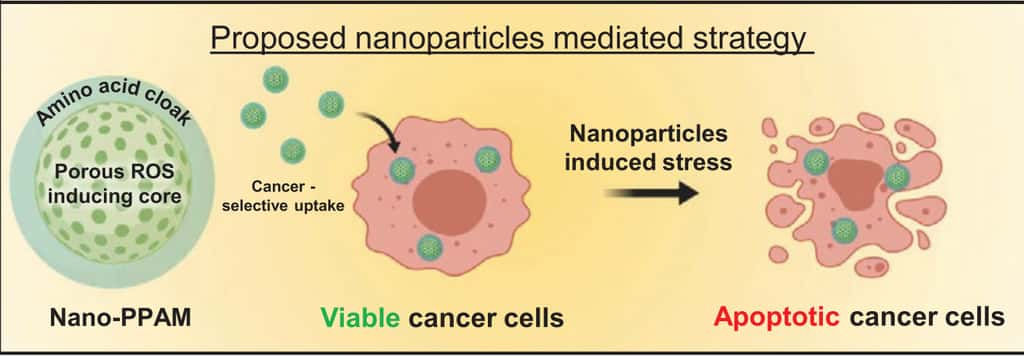
Faire entrer les nanoparticules dans les cellules cancéreuses
Les cellules cancéreuses sont des cellules qui prolifèrent de façon incontrôlée, elles ont perdu ce qu'on appelle l'inhibition de contact. Cela apparaît lorsque la cellule accumule des mutations géniquesgéniques qui dérèglent son métabolisme. Pour assurer leur multiplication rapide, elles ont besoin d'un rapport plus important en acides aminés essentiels. De nombreuses cellules cancéreuses sur-expriment le transporteur LAT-1 dont le rôle est de transporter les acides aminés du milieu extra-cellulaire vers le cytoplasme.
Face à ce constant, les chercheurs singapouriens ont imaginé une nanoparticule, appelée Nano-pPAAM, poreuse de silicesilice d'environ 30 nm de diamètre sur laquelle ils ont fixé des L-phénylalaninesphénylalanines, un acide aminé essentiel. La nanoparticule voyage par le transporteur LAT-1 pour satisfaire les besoins en acides aminés de la cellule mais, une fois à l'intérieur, elle va la pousser au suicide. En effet, à l'intérieur du cytoplasme, les nanoparticules sont considérées comme des intruses que la cellule veut à tout prix éliminer.
Dans leur publication, les scientifiques ont montré que leur présence active les voies du stress oxydatif, un mécanisme de défense cellulaire. Mais une trop forte concentration de ROS (reactive oxygen species)) dans la cellule conduit à sa mort par apoptoseapoptose. Voici en théorie comment les nanoparticules fonctionnent. Les scientifiques ont ensuite effectué des expériences in vitroin vitro et in vivoin vivo pour attester de l'efficacité des Nano-pPAAM sur la taille des tumeurstumeurs.
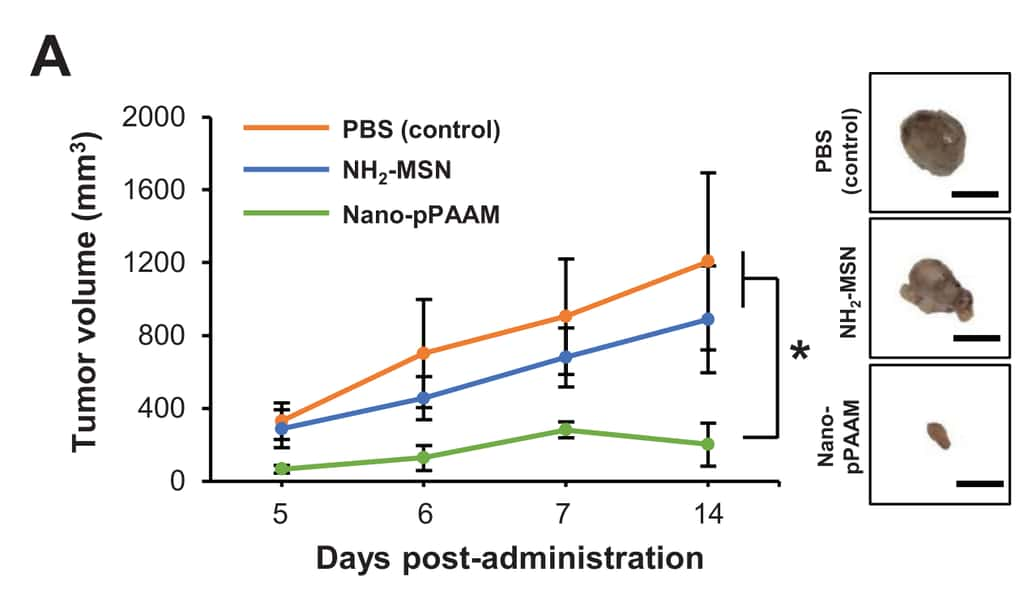
Les nanoparticules réduisent le volume des tumeurs chez la souris
La première série d'expérience a été faite in vitro. Des cellules de cancer du seincancer du sein ont été mises en cultures sur un gelgel d'agaroseagarose. Après 24 h de croissance, les cellules cancéreuses forment des sphéroïdes. Les scientifiques ont étudié la viabilité cellulaire dans les sphéroïdes lorsque les cellules ont été traitées par le Nano-pPAAM. Les nanoparticules ont moins bien fonctionné sur les sphéroïdes : environ une perte de 40 % de viabilité cellulaire lorsque les cellules sont sous cette forme, contre près de 80 % de mortalité lorsque les cellules étaient en tapis.
L'étape suivante consiste à étudier l'effet d'une injection de nanoparticules sur des souris NOD ayant reçu une xénogreffexénogreffe d'un cancer du sein. Les scientifiques ont évalué le volumevolume des tumeurs à 5, 6, 7 et 14 jours après l'injection des nanoparticules. Ces dernières ont permis de limiter le volume de la massemasse cancéreuse à moins de 300 mm3 contre plus de 1.200 mm3 pour les souris du groupe contrôle.
Les nanoparticules devront encore faire l'objet de nombreuses recherches avant de devenir un traitement viable pour le cancer, mais un des avantages de celui-ci est l'absence, pour le moment supposée, d'effet secondaire. Les souris ayant reçu l'injection de Nano-pPAAM n'ont pas souffert de poids ou de changement de comportement. Les scientifiques de Nanyang Technological University de Singapour souhaitent améliorer la spécificité de ces nanoparticules.
Des nanoparticules contre les tumeurs
Article publié le 9 avril 2008 par Laurent SaccoLaurent Sacco
La chimiothérapiechimiothérapie peut être une arme efficace dans la lutte contre le cancer. Malheureusement, les doses nécessaires de produits actifs ont souvent des effets secondaires indésirables. Cela pourrait changer grâce à l'emploi de nanoparticules recouvertes des substances activessubstances actives. Une étude récente montre qu'une dose mille fois moins forte de produits suffit à traiter certaines tumeurs.
Patrick M. Winter, Gregory M. Lanza et Samuel A. Wickline sont médecins et chercheurs. Ce sont des pionniers des nanotechnologiesnanotechnologies en médecine et ils sont membres de la Washington University School of Medicine à Saint-Louis. Dans un article du Faseb Journal, ils ont exposé les résultats de leurs recherches sur le traitement des tumeurs chez des lapins à l'aide de nanoparticules recouvertes de fumagilline, une toxinetoxine utilisée en chimiothérapie, que l'on trouve chez certains champignonschampignons. Cette idée n'est pas nouvelle. Plusieurs équipes dans le monde cherchent à utiliser les nanoparticules pour transporter vers une tumeur des principes actifs de la chimiothérapie.
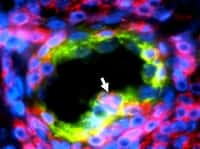
Les nanoparticules de l'expérience sont constituées essentiellement de perfluorocarbone, un composé bien connu, à la base du sang artificiel et bien toléré biologiquement. D'une taille de 200 nanomètresnanomètres de diamètre environ, elles sont 500 fois plus fines qu'un cheveu humain et les chercheurs leur ont ajouté des composants augmentant leur visibilité par contrastecontraste en imagerie par résonance magnétiqueimagerie par résonance magnétique nucléaire (IRMN). Comme on peut le voir sur la figure, en colorant ces nanoparticules sur une image de tumeurs obtenue par IRM, elles sont bien visibles.
Les chercheurs ont étudié leur effet sur la croissance des vaisseaux sanguins alimentant les tumeurs chez les lapins selon qu'elles sont administrées avec ou sans fumagilline. A forte dose, cette toxine est utile en chimiothérapie mais, hélas, elle devient un neurotoxique dont l'emploi ne peut pas être prolongé. A la surface des nanoparticules, elle aide celles-ci à se fixer préférentiellement sur les protéinesprotéines des cellules de vaisseaux sanguins alimentant les cellules cancéreuses et elle bloque la formation de ces vaisseaux. Les expériences prouvent qu'avec des doses mille fois moins importantes, passant au-dessous du seuil de toxicitétoxicité, la prolifération des vaisseaux sanguins et donc la croissance des tumeurs est fortement ralentie.
De façon plus générale, les nanoparticules, en se fixant sélectivement dans les zones où prolifèrent les cellules cancéreuses, peuvent permettre de surveiller la croissance des tumeurs de façon fine avec des techniques d'IRMN. Selon Patrick M. Winter, cela devrait ouvrir des perspectives intéressantes pour comprendre l'impact d'un traitement par chimiothérapie sur la croissance des tumeurs en suivant ses effets au jour le jour. Enfin, les chercheurs devraient passer aux applicationsapplications chez l'homme au cours de cette année.