au sommaire
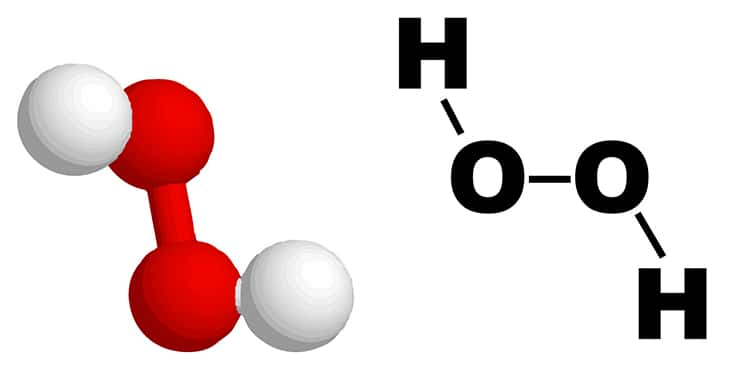
Le peroxyde d'hydrogènehydrogène est un composé chimique de formule H2O2 dont la solution aqueusesolution aqueuse est l'eau oxygénée. Incolore, celle-ci a tendance à être instable, car de nombreuses substances agissent comme catalyseurcatalyseur pour sa dismutationdismutation en eau et oxygène selon la réaction exothermiqueexothermique 2 H2O2 → 2 H2O + O2. Les plus actives sont les métauxmétaux lourds et leurs sels (cuivrecuivre, cobaltcobalt, manganèsemanganèse, chrome, nickelnickel, molybdènemolybdène, plombplomb, ferfer...)), mais de simples impuretés, une exposition à la chaleurchaleur ou à la lumièrelumière accélère aussi la réaction. Pour améliorer sa durée de conservation, les solutions d'eau oxygénée vendues dans le commerce sont stabilisées avec des agents permettant de complexer ou d'adsorber les impuretés.
Le peroxyde d'hydrogène est produit naturellement comme sous-produit de la respiration cellulairerespiration cellulaire via des enzymesenzymes appelées peroxydases qui catalysent la dismutation. Industriellement, il est habituellement fabriqué par oxydationoxydation d'anthrahydroquinone en anthraquinone.
Risques de combustion et d’explosion
En milieu acideacide, le peroxyde d'hydrogène est l'un des plus puissants oxydants connus, avec une réaction parfois violente en présence de certains produits organiques (acétoneacétone, acétaldéhydeacétaldéhyde, acide formique, alcoolsalcools). À de fortes concentrations, l'eau oxygénée peut provoquer une explosion avec des matièresmatières organiques (huiles, graisses, kérosènekérosène...) et l'inflammationinflammation spontanée de matériaux tels que le boisbois, la paille ou le coton. De plus, des vapeurs explosives peuvent se former en cas d'ébullition.
Risques toxicologiques
Chez l'humain, l'eau oxygénée est faiblement toxique grâce aux peroxydases qui la décomposent naturellement. Elle peut quand même induire des effets irritants ou caustiques sur la peau et les yeuxyeux. Elle peut aussi engendrer des eczémas et des réactions phototoxiques. Le peroxyde d'hydrogène est en revanche génotoxiquegénotoxique pour certaines bactériesbactéries (notamment E. coliE. coli) et de nombreux microorganismesmicroorganismes (d'où son action désinfectante).
Utilisations de l’eau oxygénée
Du fait de ses propriétés oxydantes et décolorantes, l'eau oxygénée trouve de nombreuses utilisations à des concentrations différentes :
- blanchiment de la pâte à papier (cet usage représente plus de 50 % de la production),
- désinfectant local et arrêt des saignements,
- blanchiment des dents,
- blanchiment et détachant ménager (linge, carrelage, plans de travail...),
- décoloration des poils et des cheveux,
- traitements dermatologiques,
- fabrication d'explosifs,
- stérilisation des cultures,
- purification d’eau de piscine,
- comburantcomburant pour la propulsion d'avions et de fuséesfusées.
















