L’hydrogène pourrait remplacer avantageusement les carburants fossiles dans les véhicules de demain. Encore faudrait-il parvenir à le produire à un coût économique et environnemental raisonnable. Des chercheurs avancent aujourd’hui une nouvelle idée pour y parvenir : extraire de l’hydrogène des champs pétrolifères.
au sommaire
Ils sont de plus en plus nombreux à voir en l'hydrogène (H2)), la solution à nos problèmes énergétiques. Sa combustion ne génère en effet pas de CO2 et produit une grande quantité d'énergie. C'est pourquoi des véhicules fonctionnant à l’hydrogène sont en développement depuis plusieurs années. Des voituresvoitures, des bus, des trains, des bateaux et même des avions. Problème : produire de l'hydrogène propre coûte cher !
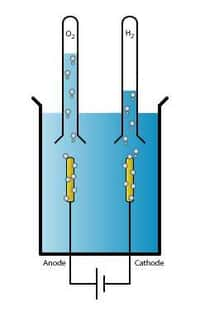
Pour l'heure, l'hydrogène est essentiellement produit à partir de gaz naturelgaz naturel, de pétrole et de charboncharbon. Par une méthode rentable, mais à l'origine de l'émission de pas moins de 830 millions de tonnes de CO2 par an. C'est l'équivalent des émissions cumulées du Royaume-Uni et de l'Indonésie. Alors, les ingénieurs imaginent produire de l'hydrogène par électrolyseélectrolyse de l'eau. Une solution propre si l'électricité qu'elle utilise est d'origine renouvelable. Mais une solution qui reste aujourd'hui peu rentable.
La solution présentée aujourd'hui par des chercheurs de l'université de Calgary (Canada) est encore différente. Et elle présente, selon eux, tous les avantages. Une méthode économique qui permet d'extraire de l'hydrogène des sables bitumineux et des champs de pétrole tout en maintenant le carbonecarbone piégé dans le sol.

La thermolyse au cœur du procédé
Comment ? En y injectant de l'oxygèneoxygène. Car l'hydrogène n'est pas préexistant dans ces réservoirs. Mais apporter de l'oxygène élève la température au-delà de 500 °C. Une chaleurchaleur qui initie la fragmentation des hydrocarbureshydrocarbures -- et des moléculesmolécules d'eau aussi, d'ailleurs -- présents dans le sol. C'est donc par thermolysethermolyse que l'hydrogène est libéré. Ne reste plus alors aux ingénieurs qu'à le récupérer et à le séparer des autres gaz grâce à des filtres sélectifs mis au point par les ingénieurs.
“Entre 15 et 50 cents le kilogramme de H2”
La société qui entend commercialiser le procédé évalue les coûts de production entre 10 et 50 cents le kilogrammekilogramme de H2, alors qu'aujourd'hui, il en coûte quelque 2 dollars. Elle estime que les champs disponibles en Alberta (Canada) suffiraient à satisfaire les besoins en électricité de l'ensemble du Canada -- soit quelque 2,5 % de la consommation mondiale -- pendant 330 ans.
Si les ingénieurs qui ont développé le procédé se montrent naturellement très enthousiastes, d'autres restent plus prudents, considérant que les niveaux de prix annoncés ne peuvent être atteints qu'avec des moyens techniques encore compliqués à mettre en œuvre. Et ils s'interrogent quant à la pureté de l'hydrogène ainsi produit.
Ce qu’il faut
retenir
- Aujourd’hui, l’écrasante majorité de l’hydrogène est produite à partir d’un procédé qui émet du CO2.
- Demain, il pourrait bien être produit, sans émission de CO2, à partir des champs de pétrole et à un coût économiquement rentable.
- Une solution qui laisse d'autres scientifiques dubitatifs, lesquels prévoyant des difficultés de mise en œuvre du procédé.