au sommaire

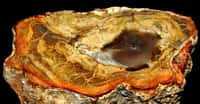
Fluorite jaune-doré. © Spathfluorminerals.com
Le nom de la fluorine vient du latin fluere signifiant fondre, couler. Certains minérauxminéraux fluorés ont des propriétés de fondant : ils abaissent le point de fusionfusion de divers minerais et les rendent plus fluides. Le caractère phosphorescent de la fluorine a été découvert par le minéralogiste Mohs au XIXe.
La fluorine (de symbole CaF2)) est utilisée depuis le Moyen Âge comme agent pour liquéfier les scories lors de la production des métauxmétaux. Au XIXe, la cryolite (Na3AlF6) était utilisée dans la préparation électrolytique de l'aluminiumaluminium, permettant ainsi une formidable expansion de la sidérurgie de ce métal.
La fluorite désigne la roche contenant la fluorine, le principal minerai du fluorfluor.
Le nom fluorescence en dérive également. L'émissionémission de lumièrelumière par la fluorite chauffée a été découverte au XVIIe.
Ce minéral, qui existe à l'état naturel en de nombreux endroits, a reçu plusieurs noms : Spatum vitreum ou Calx fluorata entre autres, avant de porter le nom de fluorite. Le terme commercial et industriel est spath fluor.
Couleurs de la fluorite
La teneur de l'écorce terrestre est inférieure à 0,1 % en fluor. Les couleurscouleurs sont dues à la présence d'éléments divers dans le cristal par exemple des ionsions (yttriumyttrium, europiumeuropium...). Les plus répandues sont :

Fluorite verte (la Barre) et fluorite mauve, violette à violet foncé (Berbès). © Spathfluorminerals.com

Fluorite transparente et bleue (Le Beix, Le Burg). © Spathfluorminerals.com

Fluorite jaune-doré. © Spathfluorminerals.com
Après concentration du minerai, pour l'industrie, on distingue deux types de produits :
- le spath fluor « acideacide » ou « chimique », contenant plus de 97 % de CaF2. Destiné à la chimiechimie il se présente sous forme de poudre ;
- le spath fluor « métallurgique » contenant moins de 97 % de calciumcalcium fluoride (CaF2), en grains.
Dans certains cas, le spath fluor est concurrencé par l'acide fluosilicique, sous-produit de l'industrie des engrais phosphatés.
Production mondiale
La fluorite est utilisée pour réaliser des lentilles transparentes aux ultravioletsultraviolets. Utilisée comme fondant en métallurgie, elle sert à la préparation du fluor.
Production mondiale en 1996, 4.200.000 tonnes (chiffres de la Société française de chimie)
- Chine : 2.000
- Mexique : 525
- CEICEI : 300
- Mongolie : 210
- Afrique du Sud : 200
- France : 130
En 1994, fermeture de Buffalo Fluorpar Mine (Afrique du Sud), la plus grande mine au monde, qui produisait 180.000 t/an.
Principaux pays exportateurs : Chine, Mexique et Afrique du Sud. Principaux pays importateurs : États-Unis (573.000 t, en 1995) et Japon.
Les minerais ont, en France, une teneur de l'ordre de 50 % en CaF2. L'arrêt définitif de la production française a été fait en avril 2006 (mines du Tarn). On consomme environ 100.000 t de spath acide et environ 20.000 t de spath métallurgique.
Quelques mines françaises exploitées pour la fluorite
- Chaillac, Indre, exploité par la SIC jusqu'en 2003.
- Le Kaymar, Aveyron, exploité depuis l'Antiquité pour l'argentargent et le plomb et depuis le XXe pour la fluorite.
- Langeac, Haute Loire, une des plus grosses productions, arrêtée en 1977.
- Le Burg, Tarn, filonfilon très pur exploité par une filiale de Péchiney.
- La Pierre Perthuis, Yonne, le plus important en tonnage et en étendue...
En tout une vingtaine de lieux d'exploitation et presque autant de mines intéressantes sur le plan minéralogique avec de très beaux spécimens dans certains endroits.

Ponts de Pierre Perthuis, Yonne (lieu d'ancienne mine de fluorite). Le plus petit (plus ancien) date de 1770, les deux enjambent La Cure. © DR
Industrie du spath fluor
Spath fluor acide et spath fluor métallurgique se partagent moitié - moitié, en tonnage, la consommation mondiale de 3 millions de t/an. La fluorite est la source de l'élément fluor pour l'industrie chimique. Elle permet de fabriquer le fluorure d'hydrogènehydrogène (HF) :
CaF2 + H2SO4------> CaSO4 + 2 HF (300 °C, four rotatif)
H2SO4 concentré fumant
La présence de silicesilice dans la fluorite est limitée au maximum car elle consomme l'acide fluorhydrique formé sous forme de SiFSiF4 et H2SiF6. Le fluorure d'hydrogène (HF) gazeux est purifié pour donner une pureté de 99,9 %. Il faut plus de 2 tonnes de CaF2 pour obtenir une tonne d'acide fluorhydrique. CaSO4, sous-produit, peut être valorisé dans la fabrication du plâtreplâtre.
Utilisations de la fluorite
- L'élaboration d'aluminium fluoride AlF3 (par attaque de l'aluminealumine Al2O3) et de la cryolite (Na3AlF6) pour le bain d'électrolyseélectrolyse qui permet de produire l'aluminium :
- cryolithe : 83 %
- AlF3 : 7 %
- CaF2 : 5 %
- Al2O3 : 5 %
Il faut entre 20 et 60 kgkg de spath fluor par tonne d'aluminium, soit 1/3 de la consommation mondiale de spath fluor (Données SFC). L'aluminium est l'industrie où les émissions atmosphériques de fluorure sont les plus importantes, avec 75 % des émissions. Comme la température est élevée à l'intérieur d'une cuve, lors de la production d'aluminium, une partie des fluorures est émise sous forme de gazgaz par évaporation des composés fluorés et pollue la région environnante si des filtres très performants ne sont pas mis en place.
- La fabrication de dérivés fluorés : chlorofluorocarbures, hydrofluorocarbures, polymèrespolymères fluorés, fluorures simples avec par exemple le NaF du sel de table fluoré...
- Par ailleurs, HF est la source du fluor, obtenu par électrolyse, utilisé pour oxyder UF4 en UF6, pour l'enrichissement de l'uraniumuranium par diffusiondiffusion gazeuse...
- La fluorite est également utilisée directement comme fondant dans l'électrolyse de l'aluminium et la sidérurgie : fluidité du laitier avec une consommation de 20 kg/t d'acieracier produit et comme fondant de la chauxchaux.
- La fluorite est également utilisée dans l'industrie céramiquecéramique comme opacifiant des émaux. Le spath fluor doit être utilisé avec précision car un mauvais dosagedosage peut provoquer le bouillonnement de l'émailémail. Elle est aussi utilisée dans l'industrie du verre : verre opaleopale, fibres de verre, verresverres spéciaux.

Aluminium Péchiney St-Jean-de-Maurienne. © DR
Lire notre dossier Le fer tombe le masque
Bibliographie
- C.König : notes personnelles
- Pascal, P., Nouveau traité de chimie minérale, Masson 1964
- Informations Chimie, n° 270, mars 1986.
- Techniques de l'Ingénieur, Acide fluorhydique, 1995.
- E. Guillou-Gotkovsky, La Mine de Fluorite de Valzergues (Aveyron)
- Fluorite et autres halogénures, Minéraux et FossilesFossiles HS N°13 - 2001
Sur Internet
Remerciements
Spathfluorminerals.com
Etienne Guillou - MultiAxes
46, petite rue Verte
78 610 Le Perray en Yvelines
France