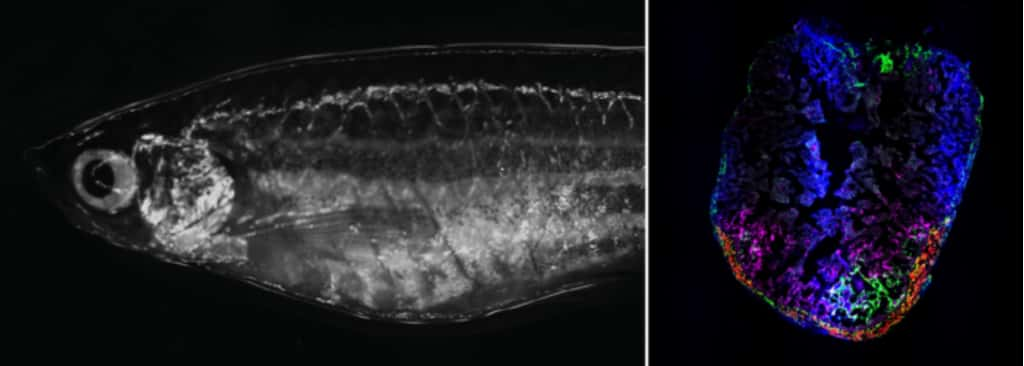
Et si notre cœur pouvait se réparer de lui-même après une crise cardiaque ? Chez les mammifères, une telle prouesse n'est pas possible. Mais des chercheurs ont observé un petit poisson capable de se régénérer après une blessure cardiaque : le poisson-zèbre.
au sommaire
Lors d'un infarctus du myocardeinfarctus du myocarde, le manque d'apport en oxygène causé par l'obstruction d'une artèreartère coronaire conduit à un endommagement des cellules cardiaques, voire à une nécrose. Dans ce cas, un tissu cicatriciel se forme, la blessure reste indéfiniment. Le cœur ne pourra plus pomper aussi bien qu'avant. Revenir à son état optimal nécessiterait une véritable régénération du tissu cardiaque, impossible pour l'humain, et tous les mammifères en général.
Or, des chercheurs rapportent dans une étude publiée dans la revue Nature Genetics que le poisson-zèbre, connu pour être capable de régénérer ses membres perdus, ou même ses rétinesrétines, peut aussi régénérer ses cellules cardiaques ! L'équipe a donc voulu analyser les mécanismes en jeu dans ce processus de régénération cardiaque. À cette fin, ils ont simulé des lésions d'infarctus du myocarde dans le cœur de poissons-zèbres, et ont ensuite observé la régénération des cardiomyocytescardiomyocytes (cellules cardiaques).
Trois nouveaux types de fibroblastes activés
Le processus de réparation commence comme chez les mammifères : une réponse inflammatoire suivie d'une cicatrisationcicatrisation des cellules du tissu conjonctif appelées fibroblastesfibroblastes. Mais, là où chez l'humain, la réponse s'arrête, chez les poissons-zèbres, ce n'est que le début. « Ils forment de nouveaux cardiomyocytes, capables de se contracter, explique Jan Philipp Junker, coauteur de l'étude et chercheur en biologiechercheur en biologie. Nous voulions identifier les signaux provenant d'autres cellules et aider à conduire la régénération ».
Chez le poisson-zèbre, trois nouveaux types de fibroblastes s'activent temporairement, capables de lire et d'exprimer plus de gènesgènes que les autres cellules, donc de produire d'autres protéinesprotéines. Lorsque l'équipe a désactivé ces cellules, plus de régénération. Ces fibroblastes proviennent, d'après l'équipe, de l'épicarde et de l'endocarde, les deux couches qui entourent le myocarde. Ils concluent leur étude sur la possibilité « d'ouvrir des approches possibles pour moduler la capacité de régénération du cœur des vertébrés », bien que leur « connaissance de la composition cellulaire de la niche régénérative et des interactions de signalisation sous-jacentes reste incomplète ».