au sommaire

Les premières images d'un supercomplexe de protéines
Les protéinesprotéines, chevilleschevilles ouvrières de l'organisme, fonctionnent généralement en coopérant entre elles. Elles s'associent sous forme de complexes protéiques et s'entraident pour remplir leurs fonctions. Si les chercheurs s'étaient jusqu'à ce jour surtout intéressés aux protéines « célibataires », les mariages protéiques restaient quant à eux un mystère. Le voile vient de se lever sur cet aspect de la biologie grâce à des biophysiciensbiophysiciens de l'Institut Curie.

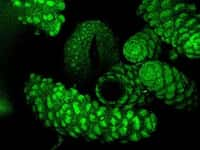
(légende de l'image : pointe d'AFMAFM se déplaçant sur un échantillon - les dégradés de couleurs indique la hauteur de l'échantillon - plus la couleur tend vers le jaune, plus l'échantillon est épais)
L'organisme est constitué d'une multitude d'organitesorganites aux fonctions variées. Pour qu'ils trouvent leur place, ils doivent être bien différenciés et surtout isolés. C'est le rôle des membranes. Composées d'une double couche de lipideslipides, elles entourent les cellules et délimitent ainsi leur volume. Mais les membranes ne sont pas de simples clôtures, elles servent aussi de garde-frontière. Et pour cela elles sont aidées par les protéines membranaires. Ce sont en effet ces dernières qui filtrent le passage entre les deux milieux. A ce titre, elles jouent un rôle clé dans la signalisation cellulaire. Une fonction essentielle à la vie cellulaire qui, si elle est altérée, peut avoir de très fâcheuses conséquences pour la cellule, voire pour l'ensemble de l'organisme. C'est en effet l'accumulation de défauts dans plusieurs gènesgènes impliqués dans la transmission des signaux et la surveillance de la machinerie enzymatiqueenzymatique qui déclenche le processus de cancérogenèse.
Le cancer, une maladie de la transmission des signaux
Les cellules ne sont pas des entités isolées : elles communiquent sans cesse avec leur environnement grâce à des récepteurs membranaires où se fixent des messages informatifs venus de l'extérieur (autres cellules, tissus et organes). La réceptionréception de ces messages active des protéines à l'intérieur de la cellule qui à leur tour en activent d'autres, et ainsi de suite. Une fois interprétés, ces signaux vont permettre aux cellules de déterminer leur position et leur rôle dans l'organisme. Ils sont indispensables à la prolifération, à la différenciation, à la morphologiemorphologie et à la mobilité des cellules. Au niveau des organes, ces signaux assurent le maintien harmonieux de la taille et de la fonction des tissus. La moindre défaillance dans ce système peut conduire à la catastrophe : les cellules cancéreuses, même si elles n'assurent plus leur fonction, continuent à proliférer dans l'organisme. Elles font « la sourde oreille » aux ordres venus de l'extérieur, ce qui fait du cancercancer, entre autres, une maladie de la transmission des signaux. Les premiers traitements "anti-signalisation" (Herceptin®, Iressa® et GlivecGlivec®)) commencent déjà à voir le jour.
Des protéines qui n'aiment pas la solitude
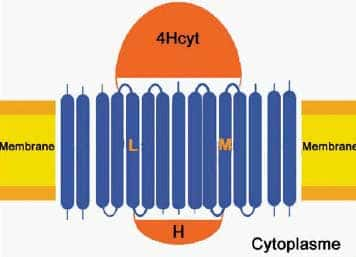
Extrêmement nombreuses puisque environ 25 % des génomesgénomes séquencés codent pour de telles protéines, les protéines membranaires ne fonctionnent généralement pas de manière isolée mais en s'associant entre elles pour former des supercomplexes protéiques. L'un des plus connus à ce jour est celui assurant la transformation de l'énergie lumineuse en ATPATP chez des bactériesbactéries photosynthétiques, comme Rhodopseudomonas viridis. Si les connaissances atomiques des différents constituants de ces membranes sont relativement avancées, très peu d'informations sont en revanche disponibles sur l'organisation et la fonction de ces supercomplexes. Leur étude représentait jusqu'à maintenant un défi pour les biologistes, car avec les méthodes disponibles, ils ne pouvaient principalement observer que des protéines isolées de leur contexte.

L'équipe de Jean-Louis Rigaud « Cristallisation bidimensionnelle de protéines membranaires » à l'Institut Curie vient de bouleverser cet état de fait en rendant possible l'observation à haute résolutionrésolution de membranes biologiques en conditions physiologiques par la microscopie à force atomique (AFM).