au sommaire

Le prototype de la Micropac (micropile à combustible). © Artechnique/CEA
A Grenoble, le Liten (Laboratoire d'innovations pour les technologies des énergiesénergies), qui dépend du CEA (Commissariat à l'énergie atomique), travaille depuis plusieurs années sur un projet de pile à combustiblepile à combustible miniature, en collaboration avec la société STMicroelectronics. Baptisée Micropile, ou Micropac, elle est construite comme un circuit électronique, sur des galettes de siliciumsilicium. Sa miniaturisation la destine particulièrement aux petits appareils nomades, à commencer par les téléphones. Le CEA vient de faire le point sur cette innovation, annonçant des résultats prometteurs et une faisabilité industrielle d'ici quatre ans.
Comme toute pile à combustible, le modèle du Liten produit de l'électricité grâce à la réaction chimiqueréaction chimique entre l'oxygène de l'airair et de l'hydrogènehydrogène préalablement stocké, qui s'associent pour former de l'eau. L'un des problèmes à résoudre est la production ou le stockage de cet hydrogène, le gazgaz le plus léger de tous.
Plusieurs filières ont été explorées. L'une, qui fonctionne à température ambiante, consiste à utiliser de l'hydrogène chimiquement lié à une grosse moléculemolécule. La plus commode est le méthanol (ou alcoolalcool méthylique), que l'on peut utiliser sous forme liquideliquide dans des réservoirs ou des cartouches jetables. Cette technique, dite DMFC (Direct Methanol FuelFuel Cell), semble bien convenir aux appareils de petites tailles et aux petites puissances mais est aussi envisagée pour des applicationsapplications plus lourdes, notamment pour l'automobileautomobile électrique.
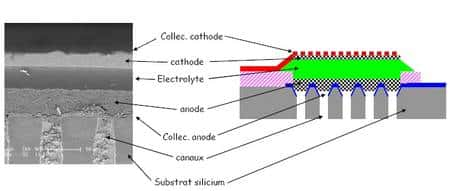
Photographie au microscope électronique et schéma d'un élément de la pile. La cathode, protégée par un revêtement percé laissant passer l'oxygène de l'air (le collecteur, Collec. Cathode sur le schéma), surmonte la membrane en polymère servant d'électrolyte. Dessous se trouve l'anode en communication grâce à des canaux avec l'arrivée d'hydrogène gazeux. Le tout est gravé avec les procédés de la microélectronique sur un substrat de silicium. © Artechnique/CEA
Une autre voie prometteuse, utilisant de l'hydrogène pur et fonctionnant elle aussi à température ambiante, est celle des piles à membrane échangeuse de protonsprotons, ou PEFMC, acronyme, au choix, de Proton Exchange Membrane Fuel Cell ou de Polymer ElectrolyteElectrolyte Membrane Fuel Cell. Dans ce cas, l'électrolyte, c'est-à-dire le composant interne entre l'anodeanode et la cathodecathode, où circulent les ionsions H+ (protons), est solidesolide. Il est composé d'un polymèrepolymère et prend la forme d'une membrane.

Ces galettes (ou waffers) porte les futurs éléments électrochimiques de la Micropac. Elles sont similaires à celles servant à la fabrication des puces électroniques. © Artechnique/CEA
De l'hydrogène dans une cartouche
La technique PEFMC apporte des gains intéressants, outre la présence de cet électrolyte solide, notamment un poids faible, une bonne robustesse, une large gamme de puissance, etc. C'est la solution retenue au Liten. La production d'hydrogène pour son alimentation reste toutefois une limite et beaucoup d'industriels, aux Etats-Unis et au Japon surtout, ont préféré poursuivre la filière DFMC. Mais, remarque-t-on au CEA, depuis 2005, cette technique montre ses limites (en puissance fournie et en miniaturisation) et la filière PEFMC revient un peu plus à la mode.
Pour le stockage de l'hydrogène, le Liten a opté pour un composé chimique, le borohydrure de sodiumsodium (NaBH). Cette solution a déjà été adoptée par l'entreprise américaine Millenium Cell, qui fournit des piles à combustibles PEFMC pour de multiples applications. Sous forme d'une poudre blanche, cet hydrure est stocké dans un petit réservoir de la taille d'un briquet, qui contient aussi de l'eau. En envoyant un peu de ce liquide sur la poudre, on déclenche une réaction chimique (une hydrolysehydrolyse plus précisément) avec dégagement d'hydrogène gazeux. Ce dispositif fourni une puissance massique de 500 wattswatts.heures par litre (Wh/l). Un litre de ce combustible fournirait donc 500 watts pendant une heure (ou un watt pendant 500 heures), soit cinq fois plus qu'une batterie classique.

Gros comme un briquet, le réservoir contient de l'eau et du borohydrure de sodium, qui libère son hydrogène par hydrolyse. La puissance actuelle est de 500 Wh/litre. © Artechnique/CEA
L'intérêt de ce procédé est qu'il fournit de l'hydrogène à la demande, c'est-à-dire fabriqué au moment où il doit être utilisé. Il n'y a donc pas de stockage d'hydrogène gazeux. Cette cartouche alimente la Micropac, constituée d'une série d'éléments électrochimiques réduits à des circuits de quelques micronsmicrons gravés sur un substratsubstrat de silicium avec les techniques habituelles de l'électronique, en l'occurrence la sérigraphiesérigraphie, le jet d’encre (qui peut aussi servir à imprimer des circuits) et la lithographielithographie). Chaque élément est composé d'une anode et d'une cathode séparées par la membrane faisant office d'électrolyte, l'une et l'autre étant en contact avec, respectivement, l'hydrogène et l'oxygène (c'est-à-dire l'air ambiant).
Cette Micropac fournit aujourd'hui 150 milliwatts par centimètre carré (mW/cm2) de manière stabilisée, avec un maximum temporaire de 400 mW/cm2. L'objectif de l'équipe est de parvenir à 1 W/cm2 dans quatre ans. Cette performance sera alors suffisante pour permettre l'alimentation d'un téléphone portable, avec un gain d'autonomie en prime et une recharge instantanée par le changement d'une cartouche.