au sommaire
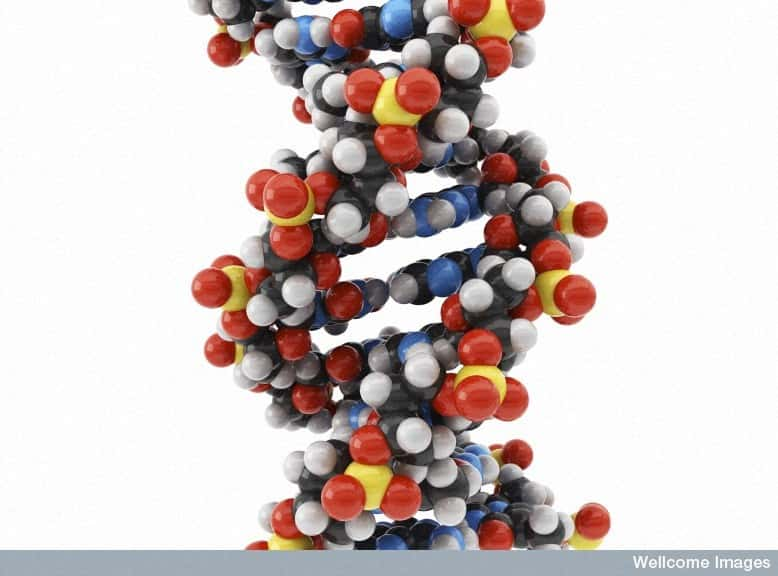
Le séquençage complet de l'ADN humain, en avril 2003, a lancé la voie vers de nouvelles méthodes de soin. Grâce à la médecine génomique personnalisée, encore balbutiante, des chercheurs espèrent prévenir l'apparition de certaines maladies et mieux comprendre les mécanismes moléculaires entrant en jeu pour apporter des réponses thérapeutiques plus ciblées. © Wellcome Images, Flickr, cc by nc nd 2.0
C'est une expérience peu banale que relate la revue Cell. Même une première dans le genre. Si l'on cherche à établir les profils génétiquesprofils génétiques et métaboliques de personnes atteintes par diverses pathologies, on n'avait jamais tenté de collecter les mêmes données chez un individu sain. Michael Snyder, généticiengénéticien de 56 ans à l'université de Stanford (Californie) s'est prêté à l'expérimentation. Et ne le regrette pas...
Tout d'abord, pourquoi lui ? À la tête d'une équipe de chercheurs, il souhaitait disposer d'une personne habitant dans la région, en mesure de fournir des échantillons sanguins régulièrement. De plus, il fallait qu'il soit sûr également que le cobaye ne se retourne pas contre les scientifiques en cas de révélation gênante. Étant le directeur de cette étude, le seul qui n'allait pas pouvoir lui faire de reproches, c'était lui-même.
Il s'est donc lancé dans un suivi de quatorze mois, se soumettant à vingt prises de sang, grâce auxquelles ont pu être observés son génome (l'ensemble des gènes), son protéome (l'ensemble des protéines), son métabolome (l'ensemble des métabolitesmétabolites), en plus de son ARNARN et de protéines du système immunitairesystème immunitaire. En tout, 3,2 milliards de nucléotidesnucléotides et 3 milliards de composants sanguins sont passés au microscopemicroscope.
La transition de l’état sain à l’état diabétique
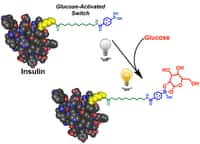
Lors du premier prélèvement, il était atteint d'un rhume. L'occasion de regarder comment un rhinovirus modifie la réponse du corps humain. Le séquençageséquençage de son ADN révèle chez lui des prédispositionsprédispositions au diabètediabète. Face à l'absence d'antécédents familiaux et sa silhouette ne laissant présager d'aucun surpoidssurpoids, le chercheur ne prend pas la nouvelle avec beaucoup d'inquiétude mais décide de se focaliser sur les marqueurs du diabète, comme l'insulineinsuline et les voies métaboliques du glucoseglucose.
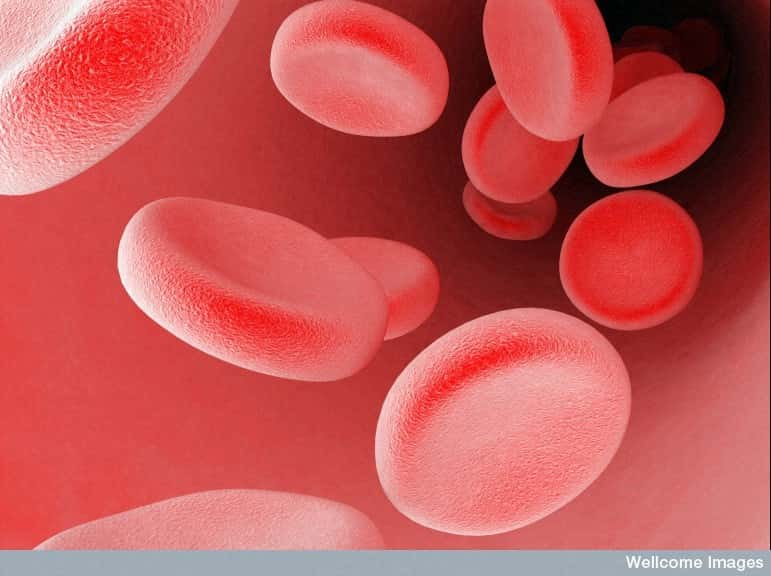
Une simple prise de sang suffit pour fournir de très nombreux renseignements. En effet, puisqu'il vient alimenter tous les organes du corps et en récupérer les déchets, le sang contient une très grande variété de molécules, dont certaines peuvent être utilisées comme biomarqueurs pour prévenir ou annoncer des maladies. © Wellcome Images, Flickr, cc by nc nd 2.0
Quelque temps plus tard, il est de nouveau infecté, cette fois par un virusvirus respiratoire syncytial, sans conséquence grave sur la santé. Pourtant, simultanément, les scientifiques remarquent une hausse de la glycémieglycémie. Un médecin finira même, pendant que l'étude était en cours, par le diagnostiquer diabétiquediabétique. Une découverte intéressante pour Snyder, qui pense qu'il avait certes des prédispositions au diabète de type 2, mais que c'est l'infection qui a déclenché la maladie. Or, jamais dans la littérature scientifique un tel lien n'avait été établi.
Grâce à ce suivi longitudinal, on a pu montrer les changements moléculaires impliqués dans la transition entre un état sain et un état diabétique. Snyder pense qu'en répétant ce genre d'études chez de nombreux individus, il pourrait être possible de mieux connaître les mécanismes moléculaires se mettant en place dans certaines maladies, ainsi que la réponse immunitaire qui en découle.
Médecine génomique personnalisée : de la population à l’individu
Ce genre de travail a malgré tout des limites. Il est difficile d'extrapoler à l'ensemble de la population les résultats obtenus chez un seul être humain. Pour George Church, de l'université d'Harvard, à l'origine du Personal Genome Project, dont l'objectif est de séquencer le génomegénome de 100.000 volontaires, ce constat n'est pas un défaut mais une qualité. Sur le site InternetInternet de la revue Nature, il défend l'idée que les études menées à grande échelle commettent parfois l'erreur de regrouper ensemble des personnes qui n'ont aucun lien, faussant les données statistiques.
« Nous avons davantage besoin d'investiguer à l'échelle individuelle, explique Church. La médecine traite les gens comme des individus, et nous devrions adopter la même attitude lors de recherches scientifiques. »
Quant à Snyder, il s'étonne de constater qu'un examen médical se limite au maximum à une vingtaine de constituants. « Quand on va voir un médecin et qu'on vous fait une prise de sang, seules une vingtaine de mesures sont effectuées. Avec les technologies actuelles, nous devrions être capables d'en récolter des milliers, si ce n'est des dizaines de milliers, voire des millions. Cela produirait une image plus fidèle de ce qu'il se passe. »
Pour l'anecdote, Snyder a communiqué à sa compagnie d'assurance les nouvelles informations dont il disposait sur sa santé. Ses cotisations sont devenues spontanément bien plus chères. Mais il veut voir le bon côté des choses, considérant que la génomique lui a sauvé la vie. Depuis qu'il se sait diabétique, il a changé ses habitudes alimentaires et son mode de vie. En attendant peut-être de pouvoir déceler l'âge de sa mort dans ses gènes...