au sommaire
Notre colonne vertébrale est constituée d'un empilement de vertèbres. Son articulation et sa flexibilité sont possibles grâce à la présence des disques intervertébraux qui forment comme des coussins entre les vertèbres. Les pathologies dégénératives des disques vertébraux sont liées aux sollicitations importantes et répétitives auxquelles est soumise la colonne vertébrale tout au long de la vie : port de charges, sports, mouvementsmouvements répétitifs, torsiontorsion. Avec le temps, les disques s'usent, se dégradent et ne peuvent plus jouer leur rôle d'amortisseur. Si ces pathologies sont d'apparition lente et progressive, elles se traduisent rapidement par des douleurs au niveau de la zone où les disques sont endommagés. On estime que la dégénérescence des disques intervertébraux est responsable d'environ 40 % des douleurs lombaires. Les recherches actuelles se focalisent donc sur la mise au point de traitements qui ralentissent ou empêchent la dégénérescence des disques et des cellules qui les composent.
D'un point de vue physiologique, le noyau pulpeux, la partie centrale des disques intervertébraux, est le premier touché. Il est composé en grande partie d'eau, ce qui lui confère ses propriétés d'amortisseur. Avec l'âge, les cellules pulpeuses deviennent progressivement moins prolifératives, plus sujettes à l'apoptose et incapables de produire cette fameuse matrice extracellulairematrice extracellulaire très hydratée.
Comment alors les remplacer par des cellules fonctionnelles ? Les chercheurs se sont intéressés au tissu adipeux qui constitue un grand réservoir de cellules souchescellules souches capables de se différencier dans une vaste gamme de types cellulaires. Encore fallait-il trouver le bon protocoleprotocole pour réussir à ce que des cellules souches du tissu adipeuxtissu adipeux puissent se transformer en cellules du noyau pulpeux.
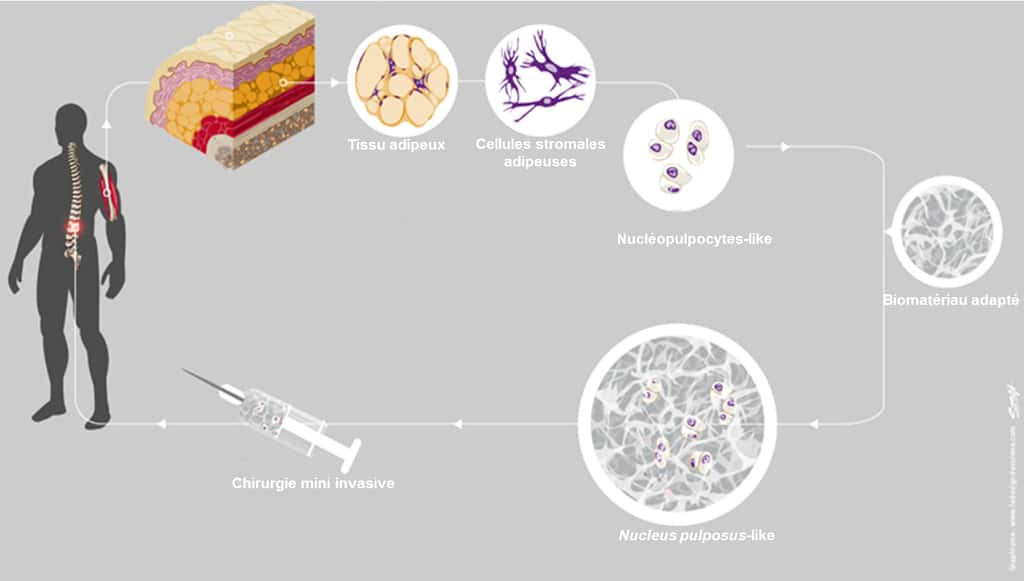
Les cellules sont cultivées avec des facteurs de croissance. Elles seraient ensuite associées avec un biomatériau de synthèse et réinjectées au patient. © Inserm, S. Renaudin/le Design de Solène pour l’Inserm
Un biomatériau couplé aux cellules
La mise au point de ce protocole peut s'apparenter à une recette de cuisine. Les chercheurs ont su trouver les bons ingrédients et le bon dosagedosage afin qu'elle soit réussie. La stratégie gagnante a consisté à ajouter au milieu cellulaire une combinaison de deux facteurs de croissancefacteurs de croissance, du TGFβ et du GDF5. En 28 jours les chercheurs ont obtenu in vitroin vitro, à partir de tissu adipeux prélevé chez neufs patients, des cellules de noyau pulpeux fonctionnelles et ressemblant à celles existant naturellement dans les disques intervertébraux.
« Le protocole s'est avéré être une réussite indépendamment de l'âge et du poids des patients, précise Jérôme Guicheux (Unité Inserm 791, Laboratoire d'ingénierie ostéo-articulaire et dentaire, Nantes). Nous devions néanmoins aller plus loin car ces cellules n'avaient aucune chance de survivre en étant réimplantées seules dans un disque intervertébraldisque intervertébral abîmé et dépourvu de tout le substratsubstrat nutritif qui leur est nécessaire. »
La seconde astuce a donc été de coupler ces cellules à un biomatériau de synthèse pour récréer un environnement favorable à leur multiplication une fois qu'elles seraient injectées dans le disque intervertébral. Les chercheurs ont évalué l'activité biologique de ces cellules in vivoin vivo après leur transplantationtransplantation chez la souris. « Ce dispositif est celui qui se rapproche le plus d'une transplantation intradiscale chez l'Homme. Nous avons démontré que le protocole que nous appliquons à ces cellules était suffisant pour qu'elles conservent leur activité sécrétoire spécifique et leur phénotypephénotype spécialisé une fois réinjectées in vivo. »
Ce travail de médecine régénératrice, paru dans Stem Cells, permet désormais aux chercheurs d'envisager la prochaine étape avant le passage en clinique : tester l'efficacité thérapeutique de ces cellules toutes neuves dans un modèle animal pertinent de pathologie dégénérative des disques vertébraux.
Inserm
--------------
Présentation de l'Inserm
Créé en 1964, l’Institut national de la santé et de la recherche médicale (Inserm) est un établissement public à caractère scientifique et technologique, placé sous la double tutelle du Ministère de l’Éducation nationale, de l’enseignement supérieur et de la recherche et du ministère des Affaires sociales, de la santé et des droits des femmes. Ses chercheurs ont pour vocation l’étude de toutes les maladies, des plus fréquentes aux plus rares, à travers leurs travaux de recherches biologiques, médicales et en santé des populations. L’ensemble des équipes regroupe près de 15 000 chercheurs, ingénieurs, techniciens, gestionnaires, hospitalo-universitaires, post-doctorants…