au sommaire
Pour obtenir du cuivre pur, aujourd'hui, on procède par affinage électrolytique du sulfate. Voyons les propriétés et utilisations du cuivre.

Le cuivre à l'état natif se trouve rarement dans la nature. Généralement on le trouve dans les sulfures tels que la chalcopyrite (CuFeS2), la covelline ou covellite (CuS), la chalcosine ou chalcocite (Cu2S) ou la cuprite (Cu2O).

- Symbole : Cu
- Poids atomique : 63,54
- Numéro atomique : 29
- Rayon atomique (Van der Waals) 0,128 nm
- Structure électronique 1s2, 2s2, 2p6, 3s2, 3p6, 3d10, 4s1
- Isotopes : Cu63 (69,2 %) ; Cu65 (30,8 %)
- Densité : 8,92 (selon une autre source 8,86 à 15° C et 8,36 à 1 100 °C)
- Dureté 3 (Mohr)
- Température de fusionfusion : 1.084 °C
- Température ébullition : 2305 à Patm.
- RésistivitéRésistivité : 1,7347 microohm.cm à 20 °C
- Potentiel électrodeélectrode : Cu cristallisé - 0,3472 V à 25 °C
- Potentiel électrode : Cu finement divisé - 0,3452 V à 25 °C
- Coefficient de dilatationdilatation : 1,7 mm/m pour 100 degrés
- Coefficient de PoissonCoefficient de Poisson 0,34 à 20 °C
- Solubilité dans l'eau à 30 °C après 6 jours : 170.10-6 g/l
- Solubilité dans l'eau à 30 °C après 29 jours : 180.10-6 g/l
- Propriétés catalytiques bonnes pour adsorptionadsorption de H2 ou SO2 ou CO par ex.
Avec l'or, le cuivre est le seul métal naturellement coloré
- Présence moyenne dans l'ensemble de l'écorce terrestre : 55 g à la tonne.
- Présence dans les organismes vivants : 1 à 10 milligrammes par kgkg.
- La raie Kα du cuivre a pour longueur d'ondelongueur d'onde moyenne 1,54182 Å.
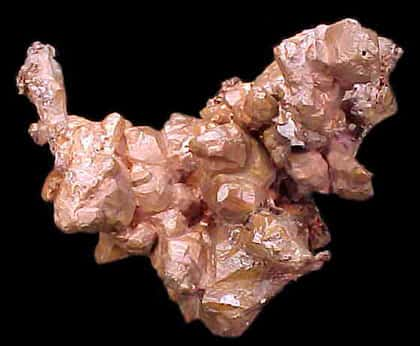
Le cuivre, meilleur conducteur de l'électricité après l'argent
La conductibilitéconductibilité électrique du cuivre a été prise comme référence par la Commission électrotechnique internationaleCommission électrotechnique internationale en 1913 et la résistivité du cuivre, d'une valeur de 1,724 microohm.cm à l'état recuit, est l'étalon de cette mesure. La conductibilité du cuivre est, par définition, égale à 100 % IACS (International Annealed Copper Standard). Seul l'argentargent a des performances légèrement meilleures sur ce point (environ 106 IACS).
La solidité du fil de cuivre et la fiabilité des contacts qu'il permet d'obtenir sont les raisons essentielles de l'emploi généralisé du cuivre dans toute l'industrie de la constructionconstruction électrique et des composants électroniques. À titre d'exemple, 95 % des fils conducteurs d'un Airbus sont en cuivre. Si une très haute fiabilité de contact est nécessaire, comme dans un satellite, on envisage alors une dorure, une argenture ou un étamage : le cuivre s'adapte très bien à ces revêtements de surface.

Propriétés, utilisations et effets du cuivre
Conductibilité thermique : le cuivre étant le métal usuel conduisant le mieux la chaleurchaleur, cette propriété est mise à profit pour chauffer ou refroidir rapidement un liquideliquide ou un gazgaz : chauffe-eau ou chaudières, radiateursradiateurs, condenseurs et réchauffeurs des centrales électriques, thermiques, nucléaires (environ 200 tonnes d'alliagesalliages de cuivre pour 1.000 mégawatts installés).
RésistanceRésistance à la corrosioncorrosion : le cuivre et ses alliages ne sont pas attaqués par l'eau ni par un grand nombre de produits chimiques : tuyaux en cuivre, récipients, conteneurs, robinetterierobinetterie, toiturestoitures. En milieu marin, on l'allie à l'aluminiumaluminium ou au nickelnickel pour lui donner une bonne résistance à l'agression contre l'eau de mer. Les pompes et canalisationscanalisations d'eau de mer, dont les débitsdébits atteignent parfois plusieurs m3 par seconde (plateformes pétrolières off-shoreoff-shore, navires, centrales électriques de bord de mer sont en cupro-aluminium ou cupro-nickel). Les bronzesbronzes et laitonslaitons résistent mieux à l'eau de mer seulement si le pourcentage de cuivre est plus grand que 70. La dégradation des cuivres dans les milieux contenant de l'oxygèneoxygène est souvent due aux courants électriquescourants électriques résultant de l'inégalité d'accès de l'oxygène aux différentes parties de la surface du métal. Dans les chaudières par exemple, la corrosion est alors due à la soude caustiquesoude caustique qui se forme dans l'eau.
Usinabilité et traitements de surface : le cuivre n'a pas en lui-même une grande aptitude à être usiné. En revanche, certains de ses alliages, et tout particulièrement le laiton, ont d'excellentes capacités d'usinabilité et notamment aux grandes vitessesvitesses. Le cuivre et ses alliages se prêtent très bien à la plupart des traitements de surface.
Malléabilité et plasticitéplasticité : c'est un métal extrêmement ductileductile. Non allié, il n'y a pratiquement pas de limite à son travail à froid. Le cuivre et les alliages cuivreux se laminent facilement en tôles, se martèlent en feuilles très minces et s'étirent en fils extrêmement fins. Ils se prêtent particulièrement bien à la déformation à chaud.
Soudabilité : le cuivre et ses alliages se soudent bien, qu'il s'agisse de soudage autogène, de souduresoudure électrique, de brasagebrasage ou de soudage à l'étain.

Esthétique : l'or de bijouterie contient d'ailleurs jusqu'à 15 % de cuivre. La couleurcouleur naturelle du cuivre est rose saumonsaumon, mais il apparaît souvent rouge par suite de son oxydationoxydation superficielle ; cette couleur est recherchée en décoration de même que la couleur jaune du laiton, qui se révèle plus ou moins soutenue suivant le pourcentage de zinczinc contenu. Soumis aux intempéries lorsqu'il est utilisé en toiture, le cuivre prend dans un premier temps une couleur brun foncé, puis une patinepatine vert clair très adhérente, qui le protège de toute oxydation ultérieure.
Amagnétisme : cette propriété lui vaut de nombreuses applicationsapplications, en tout premier lieu dans l'horlogerie, mais aussi dans la construction électrique et électronique, et dans l'armement (dragueurs de mines).
Un comportement mécanique obtenu dans le cuivre nanocristallin : ce matériaumatériau présente un comportement élasto-plastiqueplastique quasi parfait, un phénomène qui n'avait encore jamais été observé (Centre d'études de chimiechimie métallurgique du CNRS - CECM, Vitry-sur-Seine et du Laboratoire d'ingénierie des matériaux et des hautes pressionspressions du CNRS (LIMHP, Villetaneuse), publication dans Science du 11.04.2003.
Les grains sont très petits : 80 nanomètresnanomètres. On suit la déformation en fonction de la force appliquée. Pour obtenir un tel matériau, deux techniques ont été employées : la production de poudre ultra-fine par évaporation-condensationcondensation cryogénique et l'extrusionextrusion différentielle à froid. Les propriétés mécaniques obtenues sont exceptionnelles : le cuivre nanocristallin est trois fois plus résistant que le cuivre classique, il se déforme de manière homogène par un écoulement constant de la déformation jusqu'à la rupture. Les chercheurs ont ainsi observé pour la première fois un comportement élasto-plastique quasi parfait. Ce comportement pourrait s'expliquer par un glissement des grains les uns par rapport aux autres dans un écoulement fluide. Le comportement observé ouvre des perspectives très intéressantes pour la mise en forme plastique des matériaux à température ambiante. (Texte tiré du journal du CNRS)
Propriétés biologiques : La circulaire DRT no 92-14 du 29 août 1992 précise l'interdiction de recourir à des travailleurs temporaires, notamment pour des travaux de soudure pouvant exposer à l'inhalationinhalation des poussières de métauxmétaux durs (nickel, cuivre, etc.) (Circ. DRT no 92-14, 29 août 1992).
Poison dangereux : la dose mortelle est de 15 mg/kg de poids corporel, il est en général éliminé par l'organisme mais peut s'accumuler dans le foiefoie ou les reinsreins.
La maladie de Raynaudmaladie de Raynaud : le cuivre est nécessaire à la vie : l'homme et les animaux ont besoin d'absorber quotidiennement quelques milligrammes de cuivre pour assurer la formation de l'hémoglobinehémoglobine du sang. Le cuivre est largement distribué dans l'organisme, qui en contient environ 100 mg, principalement musculaire, hépatique et cérébral.
Le cuivre intervient dans diverses enzymesenzymes aux fonctions variées : minéralisation osseuse, synthèse protéique, neurotransmission, immunitéimmunité, oxydation du glucoseglucose, c'est aussi un puissant antioxydantantioxydant.
La cuprémie est habituellement comprise entre 64 et 156 µg/dl et les valeurs normales de la céruléoplasmine varient entre 180 et 400 mg/l.
Hypocuprémie. Le syndromesyndrome de Menkès, maladie récessive liée à X, carencecarence majeure en cuivre, se traduit par une anémieanémie avec leucopénieleucopénie, des anomaliesanomalies osseuses (fractures, déformations), des troubles cutanéscutanés, des cheveux blancs cassants, un retard mental sévère, des hémorragies internes, des convulsionsconvulsions chez l'enfant et la mort vers 3 ans.
La déficience modérée en cuivre est quant à elle fréquente, 30 %, dans la population française mais est cliniquement asymptomatique. Le déficit en cuivre est un facteur de risquefacteur de risque des maladies cardiovasculairesmaladies cardiovasculaires. Elle altère également l'immunité, provoque de l'ostéoporoseostéoporose...
L'apport massif de cuivre est responsable d'une intoxication aiguë avec diarrhéediarrhée hémorragique, vomissements (couleur bleue des sels cuivriques) et une anémie hémolytique. Une intoxication chronique peut résulter d'un apport en cuivre quotidien trop élevé (plus de 0,5 mg de cuivre par kilo et par jour). La cirrhosecirrhose indienne est due à la cuisson dans des récipients de cuivre. Une supplémentation non contrôlée peut constituer un risque d'intoxication. La maladie de Wilsonmaladie de Wilson, héréditaire autosomiqueautosomique récessive, résulte d'un défaut d'excrétion biliaire.
Des propriétés bactéricides. Le cuivre a des propriétés bactéricides reconnues, il assainit les canalisations qui sont utilisées dans le monde entier pour l'eau, la bière, les confitures et la distillation des alcools. II n'existe pas de maladie professionnelle dans l'industrie du cuivre.

Le cuivre a des propriétés antifouling. Ces propriétés consistent à empêcher la fixation d'algues et d'organismes marins. Cette propriété, qui s'ajoute à la résistance à la corrosion, est utilisée pour toutes les applications marines.
Les sels de cuivre, comme le sulfate, ou l'oxychlorure, présentent des propriétés fongicidesfongicides mises à profit pour la viticulture et l'agricultureagriculture : bouillie bordelaise par exemple, qui fait même partie des produits chimiques utilisés en agriculture biologiqueagriculture biologique.