au sommaire
Mesures de capacités calorifiques négatives : des copeaux de métal qui fondent….
Cette fascinante analogieanalogie entre le macroscopique et le microscopique nous donne aussi la possibilité de vérifier expérimentalement ces paradoxes thermodynamiques : si une étoile il faut se contenter de l'observer dans un télescope, des petits agrégats d'atomes peuvent par contre être produits et étudiés en laboratoire.

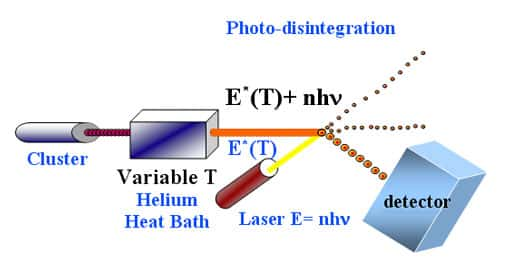
Expérience de fusion d'agrégats de sodiumsodium. Les agrégats constituent un faisceau qui passe dans un four contenant des atomes d'Helium qui leur impose aux une température donnée qui peut être contrôlée de l'extérieur. A la sortie du four, les agrégats sont illuminés par un faisceau laserlaser et évaporent des atomes qui sont détectés dans le détecteur. Le nombre d'atomes évaporés permet d'établir avec précision l'énergieénergie contenue dans chaque agrégat.
C'est ainsi que en 2001, des capacités calorifiques négatives semblent avoir été observées par l'équipe du professeur Helmut Haberland à Fribourg dans le cas de la fusion des agrégats métalliques 4 : durant la fusion d'un infime copeau de sodium ne contenant que 147 atomes la température baisserait de près de 10 degrés Celsiusdegrés Celsius.
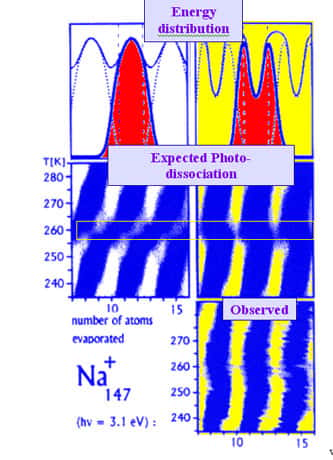
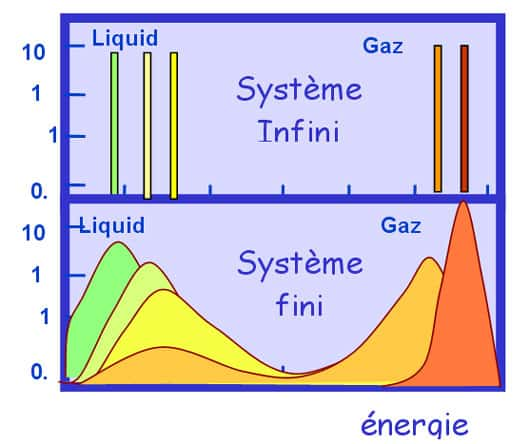
Resultats de l'expérience de fusion d'agrégats de sodium 4 Haut : deux hypothèses possibles pour la distribution d'énergie des agrégats dans le four. Celle de gauche est normale, et celle de droite correspond à une capacité calorifique négative, c'est à dire une diminution de température lors de la fusion. Centre : distribution du nombre d'atomes évaporés à différentes températures attendue dans les deux cas. Bas : distribution mesurée expérimentalement. Nous pouvons voir que l'hypothèse de capacité calorifique négative est en meilleur accord avec les données.
4 M.Schmidt et al., Phys.Rev.Lett.86 (2001) 1191.