au sommaire
Ce que les étoiles et les noyaux ont en commun
Nous pouvons maintenant comprendre pourquoi la même phénoménologie d'une capacité calorifique négative est attendue pour deux objets aussi différents comme une étoile rayonnant dans l'espace et un agrégat de quelques centaines d'atomes ou même un microscopique noyau atomique excité par un accélérateur de particules. L'étoile avec son rayon un milliard de milliards de fois plus grand que l'agrégat, d'un point de vue thermodynamique est un objet petit au même niveau que ce dernier, dans les deux cas la portée de la force (la distance sur laquelle la force agit) étant comparable aux dimensions linéaires de l'objet.
Nous venons de voir qu'un système a capacité calorifique négative doit nécessairement être isolé ; que se passe-t-il donc quand ces étonnants objets sont mis en contacte thermique ? La température décroît dans le passage d'une phase à l'autre : ceci implique que les états a capacité calorifique négative ont une énergie intermédiaire entre les deux phases. Or pour une température fixe dans la zone de transition seuls deux états d'énergie sont possibles, correspondant aux deux phases. Le système à capacité calorifique négative à contacte avec un bain thermique ne peut donc plus tergiverser entre les deux phases, et doit obligatoirement sauter sur son état d'équilibre plus stable, ce qui revient à accomplir une transition de phase.

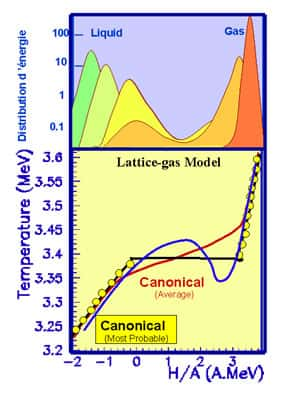
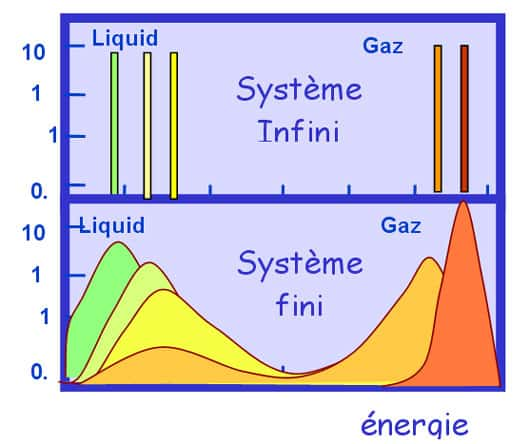
Calcul de la distribution d'énergie lors de la vaporisation d'un système liquide. A haut, pour un système infiniment grand, en bas pour un système composé de 200 particules. Chaque couleur correspond à une valeur différente pour la température. La région à énergie intermédiaire entre le liquide et le gaz est associée à une capacité calorifique négative. C'est région n'est pas accessible au liquide infiniment étendu.
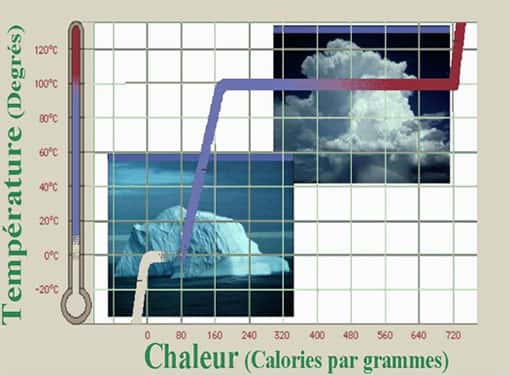
Nous pouvons maintenant comprendre pourquoi la capacité calorifique négative d'une gouttelette microscopique en ébullition se transforme dans un palier de température quand une casserole d'eau est posée sur le feufeu dans nos cuisines macroscopiques. En effet toute portion microscopique du système en ébullition, s'il était isolé du reste de la casserole, apparaîtrait comme un système a capacité calorifique négative; le contacte thermique avec le reste du système force notre microscopique portion d'eau à choisir entre le liquideliquide et le gazgaz, produisant ainsi le bien connu palier de coexistence.
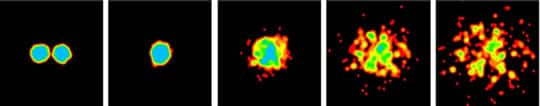
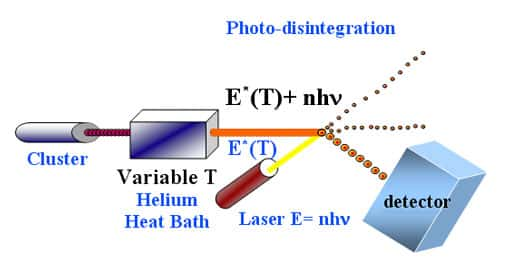
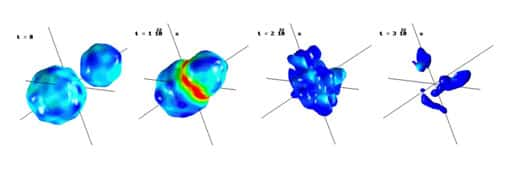
Simulation numérique de multifragmentation lors d'une collision nucléaire auprès des accélérateurs de particules

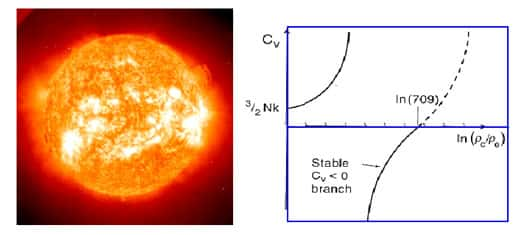
Vue artistique d'une explosion de supernovae de type II.
Dans le cas de l'étoile par contre, le fait que l'espace interstellaire soit essentiellement vide permet une stabilité sur des temps infinis (compatiblement avec la duréedurée du combustiblecombustible nucléaire), ce qui a pour étonnante conséquence la stabilité des conditions thermiques sur la terre !