au sommaire
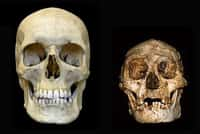
L'achondroplasie est une maladie génétique rare caractérisée par un développement osseux anormal. Les personnes atteintes de ce défaut de croissance, qui touche les os des membres inférieurs et supérieurs ainsi que certains os du crâne, sont de petite taille, n'excédant pas les 135 cm environ à l'âge adulte. Dans les cas plus sévères, des déformations du crâne et des vertèbres peuvent aboutir à des complications neurologiques ou orthopédiques.
L'origine de cette pathologie est la mutation du gène Fgfr3 (fibroblast growth factor receptor 3)). La protéine issue de ce gène est un récepteur connu pour son rôle dans la régulation de la croissance des os. En temps normal, la croissance est permise uniquement par un mécanisme subtil, au cours duquel le facteur de croissancefacteur de croissance FGF se fixe au récepteur FGFR3 et s'en détache. Dans le cas de l'achondroplasie, la perturbation du couple formé du facteur de croissance et du récepteur empêche la croissance des os de façon constante.
Dans cette étude publiée dans la revue Science Translational Medicine, les chercheurs de l'Inserm et de l'université de Nice Sophia Antipolis ont trouvé un moyen de prévenir l'activation constante de la protéine. Ils ont mis en place une nouvelle stratégie qui consiste à utiliser un leurre, des récepteurs FGFR3 humains solubles fonctionnels injectés chez des souris atteintes de la maladie, pour rétablir l'équilibre nécessaire entre l'activation et l'inhibitioninhibition de la croissance des os.
Souris naines de taille adulte
Les souris atteintes de nanismenanisme ont reçu pendant leurs trois premières semaines, période où elles sont en pleine croissance, deux injections par semaine de la solution contenant les récepteurs FGFR3 solubles. Grâce à ces récepteurs normaux supplémentaires, le facteur de croissance se fixe et se détache normalement, rétablissant la croissance des os.
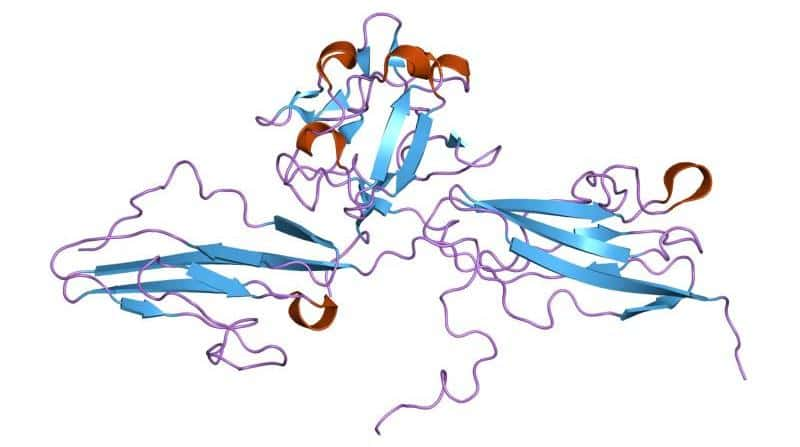
La protéine FGFR3, ici modélisée, a été très bien conservée durant l'évolution. La mutation du gène Fgfr3 entraîne des cas de nanisme, parmi lesquels ceux provoqués par l'achondroplasie. © Jawahar Swaminathan, MSD staff at the European Bioinformatics Institute, Wikipédia, DP
Les souris mutées grandissent alors normalement, et atteignent la taille adulte moyenne. Les chercheurs ont ensuite suivi les souris pendant huit mois après l'arrêt du traitement, pour s'assurer qu'il n'y avait pas de signes de toxicitétoxicité. Grâce à cette surveillance, ils ont par exemple constaté que l'augmentation de la taille du bassinbassin permet une reproduction avec des portées identiques aux souris non atteintes de la pathologie.
« De façon surprenante, notre stratégie prévient les complications les plus sévères observées chez les souris (baisse de la mortalité, problèmes respiratoires, etc.). De ce fait, on pourrait penser que le traitement pourrait permettre, par simple injection, d'éviter la chirurgiechirurgie chez des enfants atteints de la pathologie », explique Elvire Gouze, chargée de recherche à l'Inserm.
Vers un premier traitement du nanisme ?
Actuellement, aucun traitement n'a fait ses preuves pour prévenir le développement de la maladie, même si certains ont été testés, comme l'injection d'hormone de croissance ou l'allongement chirurgical des os, sans résultats probants.
« Le produit que nous avons testé dispose d'atouts majeurs par rapport à ceux testés dans d'autres études en cours : sa duréedurée de vie dans l'organisme est suffisamment longue pour ne pas nécessiter d'injections quotidiennes. Nous pensons que notre approche pourrait être efficace pour traiter les enfants atteints d'achondroplasie et peut-être d'autres formes de nanisme », souligne la chercheuse, principal auteur de l'étude.
Les chercheurs vont désormais s'attacher à vérifier l'absence d'effets toxiques à long terme. Avant d'entreprendre des études cliniques chez l'Homme, ils devront également trouver la dose minimale pour laquelle le traitement est efficace, et celle où il devient toxique. Les scientifiques pourraient aussi chercher à savoir s'il est possible de démarrer plus tardivement le traitement, ce qui permettrait à un plus grand nombre de personnes d'en bénéficier.