au sommaire

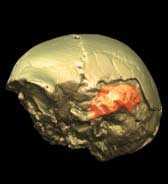
L'ecdysone, un système hormonal, est bien un frein à la croissance : quand son taux est réduit au cours du développement larvaire, on obtient un adulte de plus grande taille (à droite).© P. Léopold
« On le sait, le facteur génétique pèse très lourd dans la taille finale d'un être vivant, de 60 à 80 %, (3) annonce le généticiengénéticien. Et on connaît deux paramètres fondamentaux qui la fixent : la vitessevitesse et la duréedurée de la croissance. »Ces deux paramètres sont sous le contrôle de deux systèmes hormonaux fort différents. D'un côté, des facteurs de croissance appelés IGF (4)sont réceptionnés à la surface des tissus et activent la croissance des cellules grâce à des voies de signalisation spécifiques. De l'autre, les hormones stéroïdiennes contrôlent la durée de la période de croissance. Chez l'homme, le pic de sécrétion d'hormones stéroïdiennes lors de la puberté provoque à la fois une augmentation de la vitesse de croissance et la fin de la période de croissance. Bref, plus la puberté est tardive et plus les individus grandissent longtemps.
Jusqu'à présent, les chercheurs avaient peu d'indices concernant les interactions entre ces deux systèmes hormonaux au niveau cellulaire. Les résultats apportés sur la drosophiledrosophile par le groupe de Pierre Léopold permettent aujourd'hui de mieux comprendre ces interactions, avec de fortes probabilités que cela s'applique aux vertébrésvertébrés. Mais pourquoi travailler sur la mouche ? « Parce que l'on dispose chez cet insecteinsecte d'outils génétiques très sophistiqués permettant de manipuler facilement son génomegénome et parce que les deux systèmes hormonaux sont très semblables chez l'homme et la mouche, quoique plus simples chez cette dernière »,
affirme le chercheur. Et qui dit plus simple dit plus facile à étudier. « Le décorticage des voies de signalisation cellulaires, grâce aux outils permettant l'inactivation d'un gènegène par exemple, y est alors réalisé beaucoup plus vite que chez la souris ou sur des cellules humaines. »
Du coup, les deux systèmes hormonaux, les IGF( 5 )et l'ecdysone - l'équivalent chez l'insecte des hormones stéroïdiennes chez l'homme -, ont révélé leur liaison cachée : « Foxo, que l'on savait avoir un rôle d'inhibiteur de l'amplitude de la croissance en agissant au cœur de la signalisation des hormones de type IGF, s'est avéré à notre surprise être également un relais des hormones stéroïdesstéroïdes pour le contrôle de la durée de la croissance
», annonce Pierre Léopold. Autrement dit, chez l'insecte, à chaque phase de son développement, Foxo intègre à la fois les effets des facteurs de croissance et ceux des horloges biologiqueshorloges biologiques pour jouer un rôle de frein moteur sur la croissance. À terme, ces résultats pourraient notamment intéresser les spécialistes du cancer du seincancer du sein, dans lequel ces deux familles d'hormones sont fortement impliquées.
Fabrice Impériali
1. Institut CNRS / Université de Nice Sophia Antipolis.
2. ProtéineProtéine localisée dans le noyau cellulaire qui permet d'activer l'expression d'un gène sous forme d'ARN messagerARN messager et de produire des protéines nécessaires à l'exercice d'une fonction (par exemple la division cellulaire).
3. Les deux autres paramètres déterminants sont l'environnement socio-économique et la nutrition.
4. InsulineInsuline-like Growth Factor.
5. Chez les invertébrésinvertébrés, la séparationséparation fonctionnelle entre l'insuline, qui contrôle la glycémieglycémie, et les IGF, qui agissent sur la croissance, n'est pas clairement établie comme chez l'homme.
Contact :
Pierre Léopold
Institut de signalisation, biologie du développement et cancer, Nice
[email protected]