au sommaire
Vous avez toujours voulu savoir comment était fabriqué un médicament ? Grâce à ce dossier, retrouvez toutes les étapes du cycle du médicament, qui permettent de s'assurer de son efficacité et de son innocuité, en partant de sa conception jusqu'à sa distribution.

Les étapes du cycle du médicament
L'obtention d'un nouveau médicament est une étape de longue haleine qui fait interagir un grand nombre d'acteurs aussi bien dans le domaine médical qu'administratif. Le temps nécessaire entre la découverte d'une molécule prometteuse et l'arrivée du médicament sur le marché est de l'ordre d'une dizaine d'années.
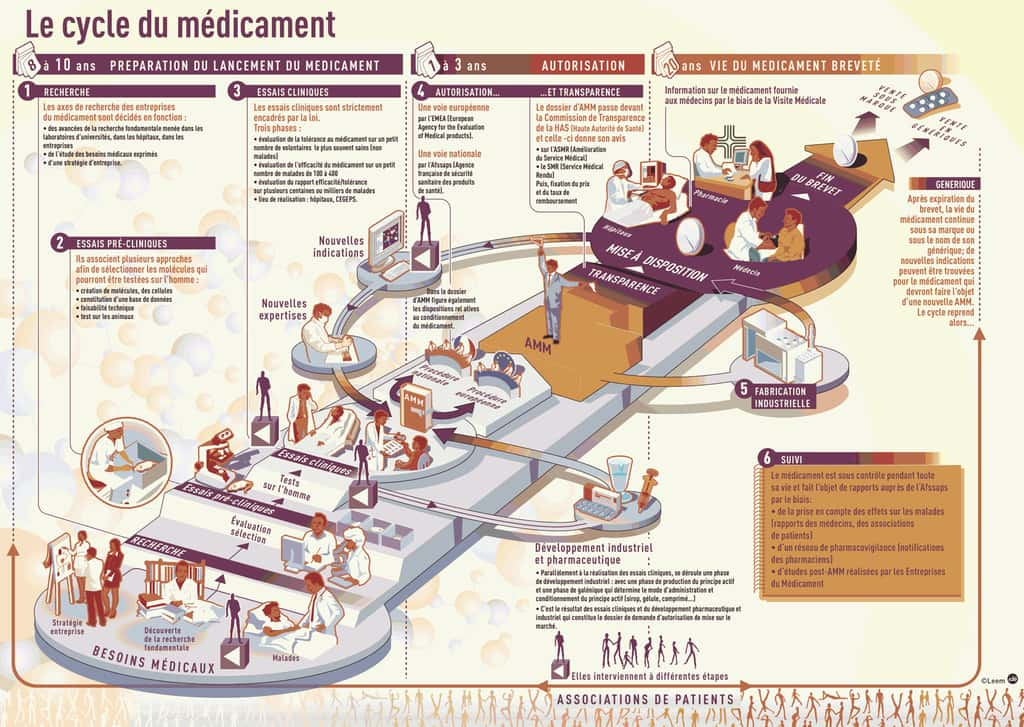
Quelles sont les recherches nécessaires à l'obtention de molécules potentiellement utiles ? Quels sont les tests effectués avant les essais cliniquesessais cliniques réalisés sur l'Homme ? Qui autorise la mise sur le marché des médicaments et dans quelles conditions ? Quels contrôles sont effectués pour s'assurer que le médicament remplisse bien ses fonctions ? Retrouvez toutes les réponses à ces questions dans les pages de ce dossier.
À noter
Après l'affaire du Médiator, les organismes gérant la mise sur le marché des médicaments ont été restructurés. Dans ce dossier, nous citons Philippe Lechat, directeur de 2007 à 2012 de l'évaluation des médicaments et des produits biologiques à l'Agence française de sécurité sanitaire des produits de santé (Afssaps). En 2012, l'Agence nationale de sécurité du médicament et des produits de santé (ANSM) s'est substituée à l'Afssaps. L'ANSM a repris pleinement les droits, missions et obligations de l'Afssaps et a été dotée d'une nouvelle organisation et d'un mode de gouvernance entièrement revu. L'ANSM évalue à la fois la qualité, l'efficacité, les risques sanitaires et les bénéfices liés aux médicaments et produits de santé en assurant le contrôle des médicaments en laboratoire ainsi que les autorisations de mise sur le marchéautorisations de mise sur le marché (AMM).
À lire aussi sur Futura
- À quoi sert la DCI d'un médicament ?
- Un puissant antibiotique découvert grâce à l'IA
- Les médicaments contiennent des excipients pas si inoffensifs que ça
- Une thérapie génique pour des enfants-bulles testées aux États-Unis