au sommaire
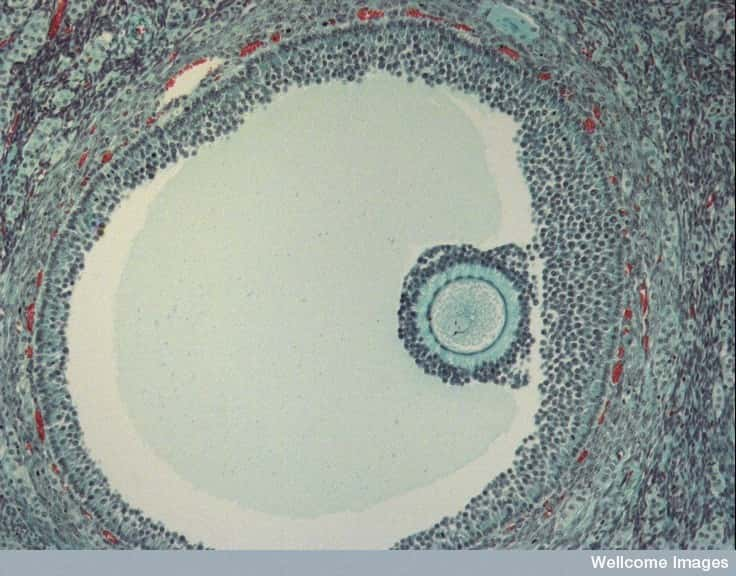
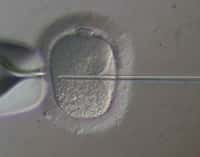
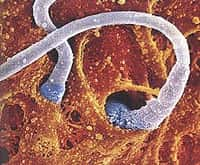
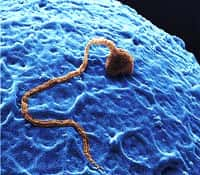
L'ovocyte est une cellule germinale qui mûrit dans un follicule, une structure fibreuse qui, entre autres, alimente l'ovocyte et le déverse pendant l'ovulation. Contrairement à ce que l'on croyait depuis les années 1950, le nombre de cellules germinales n'est pas fixe mais des cellules souches, certes minoritaires, contribuent à la formation de nouveaux ovocytes. © Wellcome Images, Flickr, cc by nc nd 2.0
Depuis soixante ans, le concept était bien établi : durant la grossesse, le fœtus de petite fille fabrique des millions d'ovocytes stockés dans les ovaires. On considérait alors qu'à la naissance, la petite fille détenait son stock définitif de cellules germinales, et qu'il n'allait cesser de diminuer au cours de l'existence sans aucune nouvelle synthèse. À la puberté, quelque 400.000 ovocytes sont disponibles, et lors de chaque cycle, un millier d'entre eux rentre en compétition pour devenir un ovuleovule mûr, mais un seul y parvient, tandis que tous les autres meurent.
Mais depuis 2004, ce modèle est remis en question puisque que des chercheurs du Massachusetts General Hospital (Boston), dirigés par Jonathan Tilly, avaient montré que des souris fabriquaient toute leur vie des ovules grâce à des cellules souchescellules souches germinales (appelées OSC), et que cela pouvait également s'appliquer à la femme. Ces travaux leur avaient valu quelques critiques, notamment concernant le manque de fiabilité de la méthode utilisée.
En 2009, des chercheurs de l'université Jiao Tong de Shanghai confirmaient ces résultats en utilisant une autre technique, moins soumise à polémique. Les embryonsembryons avaient même été fécondés in vitro et avaient atteint le stade blastocysteblastocyste avant d'être détruits.
Jonathan Tilly a donc repris ce protocoleprotocole pour vérifier la présence de ces OSC chez la femme et s'assurer qu'elles pouvaient effectivement mûrir et devenir des ovocytes. Son étude, parue dans Nature Medicine, l'atteste, et renverse donc un dogme qui semblait pourtant bien établi.
Des cellules souches OSC qui font tomber un dogme…
Les chercheurs ont récupéré les tissus ovariens de six femmes âgées entre 22 et 33 ans ayant subi une opération de changement de sexe. Ils ont d'abord isolé ces OSC (qui représentent une cellule ovarienne sur 10.000) à partir d'un marqueur protéique de surface appelé Ddx4, qu'on avait uniquement retrouvé jusque-là dans le cytoplasmecytoplasme d'ovocyte. Ces cellules se transformaient spontanément et obtenaient les caractéristiques des ovocytes, y compris en présentant un génotypegénotype haploïdehaploïde (la moitié du patrimoine génétiquegénétique) caractéristique des cellules germinales.
D'autre part, l'expérience a été poussée plus loin. Ces OSC ont été génétiquement modifiées pour exprimer une protéine fluorescente verteprotéine fluorescente verte, appelée GFP (green fluorescent protein)). Ces cellules ont été injectées dans du tissu ovarien, et le tout a été greffé sous la peau de souris dont le système immunitairesystème immunitaire est déficient, de manière à éviter tout rejet.
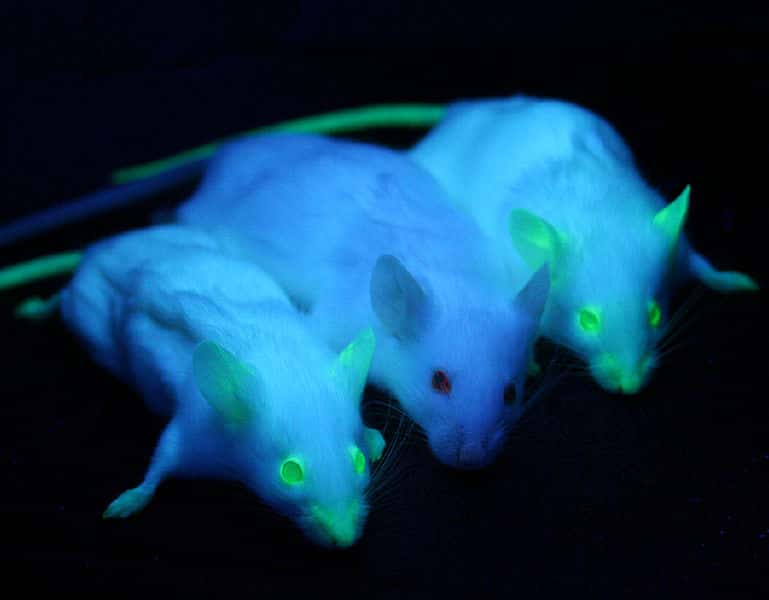
La GFP est une protéine qui a été extraite d'une méduse (Aequorea victoria) bioluminescente. Les scientifiques utilisent souvent ses propriétés dans le vivant en injectant un transgène comportant le gène pour étudier l'action d'une protéine spécifique ou localiser certaines cellules. Comme dans ce cas, la fluorescence apparaît sous un rayonnement ultraviolet. © Ingrid Moen et al., BMC Cancer, cc by 2.0
Le tissu humain a été examiné entre 7 et 14 jours après l'implantation. Leurs observations ont montré des folliculesfollicules humains immatures avec ou sans GFP. Ceux qui n'étaient pas colorés devaient déjà être présents dans l'extrait d'ovaire avant l'injection des OSC, tandis que les ovocytes en développement verts proviennent obligatoirement des cellules souches génétiquement modifiées.
… et qui laissent entrevoir un traitement contre l’infertilité
« Dans cet article, nous apportons les trois éléments clés que réclamaient les personnes plus sceptiques sur notre précédent travail, précise Jonathan Tilly. Nous avons développé et validé un protocole fiable pour purifier les OSC d'ovaires de mammifèresmammifères adultes, prouvant une fois de plus que ces cellules très spécialisées existent. Nous avons testé la fonction d'ovocytes de souris produits par ces OSC et montré qu'ils peuvent être fertilisés pour produire des embryons sains. Et nous avons identifié et caractérisé une population équivalente de cellules souches produisant des ovocytes à partir d'ovaires prélevés chez des femmes adultes. » La quatrième étape consiste à s'assurer que ces ovocytes humains sont fécondables et assurent un développement normal de l'embryon.
Mise à part la fin du paradigme que cette découverte entraîne, elle ouvre surtout des perspectives intéressantes pour les femmes souffrant d'infertilité, notamment celles victimes de maladies ou de traitements qui ont endommagé sévèrement les ovaires. Il serait en outre peut-être possible de retarder la ménopauseménopause, surtout pour des femmes chez qui elle se produit de manière précoce. Or, cela concernerait, d'après de précédents travaux, 10 % de la population féminine, alors que l'âge de mise au monde du premier enfant ne fait que reculer.