au sommaire
En 2011, 87 % des installations photovoltaïques installées dans le monde comportaient du silicium mono ou multi cristallin. Bien qu'étant l'élément chimique le plus abondant sur Terre après l'oxygène, le silicium ne peut être trouvé à l'état pur. Il doit donc être extrait de la silicesilice, purifié, mis en forme puis dopé avant d'être utilisé. Toutes ces opérations ont un important coût énergétique.
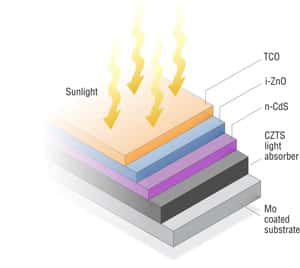
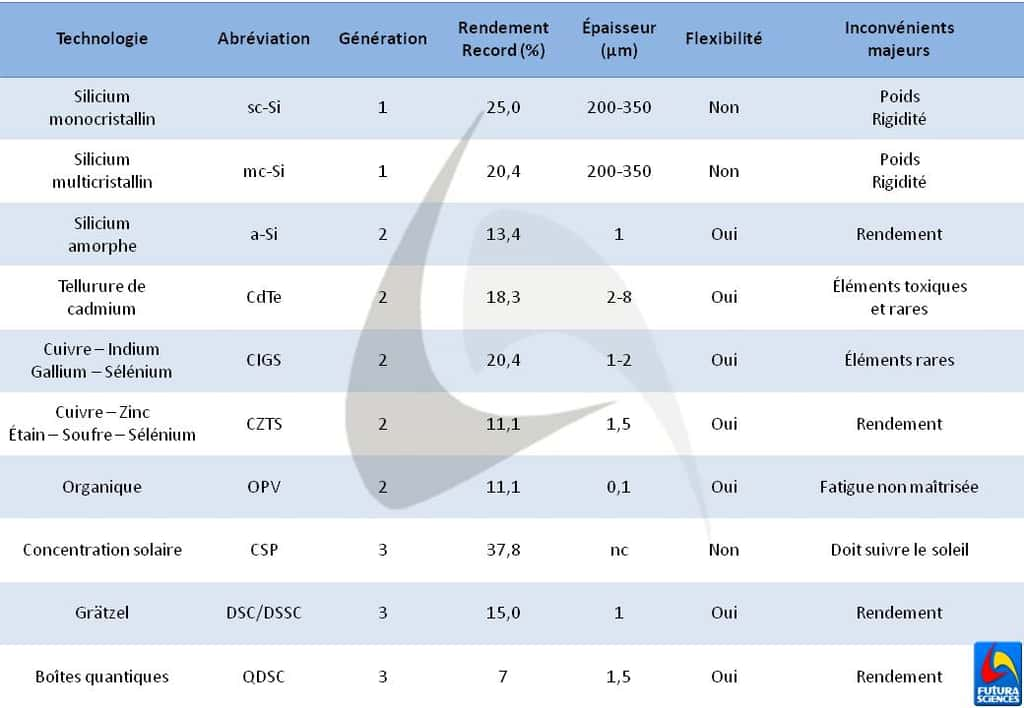
De nombreuses cellules photovoltaïquescellules photovoltaïques différentes existent de nos jours. Elles sont classées en trois générations. La première d'entre elles renferme les structures composées de silicium monocristallin ou multicristallin, qui se différencient donc par le procédé industriel employé pour fabriquer les galettes. La 2e génération rassemble les cellules dites à couches minces et les cellules organiques. Toutes les autres technologies (cellule de Grätzel, cellule à boîtes quantiques, etc.)) appartiennent à la 3e génération.
Les cellules au silicium cristallin équipaient à elles seules 87 % des systèmes photovoltaïques installés dans le monde en 2011. Perçons le secret de leur fabrication.
Le silicium, l’élément le plus abondant sur Terre après l’oxygène
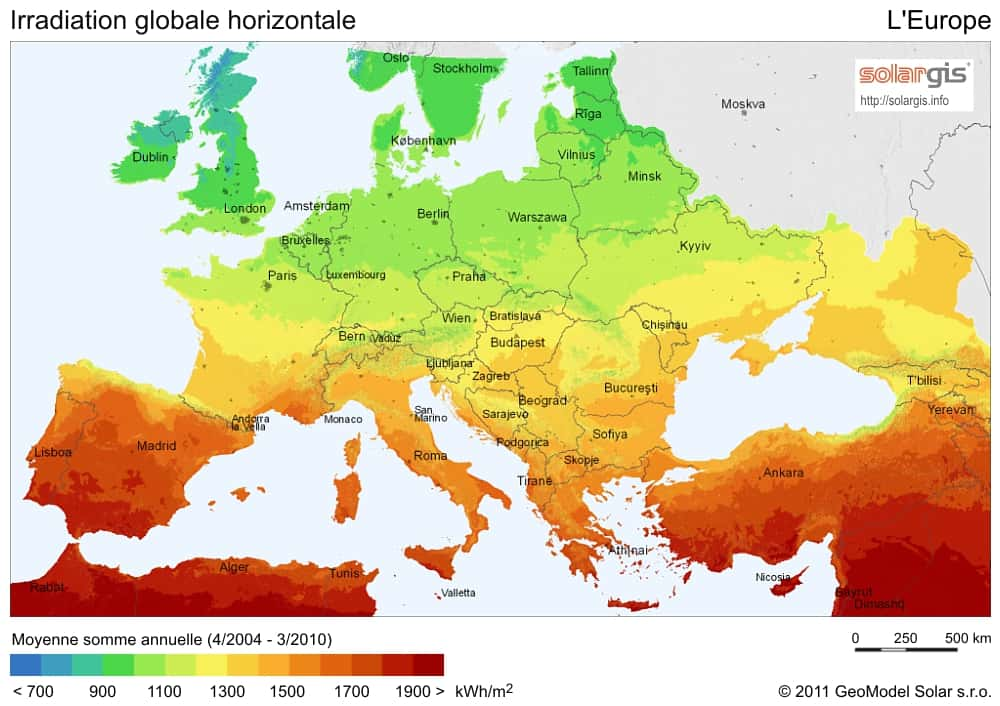
La croûte terrestrecroûte terrestre se compose à 25,7 % de silicium (Si). Cependant, cet élément, le plus abondant sur Terre après l'oxygène, n'est pas directement exploitable puisqu'il n'est pas présent à l'état pur. Il doit donc être extrait de différents minérauxminéraux, comme la silice (ou dioxyde de silicium SiO2), avant d'être exploité.

La silice correspond à la forme naturelle du SiO2. Ce minéral dur peut être trouvé dans des roches sédimentaires détritiques (comme le sable ou le grès), mais aussi dans des roches magmatiques ou métamorphiques. © Aschevogel, Flickr, cc by nc nd 2.0
Pour ce faire, il faut chauffer la matière première dans de puissants fours à arcs (jusqu'à 35 MW) afin d'atteindre des températures supérieures à 3.000 °C. Dans un premier temps, les blocs ou grains de silice sont placés dans une cuve en présence de matériaux réducteurs, tel du cokecoke. Les arcs électriquesarcs électriques sont ensuite générés entre des électrodes de graphitegraphite. Ils vont provoquer la montée en température, faire fondre la silice (dès 1.650 °C), puis faciliter la recombinaisonrecombinaison de ses atomes d’oxygène avec le carbonecarbone du matériaumatériau réducteur. Il s'en suit alors un dégagement de monoxyde de carbonemonoxyde de carbone (CO) et de dioxyde de carbonedioxyde de carbone (CO2) tandis que du silicium s'écoule hors du four par des orifices adaptés. Cette matière renfermant encore de nombreuses impuretés est à ce stade qualifiée de métallurgique.
Le silicium ne devient pur à 99,9999 % qu'après avoir subi différents traitements physiquesphysiques et chimiques complémentaires. Il est alors suffisamment pur pour être utilisé dans l'industrie photovoltaïque. C'est en adaptant l'étape suivante, la recristallisationrecristallisation, que le silicium va devenir soit monocristallin, soit multicristallin.
La fabrication des lingots de silicium
Le silicium multicristallin est facile à obtenir. Il suffit de placer la matière en fusionfusion dans un creuset en graphite, puis de la refroidir par le bas durant plusieurs dizaines d'heures. La solidificationsolidification se fait donc de bas en haut, tout en causant l'apparition de plusieurs cristaux à gros grains dans la colonne. Le lingot obtenu peut ensuite être découpé en briques de dimensions définies.
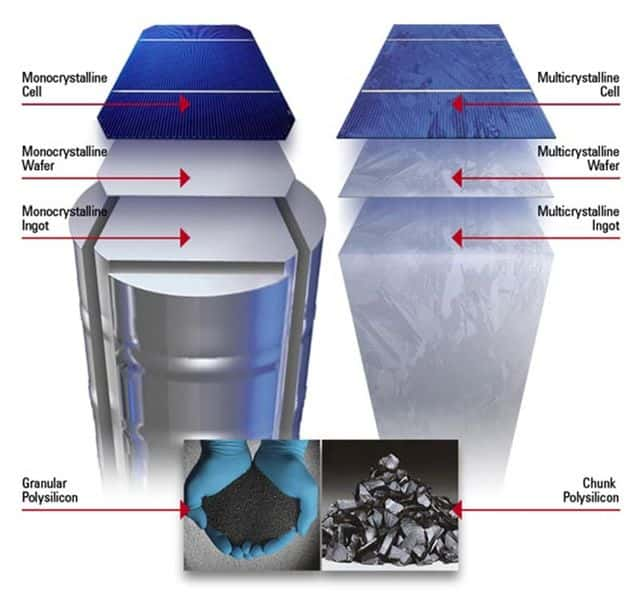
Le silicium monocristallin se présente sous la forme d’un cylindre composé d’un seul et unique cristal (à gauche). Cette structure subit, après sa fabrication, un équarrissage afin que les galettes produites par la suite aient une forme carrée (leurs coins sont cependant arrondis). Le silicium multicristallin est quant à lui directement refroidi dans une lingotière rectangulaire mais, comme son nom l’indique, il est fait d’un grand nombre de cristaux (ils correspondent aux taches visibles sur le lingot de droite). © DR
La fabrication du silicium monocristallin nécessite plus d'opérations (procédé de Czochralski). La matière première en fusion est coulée dans un creuset en quartzquartz où elle est maintenue à l'état liquideétat liquide, mais à la limite de la solidification, par chauffage. L'atmosphèreatmosphère est alors neutralisée grâce à l'injection d'argonargon, afin d'éviter tout problème d'oxydationoxydation. Par la suite, un germe monocristallin présentant une orientation cristallographique connue est mis en contact avec le liquide, puis progressivement tiré vers le haut (vitessevitesse de 1 mm/sec) et mis en rotation (30 tours/min). Du silicium liquide est alors entraîné à sa suite. Il va rapidement refroidir et donc se solidifier, tout en adoptant l'orientation cristallographique du précurseur.
Il se forme ainsi un seul et unique cristal géant de forme cylindrique. Il est ensuite équeuté (les extrémités riches en impuretés ou mal cristallisées sont retirées), avant de subir une opération d'équarrissage. Ses bords sont donc coupés de manière à lui donner une forme carrée, mais avec des coins arrondis.
Un lingot pour 2.000 wafers de silicium
Les lingots et les briques sont ensuite simultanément découpés en plusieurs centaines de plaques grâce à des scies à fils (certaines entreprises en découpent jusqu'à 2.000 en une fois). Ces galettes, ou waferwafer en anglais, font 200 à 350 µm d'épaisseur.
Près de 30 à 40 % de la matière est perdue durant cette étape, car les scies à fil font au moins 150 μm de diamètre, et le volumevolume scié est réduit en poudre. Elle peut cependant être recyclée sous certaines conditions, par exemple lorsque le silicium monocristallin a été débité à l'aide d'une scie diamantée. Les plaquettesplaquettes multicristallines sont pour leur part découpées avec des fils métalliques recouverts par d'autres mélanges d'abrasifs.
Le dopage, la clé de la jonction p-n
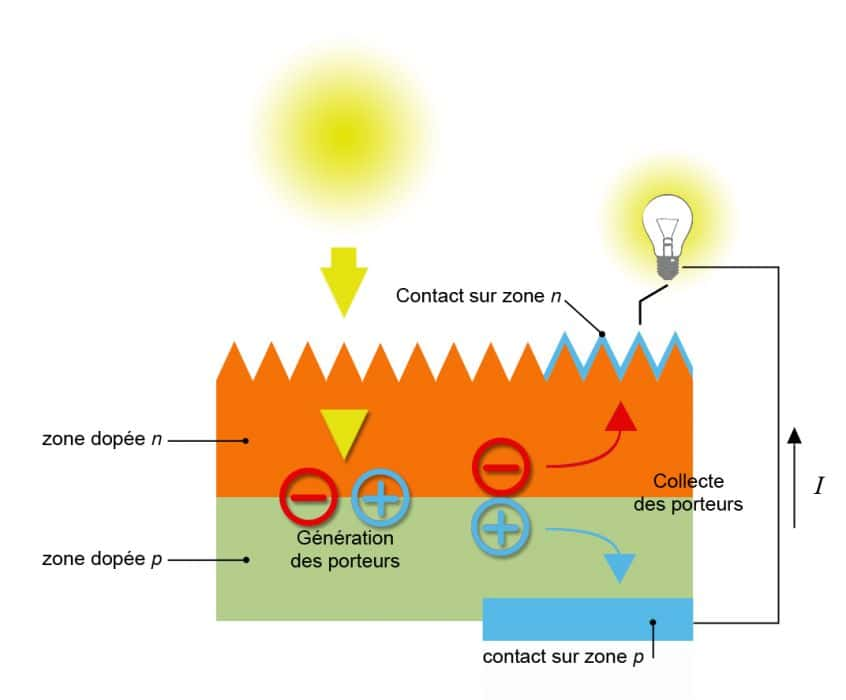
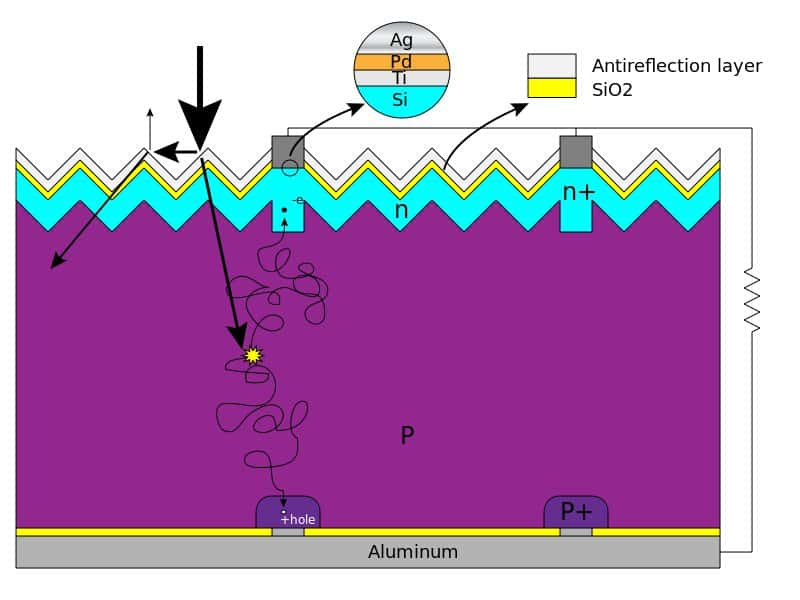
À ce stade, les galettes de silicium sont dopées uniformément p ou n, selon leur position initiale dans le lingot. La prise de contact des deux côtés n'aboutirait donc pas à la création d'une jonction p-n. Certaines zones de la plaquette doivent donc être enrichies en phosphorephosphore ou, à l'inverse, en borebore.
Plusieurs procédés existent, mais seul celui qui est majoritairement utilisé par les industriels est présenté : la diffusiondiffusion thermique. L'opération requiert à nouveau de hautes températures. Les galettes doivent en effet être chauffées entre 800 et 900 °C, avant qu'un gazgaz contenant la solution dopante, par exemple du chlorure de phosphoryle (type n) ou de diborane (type p), ne soit injecté dans le milieu. La chaleurchaleur permet alors au dopant d'acquérir suffisamment d'énergieénergie pour pénétrer dans la matière, et ainsi aller s'immiscer entre des atomesatomes de Si. Petit détail, un dopagedopage efficace ne s'obtient que lorsque la température du four est parfaitement homogène.
Les autres procédés industriels de dopage sont : l'implantation ionique, la transmutation et la technique par laserlaser. Dès la fin de cette étape, la jonction p-n est créée, les galettes peuvent être assemblées pour donner naissance à une cellule photovoltaïque cristalline.