au sommaire
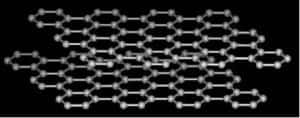
La structure du graphite, du grec "graphein" = écrire (crayon à mine, encre de chine)
Le graphite est un minéral noir friable utilisé depuis des siècles pour l'écriture (encre de Chine, crayon à mine).
La structure du graphite est constituée d'un empilement de plans, chacun étant constitué d'un pavage régulier d'hexagones en nid d'abeilles.
Chaque atome de carbone est relié dans le plan des hexagones à trois atomes voisins par des liaisons faisant entre elles des angles de 120°. Ces liaisons planes sont fortes et caractérisées par une distance entre atomes de 0,142 nm.
Les atomes sont au contraire faiblement reliés aux atomes des plans voisins, et la distance entre plans d'hexagones est de 0,34 nm.
Cette structure a une densité d'un tiers plus faible que celle du diamant et définit le graphite comme un solide très anisotrope, quasi-bidimensionnel car les plans faiblement reliés glissent facilement les uns par rapport aux autres.
Propriétés et utilisations du graphite
Le graphite est un conducteur de l'électricité, ce qui en fait un matériau de choix pour des applications comme les batteries au lithium-ionbatteries au lithium-ion et les électrodesélectrodes. Sa structure particulière permet également une excellente lubrification en raison du faible frottement entre les couches de carbone. Cela le rend idéal pour les applications nécessitant des propriétés de lubrification comme dans les moteurs ou les machines.
Applications technologiques et industrielles
En plus de son utilisation traditionnelle dans les crayons, le graphite est crucial dans la production d'acieracier comme un agent de carburisation pour renforcer le métalmétal. Il joue également un rôle vital dans les freins à disque pour avions, où il améliore la résistancerésistance à la chaleurchaleur. Avec l'avènement de la technologie moderne, le graphite est également utilisé dans les écrans tactilesécrans tactiles, les panneaux solaires et comme un substratsubstrat pour la croissance de semiconducteurssemiconducteurs.
Le graphite dans la recherche avancée
La recherche scientifique profite également des propriétés uniques du graphite. Par exemple, il est utilisé dans les expériences de physiquephysique pour étudier les propriétés des électronsélectrons dans des structures bi-dimensionnelles. Sa capacité à former des composés intercalaires, où des moléculesmolécules ou atomes sont insérés entre les plans de carbone, ouvre de nouvelles voies pour la création de matériaux avec des propriétés électriques, thermiques ou chimiques modifiées.
Impact environnemental
Le graphite est considéré comme relativement respectueux de l'environnement car il est naturel, abondant, non-toxique, et recyclable. Toutefois, son extraction peut être associée à des problèmes environnementaux significatifs tels que la dégradation des habitats, la pollution de l'airair et de l'eau. Des efforts sont donc nécessaires pour réduire les impacts de l'extraction du graphite et promouvoir des pratiques minières plus durables.
Pour plus d'informations sur les propriétés physiques et chimiques du graphite, des études récentes sont disponibles sur des plateformes comme arXivarXiv.org, où les chercheurs partagent leurs dernières découvertes.
Sources scientifiques pour approfondir vos recherches sur le graphite :
























