au sommaire

La glace dans la mer
On distingue deux types de glace : les icebergs, constitués d'eau douceeau douce, résultent de l'écoulement des glaciersglaciers polaires vers la mer. Les banquisesbanquises sont produites par la congélation de la surface de la mer. Ces dernières jouent un rôle important dans le bilan thermique de la planète.

Iceberg
La température du maximum de densité de l'eau pure est supérieure à celle de son point de congélation. Mais la présence de sels abaisse ces deux températures. A partir d'une salinité de 24,7 la température du maximum de densité est inférieure à celle du point de congélation (figure 3.8).
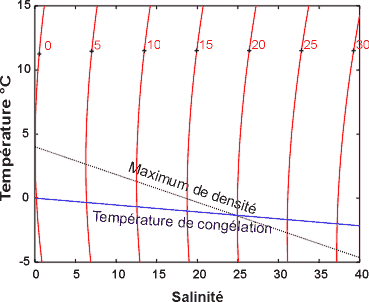
Figure 3.8 : Maximum de densité en fonction de la salinité. Les courbes graduées de 0 à 30 représentent la densité .
La salinité des océans est de l'ordre de 35. Le refroidissement de l'eau de mer s'accompagne donc d'une augmentation de densité jusqu'au changement d'état, contrairement au refroidissement de l'eau douce. Ceci explique en partie pourquoi la glace se forme plus facilement sur un lac qu'en mer. Sur un lac, les eaux les plus froides restent en surface et vont donc geler dès que la température devient négative. En mer les eaux refroidies en surface "plongent" et sont remplacées par de l'eau plus chaude. Pour créer une banquise il faut donc un refroidissement brutal.
Le changement d'état s'accompagne d'une dilatationdilatation, la glace est moins dense que l'eau et que la congélation va séparer l'eau pure des sels. Avant d'en étudier les conséquences, voyons ce que donne en laboratoire la congélation d'une cuvette d'eau de mer à S=35 lorsqu'on abaisse progressivement la température :
- à -1,91°C apparition du premier cristal de glace (eau pure) ce qui accroît la salinité de l'eau environnante. Pour voir apparaître un deuxième cristal il faut donc diminuer la température.
- Lorsque la température diminue on a de plus en plus de glace dans une saumuresaumure de plus en plus dense.
- à -8,2°C cristallisation du sulfate de soudesoude.
- à -23°C cristallisation du chlorure de sodium.
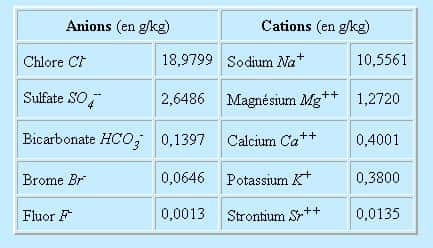
A la fin de l'expérience on obtient :
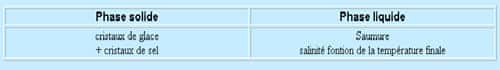
En mer les conditions ne sont pas aussi idéales :
- la surface est agitée (vaguesvagues)
- la température ne s'abaisse pas de façon régulière et continue
- le froid n'agit que sur la surface.
La glace qui se forme au cours des hivershivers arctiquearctique et antarctiqueantarctique se distingue donc de la glace créée en laboratoire. La glace reste en surface alors que la saumure s'enfonce pour être remplacée par de l'eau plus chaude et moins salée. Il se crée une eau très dense (très salée et très froide) qui va s'enfoncer très profondément. Lorsque la glace atteint une épaisseur de 2 à 3 m, elle forme un écran protecteur qui isole l'océan.
Cette glace est inhomogène, sous l'action des vagues et des oscillations de température, elle va renfermer des poches d'air et des poches de saumure ou de sel. Elle va ensuite vieillir, être lavée par la neige et devenir de plus en plus dense. On obtient des glaces de densités variables (0,86 à 0,92) et de compositions variables (salinité de 0 à 10), riches en sulfates.
La fonte de la glace donne naissance à des eaux de surfaces peu salées et froides (riches en sulfates).