au sommaire

Radiopionniers : les Curie, savants atypiques
Le sujet des rayons uraniques était donc presque abandonné, quand Pierre CuriePierre Curie suggéra à Marie d'en faire le sujet de sa thèse de doctorat. S'il n'avait pas le prestige social d'un Becquerel, Pierre Curie était pourtant un physicienphysicien exceptionnel. Il avait découvert en 1880 avec son frère Jacques la piézo-électricité (la propriété du quartzquartz de générer par déformation des charges électriques) et en avait donné l'explication, il avait étudié en détail le magnétisme (la « loi de Curie » et le « point de Curie » en gardent la mémoire), et beaucoup réfléchi aux questions de symétrie (« principe de Curie »)). Brillant théoricien, il était aussi concepteur d'instruments de précision (balance de Curie, électromètre de Curie, etc.). Il était professeur à l'École de physique et de chimie industrielles de la ville de Paris (EPCI) où il disposait d'un très modeste laboratoire. La personnalité et la vie de Maria Sklodowska sont bien connues par les nombreuses biographies de Madame Curie, à commencer par celle de sa fille Ève.
La brillante étudiante polonaise avait épousé en 1895 Pierre Curie, leur première fille Irène était née le 12 septembre 1897, et Marie décida de commencer une thèse de doctorat (la première femme en France à se lancer dans cette aventure).

Elle choisit d'étudier les rayons uraniques de Becquerel et de rechercher si d'autres corps que l'uranium pouvaient en émettre. « La question était entièrement nouvelle » écrivit-elle en 1923 dans sa biographie de Pierre. Ce n'était pas tout à fait exact, d'autres physiciens avaient déjà eu la même idée, mais leurs résultats étaient très confus.
Marie décida d'utiliser l'ionisationionisation de l'airair pour détecter et comparer l'activité de différents échantillons et surtout d'employer pour cela l'électromètre de KelvinKelvin, grandement perfectionné par Pierre, pour mesurer l'intensité du courant d'ionisation de ses échantillons.

La plaque photographique était lente, l'électroscope peu précis, l'électromètre était l'outil idéal, mais son utilisation était très délicate. L'idée de base est simple : un échantillon est placé entre les deux plaques d'un condensateurcondensateur (une chambre d'ionisation) dont on mesure le courant de décharge grâce à l'électromètre : le passage du courant fait pivoter un miroirmiroir suspendu à un long fil de torsiontorsion en quartz, ce pivotement dévie un faisceau lumineux réfléchi par le miroir et qui revient sur une règle graduée. La vitessevitesse de déplacement de la tache de lumièrelumière mesure l'intensité du courant.

Les carnets de laboratoire remplis par Marie et Pierre Curie permettent de suivre leur cheminement, leurs hésitations, leurs doutes et leurs joies. Marie commença à utiliser l'électromètre le 16 décembre 1897, et elle ajouta au montage un quartz piézo-électrique le 20 janvier pour que les mesures soient plus stables et plus précises. Sous la tension d'un poids, le quartz générait une charge électrique bien déterminée, et il ne restait qu'à mesurer avec un chronomètrechronomètre le temps nécessaire au courant d'ionisation pour compenser cette charge. Ce « montage Curie » fut la clé de la réussite. Il resta utilisé plus d'un demi-siècle pour les mesures fines de radioactivitéradioactivité.

Le 10 février Marie put commencer ses premières mesures, en commençant, bien entendu, par reproduire les expériences de Becquerel, et surtout de Kelvin et ses collaborateurs, sur divers échantillons de sels d'uranium. Tous les composés de l'uranium se révélèrent actifs et cela d'autant plus qu'ils contenaient plus d'uranium : l'activité était bien liée aux atomesatomes, indépendamment de leur composition chimique. Cependant, elle remarqua le 17 février une anomalieanomalie avec deux mineraisminerais : la pechblende et la chalcolite. Ils étaient deux fois plus actifs que l'uranium, et c'est là que l'on voit l'importance des mesures quantitatives précises que Marie CurieMarie Curie était seule à exécuter. Mais la chalcolite de synthèse ne possédait pas cette propriété, et Marie supposa donc qu'elle était due à une « impureté » contenue dans la chalcolite et la pechblende naturelles dont la composition est complexe. Elle ne s'attarda cependant pas sur cette anomalie et continua à étudier systématiquement d'autres substances.


Pechblende et Chalcolite (ou torbernite)
Le 24 février, elle découvrit que le thoriumthorium émettait lui aussi des rayonnements similaires à ceux de l'uranium, et même qu'il était plus actif. Grâce aux relations de Pierre parmi les minéralogistes, elle put examiner « un grand nombre de métauxmétaux, sels, oxydes et minérauxminéraux » dans les collections de minéralogie de l'EPCI, de la Sorbonne et du Muséum. Mais seuls les composés de l'uranium et du thorium montrèrent une activité mesurable. Elle publia le 12 avril 1898 une note sur les « Rayons émis par les composés de l'uranium et du thorium » mentionnant l'activité anormale des minerais d'uranium. Elle se posa bien sûr la question de la source d'énergieénergie de ces rayons, et comme le thorium et l'uranium étaient les éléments les plus lourds connus (avec des massesmasses atomiques de 234 et 238), cela lui suggéra une explication ingénieuse :

On découvrait presque chaque année de nouveaux rayonnements et il était en effet logique de penser que certains corps pouvaient avoir la possibilité de les capter dans l'espace comme de petites antennes, plus ou moins efficaces selon la nature des corps et des rayonnements.
Cependant en Allemagne, à Erlangen, Gerhardt Schmidt l'avait précédée et il avait annoncé dès le 14 février que le thorium émettait des rayons de Becquerel. Dès qu'elle l'apprit, Marie Curie abandonna le thorium pour se focaliser sur l'anomalie découverte dans la pechblende. Comme elle venait de montrer qu'aucun élément connu ne pouvait en être responsable, elle pensa qu'il devait exister dans la pechblende un élément inconnu et beaucoup plus actif que l'uranium : puisqu'il n'avait pas été décelé chimiquement jusque-là, il devait être présent à l'état de traces, et donc être particulièrement actif.
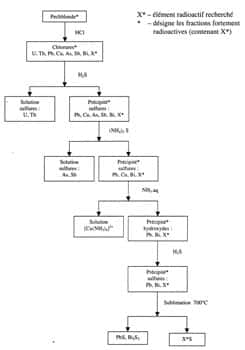
Pierre la rejoignit alors dans ses recherches, et ils se lancèrent dès le 14 avril dans la séparationséparation chimique des constituants d'un échantillon de quelques centaines de grammes de pechblende. Marie avait reçu une bonne formation de chimiste en Pologne, mais ils n'avaient bien sûr aucune idée des propriétés chimiques de ce nouvel élément, et ils tâtonnèrent donc quelque peu. Ils reçurent l'aide de chimistes de l'EPCI, Gustave Bémont en particulier, et ils utilisèrent les méthodes usuelles de chimie minérale, en se guidant « par le contrôle de l'activité radiante des produits séparés à chaque opération ».
Finalement, le « corps actif » resta avec le bismuthbismuth, et ils l'en séparèrent en répétant des cristallisations fractionnéescristallisations fractionnées (les premiers cristaux qui apparaissaient étaient plus actifs que la solution). Ils obtinrent ainsi un corps 400 fois plus actif que l'uranium, qu'ils proposaient d'appeler poloniumpolonium, en l'honneur de la patrie de Marie (alors partagée entre les empires russe, allemand et austro-hongrois). Les Curie annoncèrent leur résultat dans une note du 13 juillet 1898 à l'Académie des Sciences avec le titre « Sur une substance nouvelle radio-active, contenue dans la pechblende ». C'était la première fois qu'apparaissait le terme de radioactivité. Comme le thorium et le polonium émettaient des rayons « uraniques », ce terme ne paraissait plus approprié : il s'agissait manifestement d'une propriété nouvelle de la matièrematière, la radioactivité.
Avec le recul, nous savons que cette substance « 400 fois plus active que l'uranium » contenait extrêmement peu de polonium : le polonium 210 est dix milliards de fois plus radioactif que l'uranium 238. Les Curie avaient en réalité isolé du sulfuresulfure de bismuth avec des traces (moins d'une partie par million) de polonium. Cela explique que la spectroscopie n'ait pu déceler d'autres raies que celles du soufresoufre et du bismuth. Isoler le polonium fut un long travail, le laboratoire Curie ne parvenant qu'en 1910 à isoler quelques milligrammes d'une substance contenant 1% de polonium, permettant d'identifier des raies caractéristiques dans son spectrespectre. De plus, le polonium 210 a une période de 140 jours, il disparaît donc rapidement des échantillons.
Dans la nature il est constamment régénéré par les désintégrations radioactives à partir de l’uranium.
Au cours de leur analyse, les Curie avaient repéré la présence d'une autre substance radioactive, au comportement chimique complètement différent.
Après une pause de trois mois, sans doute pour attendre la livraison de 5 kilos de pechblende, les travaux reprirent le 11 novembre. La méthode de séparation était analogue, quoique différant dans les détails, et Gustave Bémont apporta à nouveau une aide précieuse aux Curie. La nouvelle substance était si voisine du baryumbaryum qu'il était, là encore, impossible de l'en séparer par des méthodes purement chimiques et il fallut à nouveau recourir à la cristallisation fractionnée. La nouvelle substance demeurait mêlée à une forte proportion de baryum, mais l'activité du mélange dépassait 900 fois celle de l'uranium, et une raie inconnue apparaissait dans son spectre. Sur ces bases, les Curie proposèrent, le 26 décembre 1898, dans une communication à l'Académie des Sciences l'existence d'une nouvelle substance extrêmement radioactive, à laquelle ils donnèrent le nom de radiumradium.

Le radium 226 est en fait trois millions de fois plus radioactif que l'uranium 238, et le mélange final contenait donc moins d'un millième de radium, mais c'était suffisant pour que des raies caractéristiques apparaissent dans le spectre du mélange. Il était cependant clair pour les Curie que des quantités énormes de minerai, se chiffrant en tonnes, seraient nécessaires pour extraire des quantités utiles de radium : pour continuer les recherches, il fallait passer rapidement à une échelle industrielle !