au sommaire
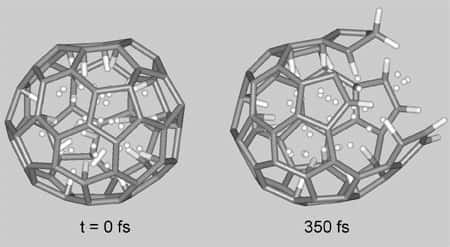
Représentation d'une simulation d'un C60. Crédit : Dr. Pupysheva
Imaginons que l'on veuille remplacer l'essence de nos voitures par de l'hydrogène, quelles sont les performances à atteindre ? Il faut savoir qu'un gramme d'hydrogène gazeux suffirait pour déplacer une automobileautomobile de taille moyenne sur une distance de 100 mètres. Mais dans les conditions de température et de pression ordinaires, un tel gramme occupe 22,4 litres !
Un rapide calcul montre que pour effectuer un trajet de 400 à 500 kilomètres, il faudrait disposer de 4 à 5 kgkg d'hydrogène, soit presque 100.000 litres pour une seule voiture dans les conditions normales de température et de pression.
La solution qui vient à l'esprit est de stocker cet hydrogène sous forme liquide, donc à une température inférieure à 20 K, ou bien sous forme gazeuse, mais à des pressions de plusieurs centaines d'atmosphèresatmosphères. Aucune de ces options n'est vraiment idéale...
Il existe pourtant une troisième possibilité, et c'est celle que Boris Yakobson et ses collègues Olga V. Pupysheva et Amir A. Farajian ont étudié plus en détail sur ordinateurordinateur, à l'aide d'une simulation de dynamique moléculaire.
On savait déjà depuis longtemps que les molécules de buckminsterfullerène (en anglais buckyball)), à soixante atomesatomes de carbonecarbone (découvertes d'ailleurs à l'Université de Rice, là où Yakobson enseigne), pouvaient stocker de 23 à 25 molécules d'hydrogène. On pouvait donc imaginer un stockage facile et sûr de l'hydrogène, sous forme d'une poudre, en le piégeant dans ces grosses molécules à peu près sphériques.
Il restait encore à savoir si l'on pouvait entasser plus de 25 molécules d'hydrogène dans ces grosses molécules en C60, une condition indispensable pour détrôner les moteurs à essence de nos voitures. En l'absence de données expérimentales, les simulations numériquessimulations numériques ont montré, à la grande surprise des chercheurs, que cela était non seulement possible mais que la relation entre la taille du fullerènefullerène considéré et le nombre de molécules d'hydrogène stockées était extrapolable à d'autres cages moléculaires que les C60.
De l'hydrogène métallique comme au cœur de Jupiter ?
Ainsi, les chercheurs ont découvert une relation générale entre la pression interne du gazgaz à l'intérieur de la cage moléculaire et son volumevolume, quel que soit le rayon de la cage.
Dans le cas des buckminsterfullerènes, il semblerait que l'hydrogène cesse d'exister sous forme moléculaire lorsque l'on dépasse 20 atomes d'hydrogène environ et que des liaisons covalentesliaisons covalentes avec les atomes de carbone se forment.

Des atomes d'hydrogène entassés dans des fullerènes. La pression est telle que l'hydrogène devrait presque se présenter sous forme métallique comme il semble l'être au centre de Jupiter (vue d'artiste). Crédit : Rice University
On peut alors grimper jusqu'à 58 atomes dans une seule molécule de C60 et à plus de 800 dans un fullerène C720. Ce qui stupéfie les chercheurs c'est que, si l'on calcule la pression atteinte dans ces cages moléculaires, on trouve que l'on s'approche de près de celle à laquelle l'hydrogène devient métallique, c'est-à-dire précisément ce qui se passe vers le centre de JupiterJupiter et de SaturneSaturne ! Une preuve de plus des remarquables propriétés de résistancerésistance mécanique des fullerènes et plus généralement des molécules parentes que sont les nanotubesnanotubes.
Il reste cependant deux étapes cruciales à franchir avant de disposer de voitures roulant à l'hydrogène. Ces résultats théoriques doivent d'abord être vérifiés expérimentalement. Il faut ensuite, et surtout, trouver le moyen d'injecter des molécules d'hydrogène dans des fullerènes et de les libérer à volonté. Ensuite, il faudra passer du stade de prototype de laboratoire à celui de la production à l'échelle industrielle.