Tous les éléments chimiques que nous connaissons dans la nature ont été créés par fusion d’éléments plus légers — comme la fusion de deux atomes d’hydrogène, aboutissant à la synthèse d’un atome d’hélium. Si la majorité des éléments se forment grâce aux réactions nucléaires au cœur des étoiles, les modèles indiquent que les éléments plus lourds que le fer (Fe) ne peuvent se former qu’au cours d’évènements cosmiques cataclysmiques, comme des supernovae ou des collisions d’étoiles à neutrons. Mais une récente étude vient de montrer que certains peuvent également se former au sein des étoiles, par réactions de fission d’éléments plus lourds que l’uranium (U) !
au sommaire
La formation des éléments chimiques (comme l'hydrogène ou le carbone) qui composent notre corps, les planètes ou encore les étoiles, est aujourd'hui relativement bien comprise. Selon les modèles, juste après le Big Bang, l'Univers est composé d'une soupe de neutronsneutrons et de protonsprotons. Grâce à la baisse rapide des températures quelques minutes après le Big BangBig Bang, ces particules élémentairesparticules élémentaires commencent à s'associer pour former les deux éléments chimiques les plus légers -- l'hydrogène, composé d'un proton et d'un neutron, et l'héliumhélium, composé de deux protons et de deux neutrons.
Les scientifiques appellent ce processus la nucléosynthèsenucléosynthèse primordiale, au cours de laquelle se sont formés les deux éléments les plus abondants de l'Univers. Il faut ensuite attendre la formation des premières étoiles pour voir apparaître des éléments chimiques plus lourds -- qui, grossièrement, contiennent plus de neutrons et de protons.
Des usines à éléments chimiques lourds
La nucléosynthèse primordiale ne parvient pas à expliquer l'existence d'éléments plus lourds que l'hydrogène et l'hélium -- que les astronomesastronomes qualifient de « métauxmétaux ». La synthèse de ces « métaux » nécessite des conditions où la matièrematière est très dense et où les températures sont très élevées : par exemple, le cœur des étoiles.
Rappelons que la température se traduit par une excitation de la matière, laquelle se met à se déplacer plus vite, agrandissant le nombre et la force des collisions entre les différentes particules (ainsi, plus il fait chaud, plus la matière est excitée et plus il y a de collisions). C'est ainsi au sein des étoiles que se forment les éléments plus lourds que l'hydrogène et l'hélium, par réactions de fusion thermonucléaire : les atomesatomes d'hydrogène (H) fusionnent pour former des atomes d'hélium (He), lesquels fusionnent pour former du BérylliumBéryllium (Be), et ainsi de suite jusqu'au ferfer (Fe).
L'ensemble de ces processus décrit ce que les scientifiques appellent la nucléosynthèse stellaire. Toutes les étoiles ne sont pas assez chaudes pour former des éléments aussi lourds que le fer ; par exemple, la fusionfusion de deux atomes d'oxygèneoxygène (O), qui peut aboutir à la formation d'un atome de soufresoufre (S), nécessite des températures de l'ordre du milliard de KelvinsKelvins, et n'intervient que dans les couches internes des étoiles « supergéantessupergéantes », au moins cinq fois plus massives que notre SoleilSoleil.
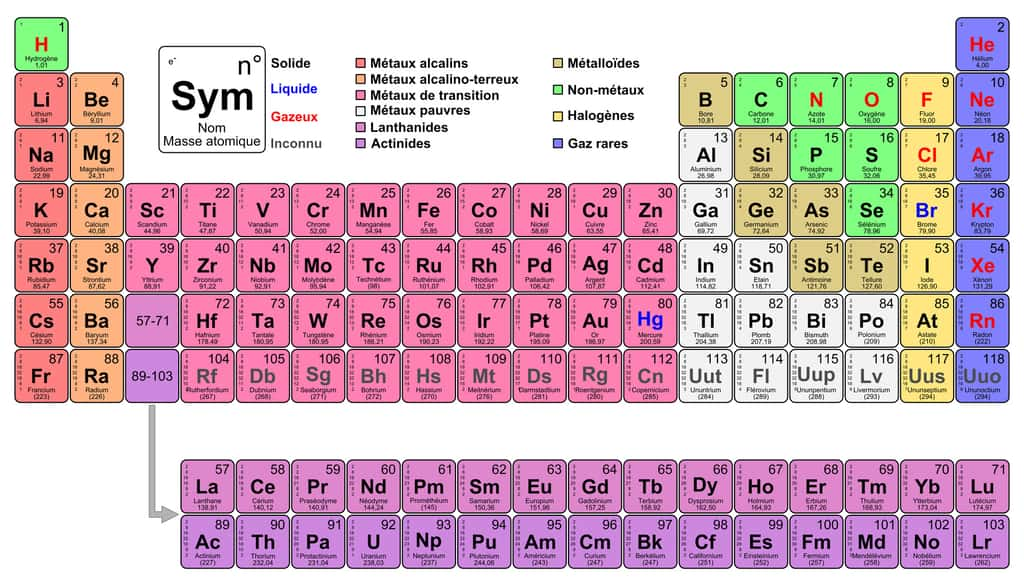
Si les atomes de fer sont les atomes les plus stables de la nature (et donc les plus résistants aux réactions de fusion thermonucléaire), on constate pourtant que le tableau périodique des élémentstableau périodique des éléments ne s'arrête pas là, et qu'il existe dans la nature de nombreux éléments chimiques plus lourds, comme l'or (Au) ou l'uraniumuranium (U). Ces éléments se forment par des processus de captures neutroniques : lorsqu'ils sont bombardés par d'intenses flux de neutrons, et qu'ils baignent dans des conditions de densité et de température extrêmes, des éléments chimiques lourds peuvent absorber des neutrons pour former de nouveaux éléments encore plus lourds, bien que plus instables (ou radioactifs : ils se désintègrent avec le temps en éléments plus légers).
Ces processus de captures rapides de neutrons ont lieu, par exemple, au sein de supernovae, des événements cosmiques de grande ampleur au cours desquels une étoile en fin de vie explose, libérant d'immenses quantités d'énergiesénergies et permettant l'apparition de conditions plus chaudes et plus denses qu'au sein des étoiles, propices à la formation d'éléments plus lourds que le fer. Ils peuvent également survenir au cours de la fusion entre deux étoiles à neutrons (principalement composées de neutrons maintenus ensemble grâce à la force de gravitationforce de gravitation), produisant d'énormes quantités d'énergie et de telles densités de neutrons que des atomes très lourds, comme l'uranium, peuvent se former. Ces phénomènes, nommés « processus r » (« r » pour rapide) décrivent en partie ce que les scientifiques appellent la nucléosynthèse explosive.
Si la synthèse des éléments chimiques connus semble plutôt bien comprise, les scientifiques ne savent pas si et comment des atomes plus lourds que l'uranium (qu'on appelle éléments transuraniques) peuvent se former dans la nature. Mais une nouvelle étude, publiée dans la revue Science, jette une nouvelle lumièrelumière sur les processus de nucléosynthèse. En analysant les compositions et abondances d'étoiles anciennes enrichies en éléments très lourds vraisemblablement formés lors de processus de nucléosynthèse explosive, l'équipe de scientifiques a montré que certains des éléments chimiques de massesmasses atomiques élevées pouvaient s'être formées à partir de réactions de fissionsfissions... d'éléments plus lourds que l'uranium.
Des éléments plus lourds que le fer formés dans les étoiles ?
En analysant les compositions et abondances des éléments chimiques de 42 étoiles anciennes de notre Voie lactéeVoie lactée, l'équipe de scientifiques a mis en évidence la présence d'éléments plus lourds que le fer, comme le rhuténium (Ru) ou l'argentargent (Ag). Les abondances de ces derniers semblaient d'ailleurs corrélées avec celles d'éléments encore plus lourds, dont certains lanthanideslanthanides (appartenant aux terres raresterres rares). En sachant que les températures au sein des étoiles ne sont pas assez élevées pour que la fusion d'éléments aboutissant à la formation d'atomes plus lourds que le fer n'ait lieu, il ne restait qu'une option plausible pour les scientifiques : ces éléments se seraient en fait formés par réactions de fission d'atomes encore plus lourds. Il apparaît ainsi que des éléments plus lourds que le fer peuvent se former dans le cœur des étoiles, non pas par réactions de fusion thermonucléaire, mais par réactions de fission d'éléments encore plus lourds.
Scénario généralisé de la formation des étoiles. © Nat Geo France
Les étoiles se forment à la suite de l'effondrementeffondrement sur eux-mêmes d'énormes nuagesnuages de gazgaz dans l'espace interstellaire ; la composition chimique de l'étoile reflète donc la composition chimique initiale du nuage de gaz. Si ce dernier contient des éléments chimiques lourds précédemment formés lors d'évènements cosmiques cataclysmiques de grande ampleur (comme des supernovaesupernovae ou des fusions entre deux étoiles à neutronsétoiles à neutrons), l'étoile formée à partir de ce nuage en contiendra également. Ainsi, la présence d'éléments chimiques plus lourds que le fer dans les étoiles observées, comme le rhuténium ou l'argent, tend à indiquer que ces étoiles présentaient lors de leur formation une composition chimique initiale enrichie en éléments chimiques encore plus lourds, formés lors de supernovae ou de fusion d'étoiles à neutrons.
Mais ce qui étonne le plus les scientifiques, c'est la masse atomique supposée de ces éléments chimiques très lourds : d'après les compositions et abondances des éléments chimiques dans les étoiles observés, des atomes dont la masse atomique dépasse 260 (encore plus lourds que l'uranium) auraient dû être présents lors de la formation de l'étoile ; les réactions de fissions les auraient par la suite fait disparaître. Des éléments aussi lourds n'ont pourtant jamais été observés à l'état naturel, que ce soit dans l'espace sur Terre, même lors de tests nucléaires.
Leurs résultats indiquent pourtant que de tels éléments pourraient bel et bien exister dans l'espace, bien que leur existence soit très brève. Ainsi, selon les scientifiques, les supernovae ou les fusion d'étoiles à neutrons créent des conditions de densité et de température tellement extrêmes que des éléments chimiques de masse atomique supérieure à 260 peuvent se former ; ils n'ont cependant pas pu être observés du fait de leur très faible duréedurée de vie.









