Des chercheurs sont parvenus à modifier les marques du vieillissement dans le génome de souris. Grâce à trois gènes, des souris ont retrouvé l'acuité visuelle de leur jeunesse.
au sommaire
Le vieillissement est-il inéluctable ? Ce processus, qui touche toutes les cellules, induit d'abord des dysfonctionnements avant de provoquer la mort cellulaire. Au niveau du génome, le vieillissement serait palpable. La communauté scientifique pense qu'il est dû à l'accumulation de modifications épigénétiques qui altèrent le fonctionnement normal des gènes.
Des scientifiques de l'école de médecine de l'université d'Harvard proposent une idée séduisante mais encore controversée : inverser les marques du temps accumulées dans le génome pour effacer le vieillissement. L'étude qu'ils publient dans Nature, le 2 décembre 2020, ne prouve pas formellement cette théorie, mais propose une série d'expériences qui la supporte.
Grâce à un cocktail de trois gènes, ils sont parvenus à limiter la dégénérescence des neurones et à promouvoir leur régénération. Des souris atteintes de glaucome ont alors récupéré leur acuité visuelle.
Trois gènes anti-âges
Les trois gènes choisis, Oct4, Sox2 et Klf4 (noté aussi OSK) par les scientifiques sont utilisés depuis une dizaine d'années dans des expériences de dédifférenciation cellulaire. Il s'agit là de transformer une cellule adulte différenciée en une cellule souche pluripotentecellule souche pluripotente, un état qu'on peut qualifier de juvénile. Les cellules souches pluripotentes sont capables de se différencier en plusieurs types cellulaires distincts.
Mais le principe choisi par les scientifiques de l'université d'Harvard n'est pas de rajeunir les cellules en jouant sur leur identité, ou leur différenciation, mais bien en modifiant leurs marqueurs épigénétiques, et plus spécifiquement les groupements méthyl.
La première expérience concerne l'effet du trio de « gènes reprogrammants » sur la régénération des neurones. Pour cela, les scientifiques se sont intéressés aux cellules ganglionnaires rétiniennes, qui font partie du nerfnerf optique situé derrière l'œilœil. Avec des forceps, ils ont endommagé le nerf optique chez des souris adultes, puis injecté les gènes OSK (les trois gènes dans un même virusvirus adénoassocié). Ce traitement a permis de limiter la mort cellulaire des neurones endommagés, mais aussi de stimuler la croissance de nouveaux.
Sous forme embryonnaire et après leur naissance, les neurones sont capables de se régénérer chez les souris, mais cette capacité disparaît avec le temps. Ici, l'injection des gènes OSK a donc eu un effet « anti-âge », en restaurant une capacité des neurones uniquement présente chez les animaux jeunes.
Mais ce n'est pas tout. Quatre jours après la blessure aux forceps, le processus de méthylationméthylation s'est accéléré dans les cellules ganglionnaires rétiniennes. Les motifs de méthylation correspondent alors à ceux d'une cellule en fin de vie. Par leur activité, les gènes OSK les ont tout simplement inversés sur tout l'ADNADN, mais plus particulièrement autour des gènes impliqués dans la détection de la lumièrelumière et la transmission synaptique. Les neurones ont retrouvé une seconde jeunesse.
Des souris qui recouvrent la vue
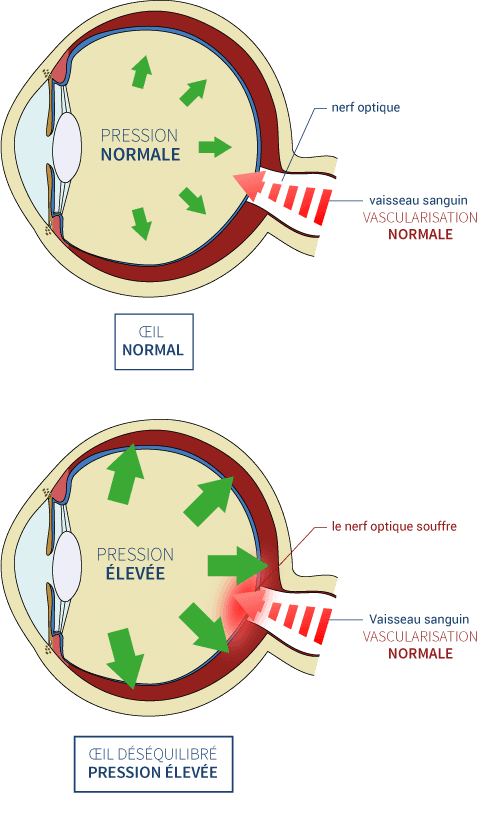
L'expérience suivante a pour sujet une maladie oculaireoculaire qui apparaît avec l'âge : le glaucome. Le glaucome est associé à l'augmentation progressive de la pressionpression intra-oculaire qui endommage le nerf optique et conduit à une perte de la vision progressive. Pour mimer cette maladie chez les souris, les scientifiques ont augmenté artificiellement la pression oculaire en injectant des billes dans la chambre antérieure de l'œil. Après 21 jours, les gènes OSK ont été injectés. L'œil traité présente alors une densité d'axonesaxones fonctionnels plus importante que l'œil malade non traité. Les souris ont aussi passé un test de vue, celles traitées ont recouvré la vue, pas en totalité, mais à hauteur de 50 % de ce qu'elles avaient perdu.
Dans une ultime expérience, les scientifiques ont injecté les gènes reprogrammants dans les yeux de souris âgées d'un an environ. À cet âge, leur vision a déjà diminué par rapport à celle des plus jeunes. Elle est environ 15 % plus faible que chez les souris âgées de cinq mois. Après quatre semaines de traitement, les vieilles souris voient aussi bien que les plus jeunes. Leur modification épigénétique présente alors le même profil.
Le saviez-vous ?
L’épigénétique s’intéresse à la modulation de l’activité des gènes qui n’est pas induite par leur séquence. Les scientifiques étudient un ensemble de structures qui entourent les gènes et régulent leur expression ou non dans une cellule donnée. Les modifications épigénétiques sont de plusieurs sortes, l’ajout ou le retrait de groupement méthyl (CH3) étant le plus étudié. Ces modifications sont réversibles et induites par l’environnement.
Ces trois expériences montrent que les cellules répondent aux gènes OSK par le réajustement des modifications épigénétiques qu'elles portent, les faisant correspondre à celles observées chez des sujets plus jeunes. La réussite des injections est aussi dépendante de la présence et de l'activité des déméthylases (TET1 et TET2), les enzymesenzymes qui retirent les groupements méthyl de l'ADN. Chez les souris en ayant moins, les résultats se sont avérés moins impressionnants.
Vouloir à tout prix rajeunir nos cellules semble alors tentant pour échapper aux affres du temps et aux maladies qu'il cause. Mais moduler ainsi les cellules n'est pas sans risque, le rajeunissement cellulaire peut conduire à l'apparition de cancercancer. Tous les mécanismes en jeu ne sont pas encore compris et les expériences doivent être répliquées avant de considérer cette approche comme un traitement possible contre les effets de l'âge, notamment dans les maladies dégénératives des yeux.