au sommaire
Après les laboratoires-sur-puce, capables d'analyser un gazgaz ou un liquideliquide sur la surface d'un circuit électronique, voici le microscope-sur-puce. Une équipe regroupant des chercheurs de l'Ecole Polytechnique Fédérale de Lausanne et du CalTech (California Institute of Technology)) y travaille depuis plusieurs années et vient de présenter une description complète de l'engin ainsi que deux séries d'observations obtenues avec deux modèles de microscopes dits optofluidiques...
Pour miniaturiser un microscope, commençons par supprimer les lentilleslentilles, trop encombrantes. La seule possibilité d'obtenir une image à haute résolution est alors de poser directement l'échantillon sur la surface sensible et d'éclairer par dessus. Si l'objet à observer est transparenttransparent et suffisamment fin, chaque élément sensible du capteurcapteur détectera la lumièrelumière ayant traversé l'échantillon verticalement et donnera un pixel.

Ce principe est celui de la microscopie en champ proche (Near field scanning optical microscope, NSOM), qui n'a pas été imaginé pour réduire la taille de l'instrument mais pour dépasser la limite de résolution théorique d'un microscope optiquemicroscope optique, correspondant à la longueur d'ondelongueur d'onde de la lumière utilisée. En plaçant au-dessus de chaque élément photosensible du capteur un trou d'un diamètre plus petit que cette longueur d'onde, on peut en principe obtenir une meilleure résolution.
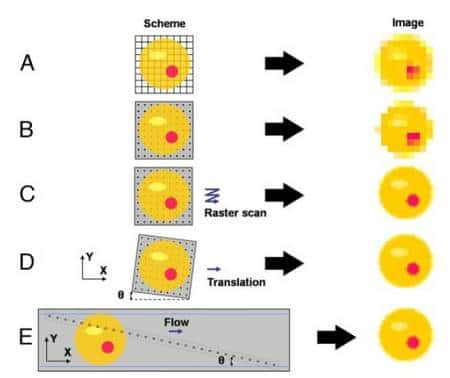
En 2006, l'équipe américano-suisse a réalisé le prototype d'un NSOM ajoutant une idée originale : déplacer l'échantillon au-dessus pour effectuer un balayage, en faisant appel aux techniques des circuits microfluidiquesmicrofluidiques, utilisés pour réaliser les laboratoires-sur-puce. Le principe est illustré dans le schéma de la figure 2. Il faut imaginer une dispositif miniature, gravé comme un circuit électronique. Le capteur (CMos) constitue la base de la structure et il est surmonté d'une surface conductrice percée de trous d'un diamètre très petit (un micronmicron) et alignés. Par gravuregravure toujours, un canal est creusé dans la couche se trouvant au-dessus, et constituée d'un polymèrepolymère, le PDMS (polydiméthylsiloxane). Le tout est fermé par une couche du même matériaumatériau. Transparente, la structure est éclairée par dessus.
La preuve par l'image
On obtient un tunnel dans lequel passe un fluide porteur coulant comme une rivière souterraine. Dans ce flot miniature, l'échantillon à observer est emporté et passe au-dessus des petits trous. L'astuce réside dans leur taille, plus petite que celle des éléments sensibles qui formeront chacun un pixel. En défilant devant le trou, l'objet réalise une sorte de scan à l'échelle de ce pixel. Les trous, faiblement espacés, sont alignés selon une diagonale qui traverse le chenal. Chaque élément envoie ses informations à un ordinateur dont le logiciel reconstitue l'image après le passage complet de l'échantillon.
Ce principe subtil (et un peu difficile à se représenter...) a été mis à l'épreuve et l'équipe vient de fournir toutes les explications dans la revue Pnas (Proceedings of the National Academy of Sciences). Les chercheurs y décrivent aussi un second modèle, dit électrocinétique, dans lequel le mouvementmouvement du fluide est imposé par un champ électriquechamp électrique.
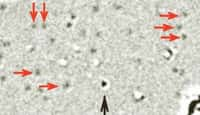
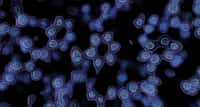
Le premier type de microscope convient bien aux objets longs et fins. Pour présenter les possibilités de l'instrument, les chercheurs ont observé un ver bien connu des laboratoires, Caenorhabditis elegansCaenorhabditis elegans (un nématodenématode vivant dans le sol et long d'environ un millimètre), qui sert de modèle en génétiquegénétique depuis une trentaine d'années. Le second modèle est plus adapté aux formes rondes, le champ électrique produisant un mouvement de rotation. Les chercheur lui ont soumis des cellules de microalgues planctoniques (Chlamydomonas), du pollenpollen de mûre et des billes de polystyrènepolystyrène.
Ces test démontrent une résolution d'environ 0,9 micron pour le premier modèle et de 0,8 pour l'instrument électrocinétique. Elle est faible comparée à celle d'un microscope électronique, dont les meilleurs descendent au demi angström, mais excellente pour un microscope optique. Selon ses inventeurs, cet engin simple, miniature et peu coûteux a un grand avenir en biologie mais aussi en médecine, par exemple pour détecter plus rapidement des infections parasitaires comme la malariamalaria. De plus, le principe se prête à d'autres utilisations, comme la spectrométriespectrométrie.