au sommaire
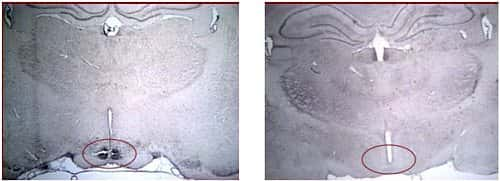
Ces microphotographies montrent une coupe de l'hypothalamus de rats soumis à un régime riche en protéines (à gauche) et de rats témoins (à droite). Les taches sombres révèlent la présence de facteurs impliqués dans la mise en place de la sensation de sati
Des travaux issus d'une collaboration entre le CNRS, l'Inserm, l'INRA et l'Université Claude BernardClaude Bernard - Lyon 1, expliquent son origine : l'ingestion de protéines stimule la synthèse de glucose par l'intestin et génère ainsi un signal de satiété pour le cerveau. Ces résultats, publiés dans le numéro de novembre de Cell Metabolism, permettent d'envisager de futures approches thérapeutiques de l'obésité.
Suite à l'ingestion d'un repas, déterminé par la sensation de faim, de nombreux mécanismes prennent place pour induire progressivement la sensation de satiété. L'un de ces mécanismes serait dépendant de l'absorptionabsorption du glucose apporté par les aliments. Le glucose lorsqu'il est libéré dans la veine porteporte peut en effet être détecté par des cellules spécialisées présentes dans la paroi de la veine, lesquelles sont connectées au système nerveux périphérique. Ce dernier transmet le message "glucose" au cerveau, ce qui se traduit par une activation de la région cérébrale impliquée dans le contrôle des sensations de faim et de satiété : l'hypothalamushypothalamus. La sensation de faim est ainsi progressivement diminuée.
L'équipe de Gilles Mithieux (CNRS), de l'Unité Mécanismes Moléculaires du DiabèteDiabète (Inserm - INRA - Université Claude Bernard - Lyon 1), avait décrit lors de travaux précédents une nouvelle fonction de l'intestin : sa capacité à synthétiser du glucose de novo et à le libérer dans le sang de la veine porte en dehors des périodes de repas. On pensait jusqu'alors que cette fonction appelée néoglucogenèse était réservée au foiefoie et aux reinsreins. La néoglucogenèse est normalement sollicitée pour synthétiser du glucose en cas de déficit alimentairedéficit alimentaire (jeûne plus ou moins prolongé) et maintenir la glycémieglycémie à un niveau suffisant.
Les chercheurs ont voulu savoir si la néoglucogenèse intestinale pouvait jouer un rôle dans les sensations de faim et de satiété prenant place après l'assimilation des aliments. Ils ont réalisé une série de tests chez des rats soumis à différents régimes alimentaires. Ils montrent que les gènesgènes nécessaires à la néoglucogenèse dans l'intestin sont fortement induits chez les rats nourris avec un régime riche en protéines. La synthèse de novo de glucose et sa libération dans la veine porte persistent ainsi après la phase d'assimilation du glucose alimentaire. Le message "glucose" transmis au cerveau persiste lui aussi, tout comme la sensation de satiété qu'il déclenche. Il en résulte une diminution de la prise alimentaire de ces rats, qui grossissent moins.
Ces travaux fournissent l'explication mécanique de l'effet "coupe-faimcoupe-faim" des protéines chez l'homme, un phénomène connu depuis longtemps et utilisé dans le traitement de l'obésité, mais qui restait à ce jour inexpliqué. Ils pourraient trouver d'autres applicationsapplications dans l'élaboration de futures approches thérapeutiques de l'obésité.