Le travail conjoint de deux équipes de chercheurs a démontré qu'il était possible de créer des structures embryonnaires humaines au début de leur développement en utilisant des cellules en culture. Une prouesse totalement inédite jusqu'alors !
au sommaire
La fécondation de l'ovule par le spermatozoïde marque le début de l'embryogenèse humaine, l'ensemble du processus de développement qui transforme le zygote en fœtus. Les quinze premiers jours de développement de l'embryonembryon, avant qu'il ne s'implante dans l'endomètreendomètre de l'utérusutérus, restent difficiles à étudier pour les scientifiques, car les embryons humains précoces disponibles pour la recherche sont assez rares.
Deux équipes, l'une affiliée à l'École de médecine du Sud-ouest de l'Université du Texas menée par Jun Wu, un spécialiste de l'embryogenèse, et l'autre affiliée à l'université Monash en Australie, sont parvenues à créer des embryons humains au stade blastocysteblastocyste à partir de cellules cultivées en laboratoire. Une technique déjà réalisée pour des embryons de souris, mais totalement inédite avec des cellules humaines.
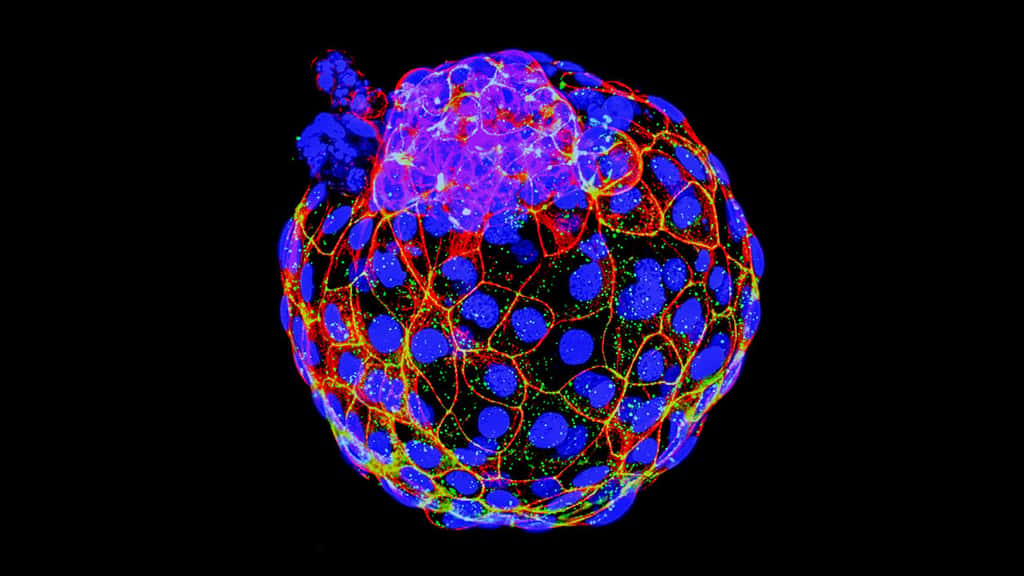
Un embryon humain de cinq jours créé in vitro
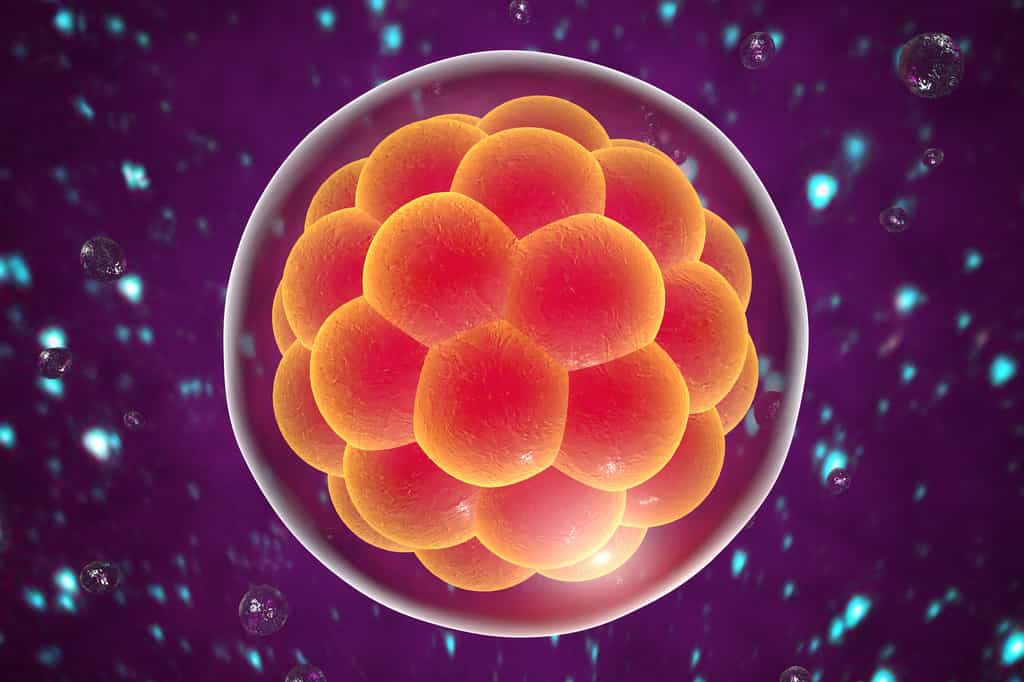
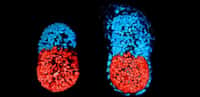
Juste après la fécondationfécondation, le zygote se transforme au fil des divisions cellulaires. Il contient d'abord deux cellules, puis quatre, puis huit et ainsi de suite. Au quatrième jour, il atteint le stade de blastocyte. Les cellules, qui étaient toutes identiques jusqu'alors, se scindent en deux populations selon leur position : les cellules à l'extérieur deviennent des trophoblastestrophoblastes et celles à l'intérieur, les cellules de la massemasse interne. Les heures suivantes sont cruciales pour ces dernières qui se séparent encore en deux populations distinctes : les cellules de la masse interne deviennent soit épiblaste et soit hypoblaste (ou endodermeendoderme primitif). Ces trois types cellulaires s'organisent autour d'une cavité, le blastocèleblastocèle. À ce stade, le blastocyte s'implante dans l'utérus pour poursuivre son développement.
Les deux équipes de chercheurs sont parvenues à recréer des blastocystes humains à partir de cellules en culture. Dans son laboratoire, l'équipe texane a utilisé des cellules souches pluripotentescellules souches pluripotentes. La deuxième équipe est partie d'une autre base, des fibroblastesfibroblastes adultes reprogrammés et dédifférenciés. La suite du protocoleprotocole est similaire pour les deux groupes, les cellules sont cultivées dans une boîte spéciale, où elles se développent dans les trois dimensions pour former des organoïdes, dans un milieu nutritif qui contient tous les éléments chimiqueséléments chimiques indispensables à la formation des blastocystes. Après une semaine de culture environ, les deux équipes ont obtenu des bastoïdes, contraction des mots « blastocyste » et « organoïde », humains de taille, forme et organisation (les trois populations cellulaires et la cavité) comparables aux blastocystes humains naturels.
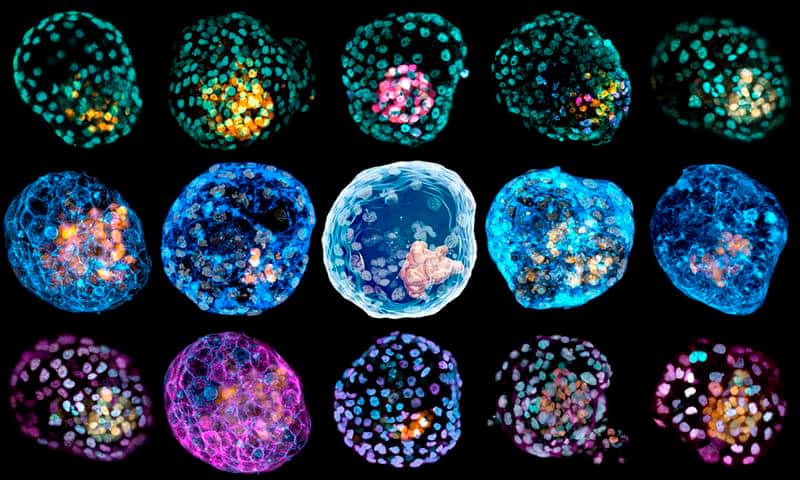
Un modèle d'étude prometteur
Les expériences ne s'arrêtent pas ici. Les scientifiques ont voulu analyser plus en avant le développement de leurs blastoïdes en mimant l'implantation dans l'utérus in vitroin vitro. Après quatre ou cinq jours de culture, plusieurs blastoïdes adhèrent à la boîte de culture et certaines populations cellulaires poursuivent leur différenciation. Les trophoblastes commencent à se spécialiser en cellules placentaires et les cellules de l'épiblaste se réorganisent autour de la cavité.
Ces blastoïdes, très semblables aux blastocystes naturels, semblent donc être des modèles in vitro prometteurs pour étudier les premiers stades du développement embryonnaire et les maladies qui y sont associées, mais ils restent pour le moment imparfaits. L'obtention de ces blastoïdes est laborieuse et difficilement reproductible. De plus, les trois populations cellulaires ne se développent pas de façon synchronisée au sein d'un même blastoïde, et les blastoïdes d'une même expérience n'évoluent pas au même rythme. Enfin, les scientifiques ont identifié des populations cellulaires présentes dans les organoïdes qui n'existent pas dans les blastocystes naturels.
L'étude du développement des blastoïdes n'ira pas plus loin car l'éthique interdit toute culture d'embryons humains au-delà de 14 jours de développement. À ce stade, les premiers tissus qui forment le fœtus apparaissent après la gastrulationgastrulation. Ces blastoïdes humains sont les premiers modèles embryonnaires humains, obtenus à partir d'une culture cellulaire, à présenter une organisation et un développement comparable aux blastocystes naturels.