Les chercheurs du monde entier planchent sur un traitement contre le coronavirus, que ce soit une molécule chimique ou un vaccin. Aux États-Unis, le premier essai clinique d'un vaccin préventif contre le coronavirus sur l'Homme vient de débuter.
au sommaire
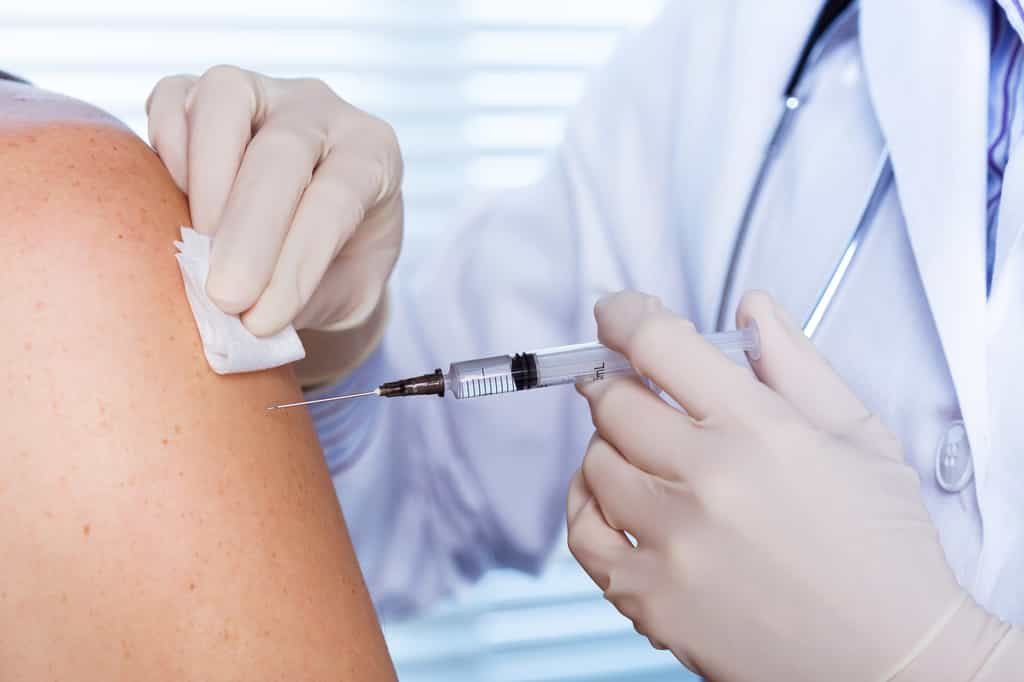
Le 16 mars 2020mars 2020, la première dose d'un vaccin expérimental pour lutter contre le coronavirus a été injectée à un volontaire à Seattle. Développé en un temps record par le National Institute of Allergy and Infectious Diseases (Niaid) en collaboration avec une entreprise de biotechnologiebiotechnologie, Moderna Inc, il s'agit du premier vaccin à entrer en étude cliniqueétude clinique de phase 1.
À l'heure où ces lignes sont rédigées, 183.304 personnes sont infectées par le coronavirus à travers le monde. En France, le nombre de cas atteint 6.633 pour 148 morts. Les mesures de confinement se multiplient pour tenter de juguler l'épidémie.
« Développer un vaccin sûr et efficace pour prévenir les infections du Sars-CoV-2 est une priorité de santé publique, affirme le directeur du Niaid, Anthony S. Fauci, dans un communiqué de presse. Cette étude de phase I, débuté en un temps record, est un premier pas important pour atteindre ce but »
45 volontaires ont reçu une injection du vaccin test
L'étude clinique de phase I est le premier stade où le vaccin est testé sur l’Homme après les études précliniques conduites sur les animaux. Compte tenu de l'urgence sanitaire et pour gagner du temps, il n'y a pas eu d'études précliniques pour ce vaccin.
Lors de la phase I, le but est d'étudier la toxicité de différentes doses vaccinales et de comprendre la réaction immunitaire associée sur des volontaires en bonne santé. Ici, le groupe est composé de 45 adultes âgés de 18 à 55 ans et durera six semaines.
Les volontaires ont reçu la première dose de vaccin par voie intramusculaire le 16 mars. Une seconde injection est prévue 28 jours plus tard. Trois dosagesdosages ont été testés : 25, 100 et 250 microgrammes.
Les participants à l'étude clinique seront suivis sur plusieurs aspects. Tout d'abord, les possibles effets secondaires provoqués par la vaccinationvaccination, comme des douleursdouleurs ou une poussée de fièvrefièvre. Puis, des prises de sang seront faites à intervalle régulier pour qualifier et quantifier la réponse immunitaire induite par le vaccin. Après la deuxième injection, les volontaires seront suivis sur une période d'un an.
Un vaccin qui bloque l’entrée du coronavirus dans la cellule
Le vaccin expérimental est composé de petits ARN messagersARN messagers, appelés mRNA-1273. Ils ont été construits en laboratoire grâce aux séquences génomiquesgénomiques du coronavirus SARS-CoV-2. La protéineprotéine obtenue après leur traduction aura une structure semblable à celle de la protéine S (ou spicule) qui permet au virusvirus d'entrer dans la cellule. Le vaccin ne contient donc pas de virus, comme cela peut-être le cas avec d'autres formulations vaccinales.
Les scientifiques espèrent que les spicules virales ainsi exprimées par les cellules stimuleront suffisamment la réponse immunitaireréponse immunitaire pour créer un pool d'anticorpsanticorps anti-spicules qui empêcheront le coronavirus d'infecter les cellules.
Ce n'est que la première phase sur les trois nécessaires pour obtenir une Autorisation de Mise sur le MarchéAutorisation de Mise sur le Marché (AMM). Les phases II et III sont plus longues, plus onéreuses et requièrent plus de personnes. Le vaccin final ne sera pas disponible avant un an ou plus.