au sommaire
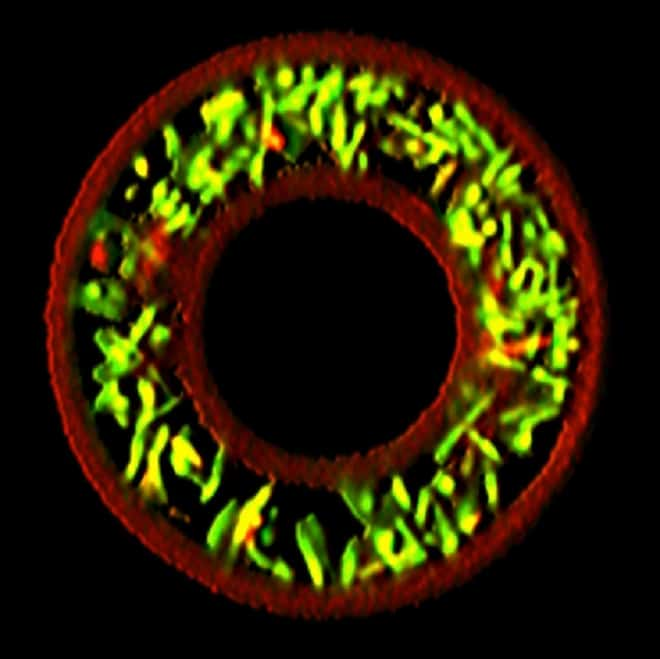
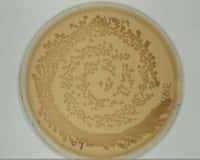
On peut apercevoir des bactéries (en vert) emprisonnées dans une cage en forme de donut (en rouge). Cette expérience, loin d’être farfelue, devrait permettre de mieux comprendre comment les communautés microbiennes communiquent au sein des environnements et développent des infections. © Jodi Connell, université du Texas à Austin
Les microbes sont partout : dans l'airair que nous respirons, sur les surfaces que nous touchons et dans la nourriture que nous mangeons. On ne peut tout simplement pas leur échapper ! Dans la très grande majorité des cas, ces micro-organismes n'évoluent pas seuls, mais font partie de communautés complexes, appelées biofilms, composées de virus, bactéries et protozoaires en tout genre qui s'échangent des signaux et établissent divers types de relations.
Depuis la constructionconstruction du premier microscope, l'infiniment petit est de plus en plus à la portée des scientifiques. Ils ont cependant encore beaucoup de travail pour comprendre comment les populations microbiennes interagissent, au sein de l'appareil digestif par exemple, où des milliards de bactéries ont élu domicile. Pour se faciliter la tâche, les chercheurs tentent de mettre au point des technologies innovantes. Ainsi, la flow cell est un petit dispositif qui permet d'observer en temps réel la formation de biofilms sur une surface, au moyen d'un microscope à fluorescence.

Dans cette animation, on peut observer en accéléré des bactéries qui se multiplient dans une cage microscopique. En fonction de sa taille, les chercheurs peuvent connaître assez précisément le nombre de cellules présentes à la fin de l'expérience. Il est ensuite possible de récupérer ces bactéries et d’étudier l'expression des gènes dans différentes conditions. © Connell et al, Pnas
Une équipe de l'université du Texas à Austin est allée encore plus loin. Elle vient de construire une « prison à bactéries », c'est-à-dire une cage microscopique qui empêche les microbes de s'échapper. Les plans de cette architecture originale sont présentés dans la revue Pnas.
Des bactéries emprisonnées mais capables de communiquer
Pour réaliser cette prouesse, les auteurs utilisent une solution de gélatine qui possède une caractéristique particulière : elle contient des moléculesmolécules photosensibles qui permettent à la gélatine de durcir lorsqu'elle est frappée par un laserlaser. Les bactéries sont introduites dans ce mélange et sont claquemurées grâce à un rayon laser appliqué à des endroits très précis. Le cachot microscopique peut ainsi prendre toutes sortes de tailles et de formes, allant du rond au triangle, en passant par le donut (l'équipe n'est pas américaine pour rien).
Mais à quoi cela peut-il bien servir ? Car, au-delà de la performance, ces travaux ont une réelle utilité. Selon les chercheurs, cette technique innovante permettrait de mieux contrôler les conditions d'une expérience et de répondre à des problématiques microbiologiques jusqu'ici inexplorées. Il est par exemple possible d'arrêter la croissance des bactéries à n'importe quel moment et de mesurer leur expression génétique.
Un outil pour comprendre la dynamique des populations microbiennes
Les auteurs peuvent alors étudier précisément comment plusieurs populations bactériennes de tailles variables communiquent les unes avec les autres. En effet, les mursmurs de ces structures empêchent les bactéries de s'évader, mais sont assez poreux pour laisser passer des substances nutritives ou des molécules signal. « Les microbes sont pris au piège, mais ils continuent à fonctionner comme dans les environnements biologiques », explique Jason Shear, le directeur de ces travaux.
Au cours de cette étude, les scientifiques ont créé deux cages, une contenant Staphylococcus aureusStaphylococcus aureus (staphylocoque doré)) et l'autre PseudomonasPseudomonas aeruginosa (bacillebacille pyocyanique), deux bactéries pathogènespathogènes pour l'Homme. Ils ont montré que la proximité de ces deux communautés augmentait la résistancerésistance du staphylocoque aux antibiotiques. En d'autres termes, les Pseudomonas envoient des signaux à leurs voisins et les rendent plus résistants.
En utilisant cette méthode, les chercheurs espèrent mieux comprendre comment les infections se mettent en place. « Nous savons que les infections nosocomiales sont transmises par l'intermédiaire de petites communautés microbiennes, poursuit Jason Shear. Avec ces prisons à bactéries, on pourrait répondre à diverses questions : combien de cellules sont nécessaires pour provoquer une infection ? Comment deviennent-elles virulentes ? Etc. » Les possibilités sont infinies et devraient permettre d'élucider certains mystères du monde de l'infiniment petit.