au sommaire
L'Agence européenne du médicament (EMA)) vient de publier un avis positif concernant le médicament Diane 35. Elle estime que sa balance bénéfices-risques est favorable dans le traitement de l'acné hormonal. Fin février, les autorités sanitaires françaises ont décidé que cet antiacnéique, largement prescrit hors AMM (autorisation de mise sur le marchéautorisation de mise sur le marché) comme contraceptif, devait être suspendu. Une décision qui vient d'ailleurs d'entrer en vigueur, ce 21 mai. Depuis l'annonce de l'autorité de santé européenne, l'Agence nationale de sécurité du médicament et des produits de santé (ANSM) n'a pas encore réagi.
« La balance bénéfices-risques de Diane 35 et de ses génériques est favorable dans la mesure où elle est prescrite dans certains cas bien définis », a estimé l'EMA. « Ces médicaments devraient ainsi être exclusivement proposés dans le traitement d'une acné modérée à sévère d'origine hormonale ou associée à un hirsutisme, chez des femmes en âge de procréer », précise l'agence.
De plus, ce type de moléculemolécule ne devrait jamais être prescrit en première intention, mais uniquement en cas de résistancerésistance aux autres traitements disponibles contre l'acné. Ces mesures doivent permettre de réduire les risques de thrombose embolique veineuse et artérielle associés à la prise de ces médicaments. À noter que ces indications ne sont pas nouvelles, puisque l'AMM de Diane 35 et de ses génériques concernait uniquement le traitement de l'acné en France.
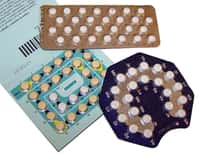
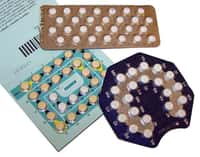
L'évaluation de Diane 35 et de ses génériques (comme Evépar) par l'EMA révèle que ces médicaments sont utiles dans le traitement de certaines formes d'acné, ce qui leur a valu une AMM. © Destination Santé.
Diane 35 : un risque faible mais bien connu
Les décès de quatre femmes survenus dans l'Hexagone depuis 1987, et attribués à la prise de Diane 35, avaient incité l'ANSM à suspendre son utilisation, à la fin du mois de mars dernier. Très largement prescrit comme « pilule », ce médicament présente en effet les caractéristiques d'un contraceptif hormonal, sans pour autant être indiqué dans ce but. C'est pourquoi l'EMA rappelle que « les femmes concernées ne devraient pas prendre d'autre contraceptif hormonal en association ». Elles augmenteraient alors leur risque de thrombose embolique.
Toutefois, « ce risque est faible et bien connu. Des avertissements sont inclus dans la notice d'utilisation », ajoute l'agence européenne. Saisie par l'ANSM en janvier, l'EMA admet quand même qu'il faudrait davantage d'informations afin de réduire encore les risques - bien que faibles - associés à cette molécule.
C'est pourquoi l'EMA recommande :
- des contre-indications et avertissements supplémentaires destinés aux patients et aux professionnels de santé ;
- des efforts pour améliorer leurs connaissances en matièrematière de risque thromboembolique. Les symptômes devraient être mieux connus, afin de réduire le délai de diagnostic et de traitement ;
- enfin, une meilleure pharmacovigilance dans tous les États.