au sommaire
Pour se multiplier sans cesse, les cellules cancéreuses court-circuitent de nombreuses régulations de la prolifération cellulaire, ce qui les amène à proliférer de manière incontrôlée. Ces cellules ont plusieurs solutions pour éviter la sénescencesénescence.
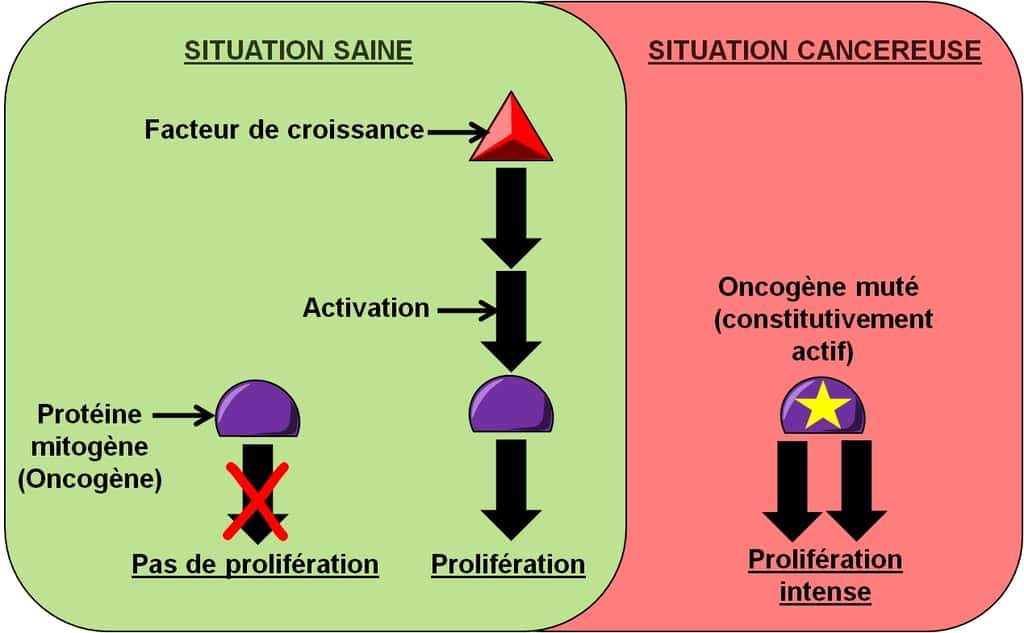
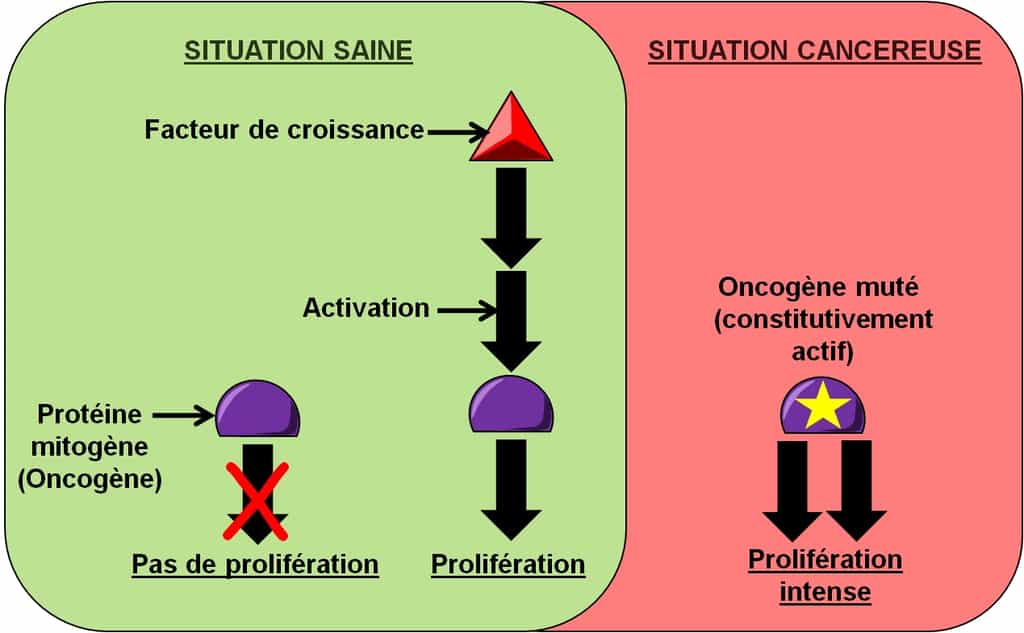
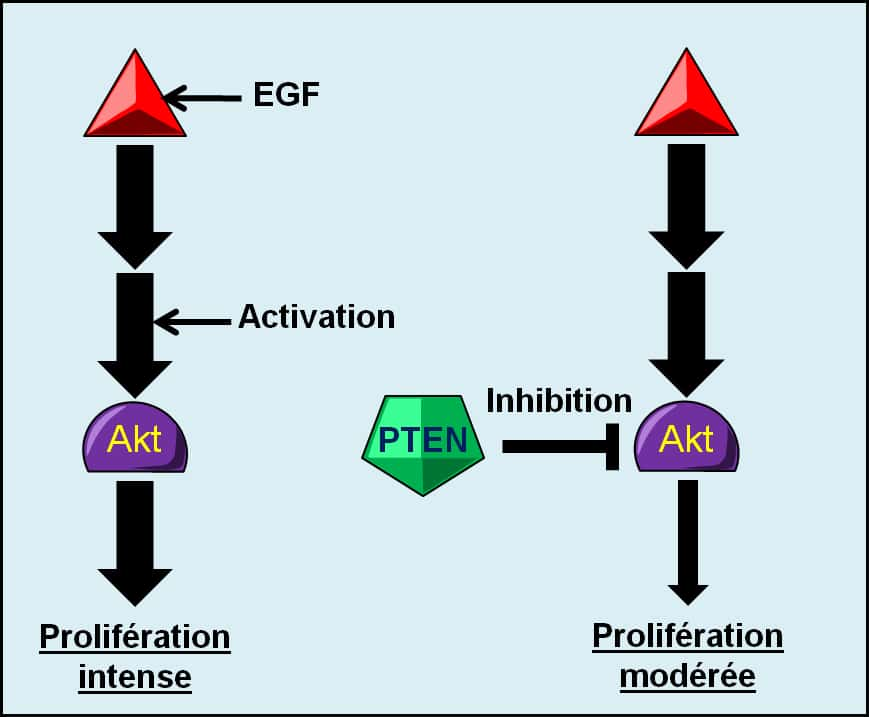
Figure 10. Dérégulation de la prolifération cellulaire. En situation saine, une cellule a besoin de facteurs de croissance pour proliférer. Dans une situation cancéreuse, la cellule cancéreuse peut muter un oncogène pour qu’il génère de façon permanente des signaux de prolifération, indépendamment de la présence de facteurs de croissance. © Grégory Ségala
La dérégulation de la prolifération cellulaire dans l’oncogenèse
Pour qu'une cellule prolifère, le point critique qu'elle doit passer dans le cycle cellulaire est le point de restriction gardé par la protéineprotéine Rb. Les signaux de prolifération doivent être soutenus pour inactiver ce point de contrôle alors que le reste du cycle cellulaire progresse sans stimulationstimulation extérieure. Pour proliférer exagérément, les cellules cancéreuses suractivent donc les signaux de prolifération cellulaire pour passer le point de restriction le plus rapidement possible. Elles utilisent plusieurs stratégies pour sur-activer ces signaux.
De nombreuses protéines mitogènes, par exemple Akt, sont des oncogènesoncogènes (Figure 10). Les cellules cancéreuses possèdent des mutations qui rendent ces oncogènes constitutivement actifs. Cela veut dire que ces protéines transmettent en permanence un signal de prolifération à la cellule indépendamment de la stimulation par un facteur de croissancefacteur de croissance normalement prérequise. Les cellules cancéreuses peuvent aussi surproduire elles-mêmes le facteur de croissance qui active son propre récepteur à la surface des cellules cancéreuses : c'est une stimulation autocrine de la prolifération cellulaire.
À cause de signaux de prolifération permanents et intenses, la protéine Rb est maintenue inactive et le cycle cellulaire peut être initié à volonté. Les cellules cancéreuses bénéficient d'une prolifération autonome puisqu'elles ne dépendent plus des autres cellules pour obtenir l'autorisation de proliférer : la prolifération est incontrôlée.
La protéine Rb est un suppresseur de tumeurssuppresseur de tumeurs très important puisque c'est la dernière barrière que rencontrent les cellules cancéreuses pour pouvoir proliférer. Chez de nombreuses cellules cancéreuses, on retrouve des mutations inactivatrices du gènegène Rb qui empêchent la protéine Rb de garder le point de restriction. Cette invalidation du point de restriction confère aux cellules cancéreuses la capacité de proliférer librement.
La sénescence : un obstacle érigé contre la prolifération incontrôlée
Dans les cellules, la suractivation des signaux de prolifération active la sénescence. La sénescence est un mécanisme naturel de défense contre les cellules qui bénéficient d'une stimulation de la prolifération anormalement élevée. La sénescence verrouille définitivement le point de restriction qui ne peut plus être inactivé par les signaux de prolifération. La cellule sénescente ne peut définitivement plus proliférer.
Pour éviter la sénescence, les cellules cancéreuses peuvent avoir recours à plusieurs solutions : générer des signaux de prolifération justement dosés pour inactiver le point de restriction mais ne pas activer la sénescence, ou bénéficier de mutations inactivant les gènes de la sénescence. Les gènes suppresseurs de tumeurs p16 et p53p53 déclenchent la sénescence lorsque la prolifération cellulaire est trop intense. Le gène p53 est inactivé dans la plupart des cancerscancers et l'inactivation de p16 est retrouvée dans de nombreux mélanomes.