au sommaire
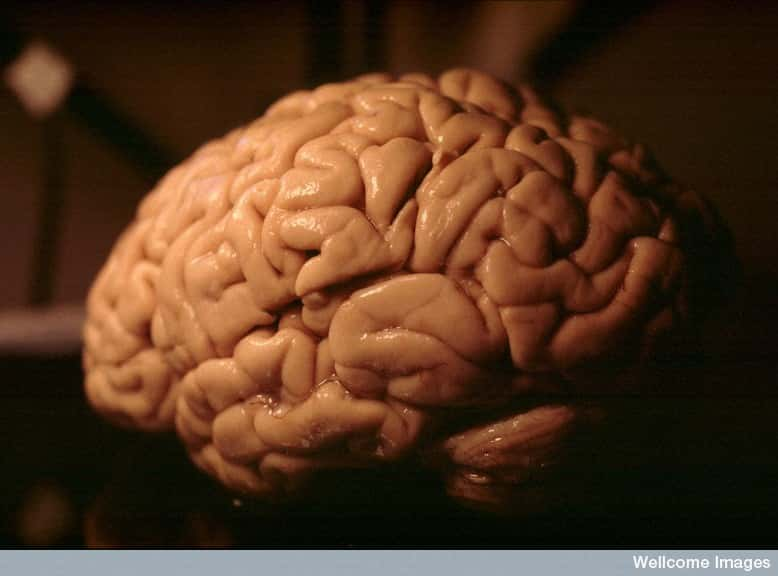
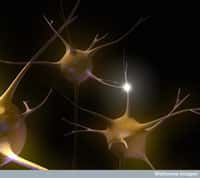
La maladie d'Alzheimer se caractérise par une perte neuronale forte dans des régions du cerveau liées à la mémoire et à l'apprentissage, entraînant progressivement de grandes difficultés dans le quotidien. Les causes pourraient être épigénétiques. © Heidi Cartwright, Wellcome Images, Flickr, cc by nc nd 2.0
Principale neurodégénérescence dans le monde, la maladie d’Alzheimer reste encore bien incomprise. Face à cette méconnaissance, la difficulté d'agir pour enrayer la perte neuronale accélérée. Si les chemins actuellement suivis n'ont pas encore abouti à des traitements efficaces, des scientifiques choisissent de sortir des sentiers battus pour se focaliser sur de nouveaux aspects. Si les gènes en lien avec la démence ont été étudiés, les aspects épigénétiques le sont beaucoup moins.
Qu'est-ce donc ? Toutes les cellules possèdent la même moléculemolécule d'ADN, mais pour se spécialiser, ce long code-barre n'est pas interprété de manière identique. Des modifications moléculaires, comme l'ajout de groupements chimiques (principalement des méthyles), viennent modifier la façon dont les gènes sont lus. L'environnement constitue l'un des acteurs pouvant altérer les profils épigénétiques.
Des chercheurs néerlandais de l'université de Maastricht, sous l'égide de Däniel Van den Hove, ont annoncé avoir avancé dans ce sens lors du 26e congrès du Collège européen de neuropsychopharmacologie (ECNP)), qui se tient du 5 au 9 octobre à Barcelone. Ils posent les jalons pour de nouvelles études qui pourraient déboucher sur de nouveaux traitements et diagnostics de la maladie d'Alzheimer.
Des changements épigénétiques liés à l’âge
Leur recherche a été menée en parallèle chez les souris et l'Homme, en comparant les profils épigénétiques de l'hippocampe (région du cerveau impliquée dans la mémoire et l'apprentissage, très vite touchée par la démence) liés au vieillissement et à la maladie neurodégénérative.

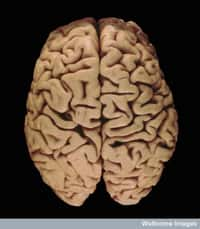
La maladie d'Alzheimer frappe principalement les personnes âgées. Alors, de nombreuses études tentent de comparer les mécanismes du vieillissement naturel lié à l'âge et de le comparer à la maladie neurodégénérative. D'un point de vue épigénétique, les deux aspects sont différents. © Jean-Marie Huet, Flickr, cc by nc sa 2.0
Avec l'âge, les rongeursrongeurs présentent une augmentation de la concentration en une enzymeenzyme : l'ADNADN méthyltransférase 3a, qui ajoute des groupements méthyles sur l'ADN et que l'on associe à la prolifération et la différenciation cellulaire. Les auteurs ont également remarqué une hausse de 5-méthylcytosine (5-mC) et de 5-hydroxyméthylcytosine (5-hmC), deux molécules utilisées comme marqueurs de méthylation de l'ADN global. Autre observation associée au vieillissement : une augmentation de la concentration en une autre enzyme, l'histonehistone déacétylase 2 (HDAC2), impliquée dans la formation de la mémoire mais aussi dans les troubles cognitifs liés à la neurodégénérescence.
Fait intéressant : il semble que la restriction calorique prévienne ces changements épigénétiques, ce qui expliquerait pourquoi manger peu limite les risques et la progression de la maladie.
Vers une nouvelle façon de traiter la maladie d’Alzheimer
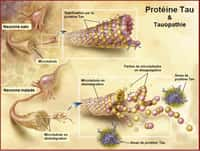
Les auteurs ont ensuite étudié des tissus cérébraux humains issus de patients décédés. Les profils de méthylationméthylation et d'hydroxyméthylation de l'ADN différaient entre les anciens Alzheimer et les individus témoins. Dans ce premier cas, les scientifiques ont constaté une forte chute de 5-mC et de 5-hmC. Et plus la baisse était importante, plus on retrouvait en fortes concentrations les plaques amyloïdes dans l'hippocampehippocampe, caractéristiques de la démence. Là encore, l'épigénome pourrait apporter les éléments expliquant les aberrationsaberrations constatées avec l'accumulation des bêta-amyloïdesbêta-amyloïdes.
Pour les souris atteintes d'une maladie semblable à Alzheimer, on observe un déséquilibre dans les balances de méthylation et d'hydroxyméthylation par rapport aux rongeurs témoins âgés. Une partie des explications de la démence pourraient donc se trouver à ce niveau-là.
Et comme les processus épigénétiques sont dynamiques et réversiblesréversibles, les chercheurs envisagent de trouver les éléments pour leur redonner un profil plus proche de l'état normal, ce qui pourrait conduire à un traitement efficace contre la maladie d'Alzheimer. Vu la corrélation entre les méthylations du cerveaucerveau et celles observées dans le sang, les auteurs envisagent déjà un possible diagnostic de la neuropathologie. Il faudra simplement déblayer cette piste avant de s'assurer que le chemin en vaut la peine.