au sommaire
Comment user des propriétés de la graisse à notre avantage ? Voilà une question qui interpelle les scientifiques depuis longtemps. Bien que cette couche nous soit utile pour stocker l'énergieénergie et nous préserver du froid, elle est devenue une ennemie féroce à combattre, alors que le monde est en proie à une épidémie de surpoids. Et des chercheurs de l'université Harvard, dirigés par Bruce Spiegelman, viennent d'entr'ouvrir une nouvelle piste à étudier, car le tissu adipeux posséderait une propriété jusque-là jamais estimée : il pourrait de lui-même brûler des calories lorsqu'il fait trop froid.
Depuis le début des années 1990, on sait que la graisse ne joue pas que le rôle d'un isolant thermique. En effet, lorsque les températures baissent, des nerfs sensoriels envoient des informations au cerveau. En réponse, celui-ci donne des ordres aux cellules adipeuses brunes par l'intermédiaire de la noradrénaline, un neurotransmetteur clé du système nerveux parasympathiquesystème nerveux parasympathique. Le processus incite alors cette la graisse brune à utiliser l'énergie pour en faire de la chaleurchaleur. Voilà comment faire partir nos calories en fumée. En revanche, cela ne se produit pas sur les cellules adipeuses blanches, celles qui s'accumulent sous la peau et qui donnent cette fameuse ceinture abdominale dont on veut souvent se débarrasser.
Les graisses blanche et beige tiennent chaud quand il fait froid…
Pour transformer l'énergie en chaleur, le tissu adipeux brun a recours à UCP1, une protéineprotéine activée par la liaison de la noradrénaline à des récepteurs bêtabêta-adrénergiquesadrénergiques présents sur les cellules. Cette protéine, considérée comme l'une des pistes contre l'obésité, serait aussi impliquée contre le diabètediabète. Elle revêt donc un intérêt certain pour les scientifiques. Bien que l'on connaisse bien la voie de signalisation, ils espèrent désormais trouver un moyen de l'activer.
Bruce Spiegelman et son équipe viennent de faire une découverte qui pourrait y aider. Dans les Pnas, ils relatent leurs expériences menées in vivoin vivo et in vitroin vitro, qui laisseraient entendre que le reste du tissu adipeux, insensible à la noradrénaline du système nerveux, pourrait malgré tout produire de la chaleur lorsque la température extérieure vient à chuter.
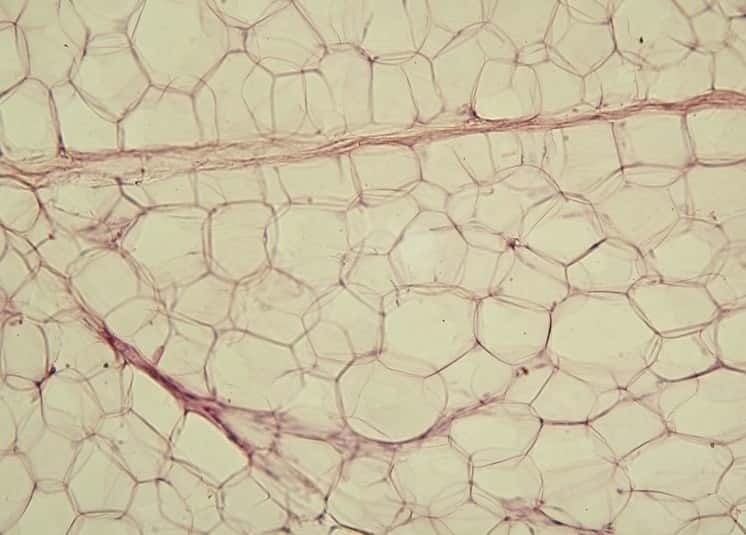
La graisse existe sous trois formes : les tissus adipeux blanc et brun, et le tissu adipeux beige, mélange des deux précédents. Tous ces tissus pourraient donc produire de l’énergie en dépensant de la chaleur lorsqu'à l'extérieur, il fait froid. © Jagiellonian University, Wikipédia, cc by sa 3.0
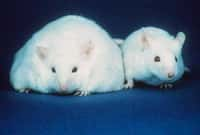
Dans une première expérience, ils ont exposé des souris pendant 20 heures à 10 °C. Les rongeursrongeurs choisis étaient déficients en récepteurs bêta-adrénergiques. Autrement dit, leur système nerveux périphérique ne pouvait activer les cellules de la graisse brune. Comme attendu, la production de chaleur était plus faible que chez les contrôles. En revanche, ils ont remarqué qu'au niveau des tissus adipeux blanctissus adipeux blanc et beige, retrouvé juste sous la peau, le gènegène de la protéine UCP1 était plus actif.
… En toute indépendance du système nerveux
Les chercheurs ont alors exposé in vitro les trois formes des cellules adipeuses à des températures variant entre 27 et 39 °C pendant 4 heures, 8 heures, ou jusqu'à 10 jours. Dans les environnements les plus frais (entre 27 et 33 °C), la graisse brune n'a manifesté aucun changement. En revanche, les graisses blanche et beige ont vu leur taux d'UCP1 multiplié par deux environ 8 heures après le début du traitement. Les niveaux retournaient à la normale lorsque les températures approchaient les 37 °C.
In vivo, les constats sont les mêmes. Les souris déficientes en récepteurs bêta-adrénergiques voient l'activité calorifique de leurs tissus adipeux blanc et beige augmenter lorsqu'elles sont placées dans un environnement froid. C'est donc la preuve qu'une partie du tissu graisseux a la propriété intrinsèque de produire de la chaleur lorsque le milieu extérieur est frais. Le cerveaucerveau n'explique pas tout.
Vers un traitement de l’obésité tout en gestion des dépenses
Bien que cette trouvaille ne débouche sur aucune applicationapplication concrète pour le moment, elle constitue un point de départpoint de départ pour envisager de nouvelles pistes dans l'espoir de déterminer un nouveau traitement contre l'obésité et le diabète. Reste à comprendre comment nous pourrions exploiter cette propriété pour faire fondre les kilos de graisse en excès.
De nombreuses questions demeurent. Par quels mécanismes ces cellules adipeuses deviennent-elles sensibles à la température ? Comment cela affecte-t-il l'expression des gènes ? L'idée que des cellules puissent changer l'activité de leur génomegénome en fonction de la température extérieure est assez nouvelle. Enfin, quelle serait la part d'un tel processus dans la dépense énergétique ? Les auteurs veulent désormais l'estimer et poursuivent leurs recherches dans cette direction.
À terme, on pourrait déboucher sur une gestion de l'obésitéobésité par la régulation des dépenses caloriques. S'il y a des excédents à éliminer, il suffirait d'inciter les cellules adipeuses à évacuer le trop-plein pour retomber à une situation d'équilibre. Un beau principe, qu'on ne verra pas en application de sitôt...