au sommaire
Nombre de recherches en exobiologie se tournent vers l'apparition des acides aminésacides aminés. Les molécules organiques ont pu arriver sur Terre par l'intermédiaire de météorites entrées en collision avec notre Planète bleue.

L'apparition des acides aminés est-elle liée aux météorites ? © Muratart, Shutterstock
Les météorites carbonées, représentées typiquement par les météorites d'Orgueil et de Murchison, renferment des composés organiques comme des hydrocarbures aliphatiques et aromatiquesaromatiques. Des hydrocarbures aromatiques polycycliques, des kérogèneskérogènes et des fullerènesfullerènes sont également présents.

Les premières molécules organiques sur Terre sont-elles arrivées par les météorites ? © DR
Des composés plus proches des composés biologiques ont été identifiés :
- acides carboxyliquesacides carboxyliques ;
- acides aminés ;
- bases nucléiquesbases nucléiques ;
- amines ;
- amides ;
- alcoolsalcools, etc.

Les molécules retrouvées dans la météorite de Murchison. © DR
La météorite carbonée de Murchison
La météorite carbonée de Murchison renferme plus de 70 acides aminés différents. Au nombre de ceux-ci, on trouve 8 acides aminés protéiques. Dans les molécules organiques, l'atomeatome de carbonecarbone occupe généralement le centre d'un tétraèdre. Lorsque les groupes d'atomes aux quatre sommets du tétraèdre sont différents, l'image du tétraèdre dans un miroirmiroir ne lui est pas superposable. Le carbone devient asymétriqueasymétrique.
Il existe alors deux formes spéculaires (Figure 1) non superposables, images l'une de l'autre dans un miroir, appelées énantiomèresénantiomères (du grec enantios, opposé). Les molécules biologiques n'utilisent qu'une des deux formes spéculaires. On dit qu'elles sont « homochirales » (du grec kheir, main).
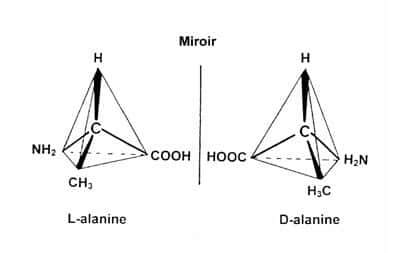
Figure 1. La plupart des acides aminés existent sous deux formes, images l’une de l’autre dans un miroir. Les protéines n’utilisent que la forme L (gauche). © DR
Géométrie des macromolécules biologiques
Une vie racémique qui utiliserait indifféremment et simultanément les deux énantiomères gauches et droits des molécules semble très improbable. Le premier argument est lié à la géométrie des macromoléculesmacromolécules biologiques. Par exemple, les protéinesprotéines adoptent des formes rigides dans l'espace, appelées conformationsconformations :
- hélices α ;
- feuillets β.
L'hélice α ressemble à un tire-bouchon. Elle renferme 3,6 acides aminés par tour et elle est stabilisée par des liaisons hydrogèneliaisons hydrogène qui s'établissent à l'intérieur d'une même chaîne. Les feuillets β sont formés par l'association côte à côte de plusieurs chaînes. Dans ce cas, les liaisons hydrogène s'établissent entre deux chaînes voisines. La présence simultanée des énantiomères L et D des acides aminés dans une même chaîne n'empêche pas la formation d'hélices α. Ces dernières sont simplement un peu moins stables. En revanche, les feuillets β ne peuvent plus se former lorsque les énantiomères L et D se côtoient dans la chaîne. Comme l'activité des enzymesenzymes est liée à leur géométrie spatiale, l'absence de feuillets β diminuerait considérablement leur champ d'action et une vie racémique serait nécessairement différente de celle que nous connaissons, nécessairement plus élémentaire, voire impossible.
D'autre part, l'utilisation de monomèresmonomères homochiraux réduit considérablement le nombre d'arrangements possibles des monomères dans une chaîne. Pour un polymèrepolymère renfermant n unités monomériques, le nombre de combinaisons possibles sera divisé par 2n si le système n'utilise qu'un seul énantiomère.
Quand on sait qu'une chaîne de protéine renferme quelques centaines d'acides aminés, on réalise l'énorme simplification apportée par l'usage de monomères homochiraux. La qualité première de la vie est de faire plus de soi-même par soi-même. En chimiechimie, cette qualité qualifie les molécules autocatalytiques : elles sont capables de catalyser leur propre formation et se retrouvent inchangées à la fin de la réaction. Le mode de copie doit être suffisamment fidèle pour ne pas dénaturer le message tout en laissant une petite possibilité de mutation permettant au système d'évoluer. Si le biopolymère à copier renferme des énantiomères L et D à des endroits bien précis, le procédé de copie devra non seulement positionner le monomère au bon endroit de la chaîne, mais également être capable, pour un monomère donné, de choisir entre deux énantiomères qui ne diffèrent que par la géométrie de leurs atomes de carbone. Dans l'état actuel des connaissances, une vie racémique qui utiliserait simultanément les deux énantiomères L et D des enzymes semble très improbable. En revanche, une vie utilisant exclusivement les acides aminés D est parfaitement envisageable.
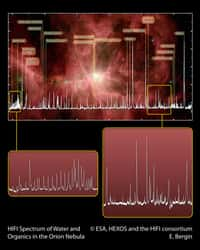
Deux vies énantiomères concurrentes se sont peut-être développées sur la Terre primitive, la vie que nous connaissons finissant par l'emporter. Cependant, il n'y a aucune signature fossilefossile connue de cette vie « dans un miroir ». Le minéralogiste américain John Cronin (Cronin et Pizzarello, 1997 ; Pizzarello et Cronin, 2000) trouva un excès d'environ 9 % d'énantiomères gauches pour certains acides aminés non protéiques présents dans cette météorite. La découverte par les astronomesastronomes d'un rayonnement infrarougeinfrarouge fortement polarisé dans un nuagenuage moléculaire de la nébuleuse d'Orionnébuleuse d'Orion pourrait expliquer l'origine extraterrestre de cet excès de formes gauches (Bailey et al., 1998).
Micrométéorites et grains interplanétaires sur Terre
Des collectes de poussières interplanétaires dans les glaces du Groenland et de l'AntarctiqueAntarctique par Michel Maurette (Maurette, 1998 ; Maurette et al., 2000 ; Maurette et al. 2001) permettent d'évaluer à environ 50 à 100 tonnes la quantité de grains interplanétaires arrivant tous les jours actuellement à la surface de la Terre.

Les micrométéorites ont apporté de la matière carbonée. © DR
Environ 99 % de cette massemasse est apporté par des micrométéorites dont le diamètre est compris entre 50 et 500 micronsmicrons. Les micrométéorites sont apparentées aux météorites les plus primitives, celles du groupe des météorites carbonées représentées par la météorite de Murchison.
Une analyse détaillée des teneurs en carbone de différents groupes de micrométéorites permet d'estimer à cent tonnes le flux total de carbone organique apporté tous les ans à la Terre. La quantité livrée à la Terre pendant les 200 millions d'années de la phase la plus active du bombardement terrestre, quand le flux micrométéoritique était vraisemblablement mille fois plus intense qu'aujourd'hui, est estimée à 4x1021g. Pour donner un ordre de grandeurordre de grandeur, le carbone biologique recyclé aujourd'hui à la surface de la Terre représente 1018g. Ces grains renferment une forte proportion de sulfuressulfures métalliques, d'oxydes, d'argilesargiles qui sont autant de catalyseurscatalyseurs. Au contact de l'eau liquideliquide, les grains ont donc pu fonctionner comme des microréacteurs chimiques transformant la matièrematière organique des grains à l'aide des catalyseurs présents.
L'analyse des poussières prelevées dans la comacoma de Wild-2 par la sonde américaine StardustStardust permet d'attribuer une l'origine cométaire aux microméteorites collectées en Antarctique. Les sondes Véga 1 et 2, GiottoGiotto, Suisei et Sakigake ont montré que la comète de Halleycomète de Halley est riche en matériaux organiques, le taux moyen en poids de carbone présent dans les grains cométaires étant estimé à 14%. Parmi les molécules identifiées, on retrouve l'acide cyanhydriqueacide cyanhydrique et le formaldéhydeformaldéhyde. Ces composés, ainsi que de nombreuses autres molécules d'intérêt prébiotiqueprébiotique, ont été observés dans les comètes Hyakutakecomètes Hyakutake en 1996 et Hale-BoppHale-Bopp en 1997. Les comètes se déplacent sur des orbitesorbites instables et succombent parfois au champ gravitationnel d'une planète. La collision de la comète Shoemaker-Levy 9Shoemaker-Levy 9 avec JupiterJupiter en juillet 1994 en est un exemple récent. Ce genre de collision était vraisemblablement plus fréquent il y a 4 milliards d'années, les planètes orbitant autour du SoleilSoleil étant plus nombreuses. En percutant la Terre, les comètes ont pu fournir une fraction importante de l'eau et les grains cométaires ont dû fournir de grandes quantités de molécules carbonées. La chimie qui se développe à la surface du noyau cométaire est encore mal connue. Lancée en 2004, la mission cométaire RosettaRosetta va procéder en 2014 à l'analyse du noyau de la comète Churyumov-Gerasimenko. La sonde spatiale étudiera d'abord l'environnement de la comète en restant dans son sillage pendant plusieurs mois puis une sonde s'y posera pour analyser la surface mais également la glace sous-jacente qui sera extraite par forage.
En savoir plus :