au sommaire

James Clerk Maxwell
Le démondémon de Maxwell est une expérience de pensée proposée par James Maxwell en 1867 pour violer le second principe de la thermodynamique.
Maxwell s'était intéressé à la théorie cinétique des gaz, où l'on réduisait les propriétés thermodynamiques de ceux-ci à la mécanique d'un très grand nombre de molécules. La chaleur y était alors ramenée à une forme particulière d'énergie, sous forme d'agitation désordonnée des molécules. Plus l'agitation étant importante plus la température du gaz étant élevée.
Seulement voilà, la science des transformation de l'énergie, et notamment des règles de transformation de la chaleur en travail utilisable, la thermodynamique, implique une direction à l'écoulement du temps et limite les transformations possibles de l'énergie et de la matièrematière. La chaleur ne passe pas spontanément d'un corps froid à un corps chaud, ne peut pas se transformer complètement en travail si la température est la même partout dans un système et un vase brisé ne se recolle pas spontanément ou une goutte d'encre dans un verre d'eau ne se rassemble pas toute seule après s'être diffusée.
Or, si l'on prend vraiment au sérieux la réduction de la thermodynamique à la mécanique, cela est plus que paradoxal. Les équationséquations du mouvementmouvement des particules dans un gaz, ou constituant tout autre corps matériel, ne font pas de différences entre un mouvement dans un sens du temps donné et un mouvement dans le sens inverse. Ce qui veut dire qu'il pourrait y avoir autant de chance de voir un vase se briser que de le voir se recoller spontanément, ou que la goutte d'encre diffusant dans un verre ne revienne à son état de concentration initiale. Le second principe ne serait donc vrai qu'en moyenne, approximativement et devrait donc pouvoir être violé même si cela resterait, en pratique, très difficile. Sauf évidemment pour un analogue du Démon de Laplace, c'est-à-dire le fameux démon de Maxwell !
Si l'on imagine une boite avec initialement les molécules d'un gaz réel rassemblées dans un coin, l'agitation thermique, et donc le second principe de la thermodynamique, va faire que ce gaz va se diffuser jusqu'à occuper uniformément tout le volumevolume de la boite. On rejoint une situation dite d'équilibre thermodynamique, où le gaz n'exhibe aucune tendance à se rassembler à nouveau dans un petit volume de la boite. Cela permet de définir un sens pour l'écoulement du temps.
Maintenant imaginons une paroi séparant la boite en deux parties, dont l'une B est plus importante que l'autre A. La partie A correspondant à la zone initiale où se trouvait le gaz avant de diffuser. Un petit trou est percé dans cette paroi avec une porteporte qu'un petit démon peut fermer ou ouvrir à volonté.
Le gaz étant initialement réparti de façon uniforme dans chacune des parties de la boite, dès qu'une molécule se dirige vers ce trou, de la partie B vers A, le démon laisse la porte ouverte. Inversement, si la molécule vient de A en direction de B, le démon ferme la porte.
On comprend bien qu'au bout d'un certain temps, le gaz sera à nouveau dans un coin de la boite et qu'on sera revenu à une situation de non-équilibre. On a donc violé le second principe de la thermodynamique !
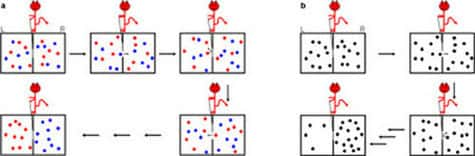
En a le démon de Maxwell sépare deux types de molécules initialement mélangées, en b il rassemble les molécules dans une partie de la boite
En fait non ! Répondront quelques années plus tard Léon Brillouin et Léo Szilard. Pour observer les molécules, le démon aura besoin de dépenser de l'énergie en les éclairant. Une analyse fine montre alors que le second principe, chassé par la porte, revient par la fenêtrefenêtre !