au sommaire
En chimie organique, un aldéhyde est une molécule dont la fonction caractéristique est un groupe carbonyle C=O situé obligatoirement au bout de la chaîne carbonée, c'est-à-dire que le carbone porteur de la fonction est lié par une double liaison à un oxygène et par une simple liaison à un hydrogène. Le groupe fonctionnel est donc au final de la forme CHO.
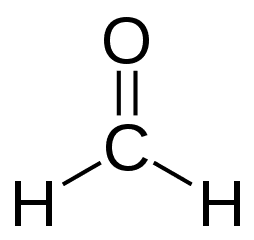
L’aldéhyde le plus simple est le méthanal de formule H-CHO. Dans tous les autres composés, le carbone porteur est relié à une chaîne carbonée. © Wereon, Wikimedia Commons
Le nom de l'aldéhyde dérive de l'hydrocarburehydrocarbure correspondant auquel on ajoute la terminaison -al. Ainsi, méthanal vient de méthane, éthanal d'éthane, etc. Le méthanal, aussi appelé formaldéhydeformaldéhyde ou aldéhyde formique est gazeux, mais tous les autres aldéhydes sont liquidesliquides ou solidessolides. Ces composés ont un intérêt dans l'industrie pour la fabrication de parfums, de médicaments, de plastiquesplastiques, de solvantssolvants, de papier ou encore de textiles.
Synthèse des aldéhydes
À l'échelle industrielle, l'oxydationoxydation ménagée des alcoolsalcools primaires permet de produire des aldéhydes, en prenant des précautions pour que la réaction s'arrête avant la formation d'acides carboxyliquesacides carboxyliques. C'est ainsi que le méthanal est fabriqué à partir de méthanol.
Les aldéhydes sont aussi produits massivement à partir d'alcènesalcènes par hydroformylation, une méthode souvent appelée procédé oxo : le butanal, par exemple, est synthétisé à partir de propène, de monoxyde de carbonemonoxyde de carbone et de dihydrogène, en présence d'un catalyseurcatalyseur.
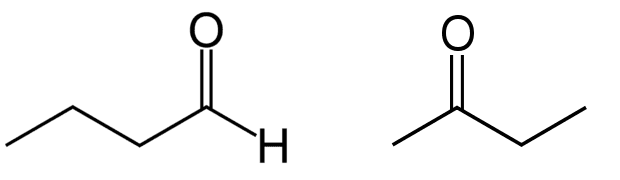
Le butanal (un aldéhyde) à gauche et la butanone (une cétone) à droite. Les aldéhydes ont des propriétés similaires aux cétones, avec lesquels ils ne doivent pas être confondus : les cétones possèdent un groupe carbonyle en milieu de chaîne. © Wikimedia Commons
Réactivité des aldéhydes
De par la forte polarisation de la liaison C=O, les aldéhydes, comme les cétonescétones, sont susceptibles de subir une addition nucléophilenucléophile sur le carbone porteur de la fonction. Cette propriété est utilisée pour protéger la fonction carbonyle par acétalisation, un procédé réversibleréversible consistant à additionner deux alcools sur le carbonyle pour former un composé inerte appelé acétal.
Au niveau industriel, les aldéhydes sont surtout utilisés pour synthétiser des plastifiants et des glycols par condensationcondensation, ou des alcools lors d'une réaction de réduction par le dihydrogène.