au sommaire
En chimie organique, un alcène est un hydrocarbure insaturé, constitué exclusivement de carbone et d'hydrogène, et présentant obligatoirement une double liaison entre deux atomes de carbone. L'alcène le plus simple est l'éthène, plus couramment appelé éthylèneéthylène, de formule H2C=CH2.
Le nom de l'alcène s'obtient en ajoutant la terminaison -ène au radical de l'alcane correspondant. Ainsi, éthène vient d'éthane, propène de propanepropane.
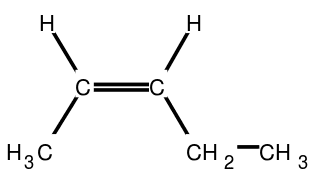
La position de la double liaison au sein de la chaîne carbonée est indiquée par le numéro du carbone qui la porte, ici par exemple : pent-2-ène. © JeanMi, Wikimedia Commons
Production des alcènes
Les alcènes sont rares à l'état naturel. Ils sont incolores et peuvent être gazeux, liquidesliquides ou solidessolides selon la longueur de la chaîne carbonée. Les plus courants dans l'industrie chimique sont l'éthène et le propène. Ils servent de moléculesmolécules de base pour synthétiser des composés plus intéressants, notamment des polyéthylènespolyéthylènes et du polypropylènepolypropylène.
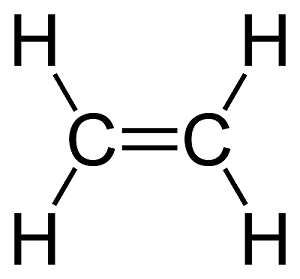
L’éthène, ou éthylène, est le composé organique le plus massivement produit par l’industrie. © Wikimedia Commons
À l'échelle industrielle, les alcènes intéressants (éthène et propène) sont obtenus par craquage des hydrocarbures présents dans le gaz naturelgaz naturel et le naphta. Les alcanes et alcènes obtenus par ce procédé sont séparés par distillationdistillation fractionnée.
Réactivité des alcènes
Les alcènes sont plus réactifsréactifs que les alcanes en raison de la présence d'une double liaison. Ils sont susceptibles de subir une réaction d'addition électrophile sur les carbones porteurs de la double liaison. Cette dernière laisse alors place à une liaison simple. Ainsi, l'addition de dihydrogène sur l'éthène forme de l'éthane.
Comme les alcanes, les alcènes peuvent être détruits par une réaction de combustioncombustion avec le dioxygène, qui produit du dioxyde de carbonedioxyde de carbone et de l'eau.